Введение. Мочекаменная болезнь (МКБ) – социально-экономически значимое заболевание [1]. Нефролитиаз является широко распространенным заболеванием и составляет 30–40% от всего контингента урологических пациентов, госпитализируемых в стационары [1, 2].
В России показатель заболеваемости уролитиазом за период с 2003 по 2013 г. составил 561,7 на 100 тыс. населения и в настоящий момент продолжает неуклонно расти [2].
Нефролитиаз наблюдается чаще всего у трудоспособного населения в возрасте 20–50 лет [1–3]. Ежегодно регистрируется не менее 85 тыс. случаев МКБ, причем 62 тыс. из них – рецидивы камнеобразования [2, 4].
По данным Н. К. Дзеранова, дистанционно-ударноволновая литотрипсия за счет своей высокой эффективности и малой инвазивности получила широкое распространение, но возможны побочные эффекты и осложнения от проведенного лечения. К осложнениям от ДУВЛ относят субкапсулярные и околопочечные гематомы, отеки околопочечной клетчатки в результате воздействия ударной волны, «каменные дорожки», почечную колику.
J. E. Lingeman в 1992 г. описал изменения в почке, возникающие разной степени выраженности при каждой проведенной ДУВЛ. Осложнения могут приводить к склерозированию почечной ткани и последующему снижению функции почки. На сегодняшний день, чтобы провести контроль состояния почечной паренхимы после проведенной ДУВЛ, помимо лучевых методов исследования необходимо определение маркеров повреждения почки: гемоглобина, протеина, β2-микроглобулина, концентрацию токоферола с целью определения травматического воздействия дистанционной литотрипсии на почку [13]. Применение в лечении МКБ высокотехнологичных аппаратных методов, совершенных хирургических тактик по удалению и дезинтеграции конкрементов без применения в дальнейшем медикаментозного и метафилактического лечения, заранее обречено на неудачу [5, 6].
В настоящее время имеется весьма ограниченный набор лекарственных химически синтезированных препаратов, применяемых в лечении МКБ, однако значительную часть в метафилактическом лечении занимают препараты растительного происхождения [6, 7].
В урологической практике лечения МКБ в качестве эффективных препаратов в литокинетической терапии прекрасно зарекомендовали себя растительные добавки на основе терпенов [8–10].
Терпены – класс углеводородов, продуктов биосинтеза с общей формулой (C5H8) n и углеродным скелетом, формально являющихся производными изопрена СН2=С(СН3) – СН=СН2. В больших количествах терпены содержатся в растениях семейства хвойных. Основной фармакологический эффект этих веществ заключается в снятии спазма гладкой мускулатуры чашечно-лоханочной системы и мочеточника. Терпены усиливают почечный кровоток, что приводит к увеличению диуреза. Кроме того, терпены в высоких концентрациях демонстрируют бактериостатический эффект [8, 11, 12].
Отечественным фармакологическим производством, в частности производителем ООО «Полярис», выпущен на рынок новый БАД Ренотинекс®, созданный на основе терпенов и дополненный альфа-токоферола ацетатом (витамином Е).
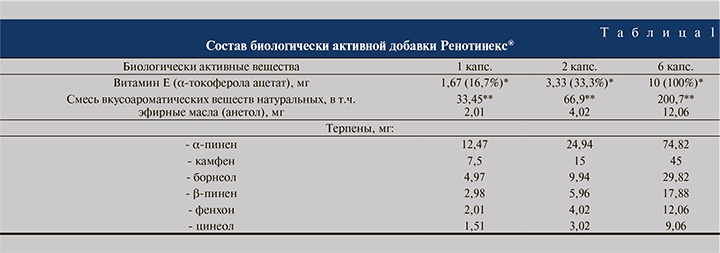
Таким образом, Ренотинекс® – комбинированный БАД растительного происхождения, в состав которого входят биологически активные вещества:
- α-токоферола ацетат (витамин Е), обладающий антиоксидантным действием;
- пинен, имеющий мочегонное и антибактериальное действия;
- камфен, способствующий улучшению тканевого кровотока, помимо прочего, имеющий антибактериальное, спазмолитическое, желчегонное действия;
- борнеол – обладающий сосудорасширяющим (улучшение тканевого кровотока), антибактериальным, обезболивающим, спазмолитическим и желчегонным действиями;
- анетол – проявляющий мочегонное противовоспалительное, антибактериальное, улучшающее тканевой кровоток и желчегонное действия;
- фенхон – природный антисептик;
- цинеол – активно проявляющий антисептическое и спазмолитическое действия.
Количество веществ, поступающих в организм, регулируется количеством принимаемых капсул (см. табл. 1).
Рекомендуемая доза 1–2 капсулы 3 раза в сутки принимается внутрь до еды.
Производителем рекомендовано применение БАДа Ренотинекс® пациентам старше 18 лет: при литокинетической терапии – по 2 капсулы 3 раза в сутки 1–2 месяца, после проведенной ДУВЛ – по 4 капсулы 3 раза в сутки 1–2 месяца и при профилактике повторного камнеобразования рекомендован прием по 2 капсулы 3 раза в сутки 1–2 месяца и более (по назначению врача).
Противопоказанием к приему БАДа Ренотинекс® служит индивидуальная непереносимость компонентов продукта.
В стандарты регистрации БАД не входит определение фармакокинетики и фармакодинамики, а также исследование побочных эффектов.
С учетом появления новой биологической активной добавки на российском рынке представляется целесообразным определение оценки эффективности БАДа Ренотинекс® для пациентов с МКБ после проведенной дистанционной ударно-волновой литотрипсии (ДУВЛ).
Цель исследования: оценить эффективность применения биологически активной добавки Ренотинекс® при комплексном лечении пациентов с нефролитиазом методом дистанционной ударно-волновой нефролитотрипсии.
Материалы и методы. Исследование проводилось на базе Научно-исследовательского института – Краевой клинической больницы № 1 им. С. В. Очаповского. Были обследованы и пролечены 60 пациентов с неосложненной первичной формой МКБ с впервые выявленными (до 1 см) конкрементами. Ни у кого из пациентов не было выраженной соматической сопутствующей патологии. Средний возраст пациентов составил 41,3±4,7 года, 37 пациентов мужского пола.
Критерии исключения из исследования: нефролитиаз при наличии конкрементов более 1 см в диаметре, конкременты, требующие другого вида оперативного лечения (микро- или мини-перкутанная нефролитотрипсия); острые воспалительные заболевания мочевыделительной системы; выраженные нарушения функции почек и печени, обострения заболеваний желудочно-кишечного тракта (ЖКТ).
Все пациенты разделены на две равные группы и пролечены методом дистанционной ударно-волновой нефролитотрипсии. Первая группа – 30 пациентов, в лечении которых на фоне проводимой ударно-волновой нефролитотрипсии применялись БАД Ренотинекс® по 3 дражже 3 р/сут и комплексная терапия с применением спазмолитической противовоспалительной терапии, использования анальгетиков; вторая группа – 30 пациентов, при лечении которых БАД Ренотинекс® не применялся.
Клинический контроль включал стандартные лабораторные и лучевые методы исследования, рекомендованные Европейской и Российской ассоциациями урологов при диагностике и лечении пациентов с МКБ, а также проводились определение концентрации уровня β2-микроглобулина в моче, концентрации токоферола в плазме крови, обязательная оценка боли по визуальной аналоговой шкале; контроль производился на 1-е, 7- и 14-е сутки лечения, прием Ренотинекс® продолжался в течение месяца.
Основным маркером оценки эффективности нефропротективных свойств БАДа Ренотинекс® служило определение показателей β2-микроглобулина в моче. Бета-2-микроглобулин является маркером поражения почечных канальцев и используется в качестве раннего показателя повреждения проксимальных канальцев почек.
Курс наблюдения и лечения составил 1 мес., среднее количество ДУВЛ – 2,6 сеанса в обеих группах на аппарате Richard Wolf Piezolith 3000.
Проведена оценка физико-химической структуры мочевых камней на основе элиминировавшихся фрагментов.
В обеих группах деструктивных процессов в почках выявлено не было.
Статистический анализ результатов проводили с помощью пакета прикладных программ STATISTICA 7.0, используя t-критерий Стьюдента для несвязанных выборок. Различия считали статистически значимыми при p<0,05.
Результаты и обсуждение. За 1-е сутки после ДУВЛ показатели β2-микроглобулина мочи в 1-й группе (94,7±30,5 мг/л) были статистически значимо (p<0,01) меньше, чем во 2-й (157,9±36,1 мг/л). В течение последующих 7 сут. данный параметр начал снижаться в обеих группах при сохранении статистически значимых (p<0,01) различий между группами (рис. 1). На 14-е сутки показатель был статистически значимо (p<0,01) меньше у пациентов 1-й группы (0,7±2,2 мг/л), чем у пациентов 2-й группы (15,1±17,7 мг/л) (рис. 1).
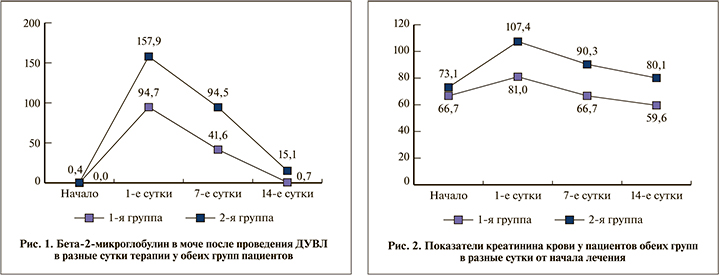
При оценке биохимического анализа крови (мочевина и креатинин), эритроцитурии и лейкоцитов крови выявлено, что в 1-е сутки средние значения креатинина статистически значимо (p<0,01) меньше у пациентов 1-й группы (81,0±15,6 мкмоль/л), чем у пациентов 2-й группы (107,4±15,5 мкмоль/л). При дальнейшем анализе средних значений креатинина на 7-е и 14-е сутки отмечали статистически значимое (p<0,01) снижение у пациентов 1-й группы (66,7±22,6 мкмоль/л) (59,6±9,7 мкмоль/л) соответственно, чем у пациентов 2-й группы (90,3±37,1 мкмоль/л) и (80,1±18,7 мкмоль/л). При анализе в начале лечения средние значения креатинина статистически значимо не различались в обеих группах (рис. 2).
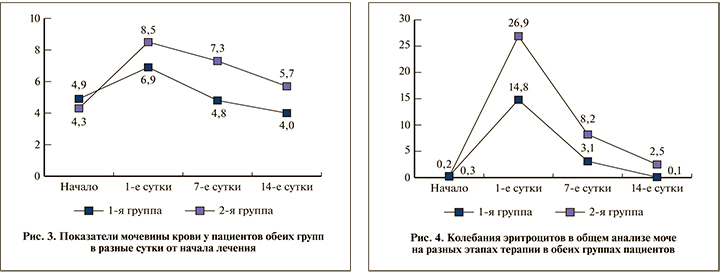
В 1-е, 7, и 14-е сутки после начала терапии средние значения мочевины статистически значимо (p<0,01) меньше у пациентов 1-й группы (6,9±1,5ммоль/л) (4,8±2,1ммоль/л) и (4,0±1,3ммоль/л), чем у пациентов 2-й группы (8,5±0,8 ммоль/л) (7,3±2,8 ммоль/л) и (5,7±2,2 ммоль/л) соответственно. В свою очередь в начале лечения средние значения мочевины крови статистически значимо не различались у больных обеих групп (рис. 3).
До лечения группы не различались по уровню лейкоцитов в общеклиническом анализе крови – 6,8±1,0×109/л и 6,5±1,3×109/л в 1-й и 2-й группах соответственно. На всех сроках наблюдения статистически значимой разницы показателей отмечено не было, она находилась в пределах нормы.
При анализе несвязанных выборок эритроцитов в общем анализе мочи выявлено, что в 1-е сутки средние значения эритроцитов статистически значимо (p<0,01) меньше у пациентов 1-й группы (14,8±5,1 в п/з), чем у пациентов 2-й группы (26,9±13,2 в п/з). На 7-е и 14-е сутки средние значения эритроцитов статистически значимо (p<0,01) снизились в обеих группах, но все же меньше у пациентов 1-й группы (3,1±13,6 в п/з) (0,1±0,4 в п/з), чем у пациентов 2-й группы (8,2±5,8 в п/з) и (2,5±3,1 в п/з) соответственно. В начале лечения средние значения эритроцитов статистически значимо не различались (рис. 4).
При анализе концентрации витамина Е в 1-е сутки средние значения статистически значимо (p<0,01) меньше у пациентов 1-й группы, получавших Ренотинекс® (5,8±3,2мкг/мл), чем у пациентов 2-й группы (8,8±3,8 мкг/мл).
В свою очередь выявлено, что на 14-е сутки средние значения витамина Е статистически значимо (p<0,01) больше у пациентов 1-й группы (13,7±1,9 мкг/мл); у пациентов второй группы изменения по концентрации витамина Е остаются статистически не значимыми относительно первых суток от начала терапии (рис. 5).
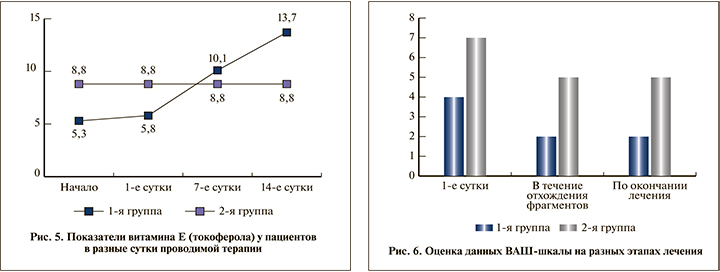
Выраженность боли оценивалась по визуальной аналоговой шкале (ВАШ) в группе пациентов, принимавших Ренотинекс®, отмечено значительное снижение выраженности боли (p<0,01) на фоне отхождения фрагментов конкрементов (рис. 6).
Всем пациентам (n=60) проведена оценка физико-химической структуры мочевых камней на основе элиминировавшихся фрагментов конкрементов для определения вида первичного или рецидивного нефролитиаза. Рентгенофазовый анализ проведен на дифрактометре ДРОН-3М (CuKa-излучение, Ni-фильтр). 90% элиминировавшихся фрагментов состояли из оксалата кальция. В результате проведенного спектрального анализа 76% конкрементов состояли из оксалата кальция моногидрата (Вевеллит), 14% оксалата кальция дигидрата (Ведделлит), 9% конкрементов из дигидрата мочевой кислоты и 1% имели дигидоксофосфат кальция.
В группе пациентов, принимавших БАД Ренотинекс®, отмечена 100%-ная элиминация фрагментов конкрементов в течение месяца, доказанная СКТ-контролем, что статистически значимо (p<0,05) быстрее (в 2 раза) после проведенного комплексного лечения с применением ДУВЛ.
В результате проведенного исследования выяснено, что компоненты БАДа Ренотинекс® обладают антисептическим спазмолитическим противовоспалительным действиями на мочеполовую систему, усиливая почечный кровоток и уменьшая проницаемость капилляров почек, обладают диуретическим эффектом, улучшают функцию почек, обладают нефропротективным действием при применении агрессивного лечебного воздействия (дистанционной ударно-волновой нефролитотрипсии). Антиоксидантный и нефропротективный эффекты – одни из основных эффектов БАДа Ренотинекс®.
Увеличение диуреза, вызванное эфирными маслами (анетол, пинен), происходит за счет вазодилятирующего эффекта на почечные сосуды и улучшения перфузии. Вазодилятирующими свойствами обладают и камфен, борнеол, анетол. Эфирные масла действуют на реабсорбционную способность эпителиальных клеток почечных канальцев. Диуретический эффект природных терпенов связывают с тем, что они, снижая щелочной резерв и смещая реакцию крови в кислую сторону, приводят к сдвигу баланса перераспределения жидкости из тканевого в сосудистый компартмент и освобождающаяся жидкость выводится с мочой.
Противовоспалительный эффект добавки связан преимущественно с таким природным терпеном, как анетол, что происходит за счет ингибирования неспецифической активации системы комплемента, что в результате приводит к торможению синтеза лейкотриенов.
Антибактериальным действием обладает ряд компонентов: пинен, камфен, борнеол, анетол, за счет естественных антисептических свойств. Компоненты БАДа Ренотинекс® жирорастворимы и поэтому основой препарата является витамин Е. Витамин Е (токоферол) – генерическое название группы соединений с 6-хромоноловым кольцом, боковой изопреноидной цепью и биологической активностью а-токоферола, состоит из a-, b-, g-, s-токоферолов, различающихся по месту метилирования хромонолового кольца. Токоферол препятствует пероксидации полиненасыщенных липидов клеточных мембран, что усиливает нефропротективный эффект БАДа Ренотинекс®.
Выводы. Результаты проведенного исследования достоверно демонстрируют, что добавка к комплексной терапии обладает доказанным антисептическим спазмолитическим противовоспалительным действиями на мочеполовую систему, улучшает функцию почек, обладает нефропротективным действием при применении агрессивного лечебного воздействия ДУВЛ и отсутствием выраженных колебаний мочевины, креатинина, эритроцитов и лейкоцитов крови у пациентов, получающих Ренотинекс®.
Концентрация витамина Е в крови увеличивается начиная с 1-х суток и к 14-м суткам становится в двое выше от начального этапа лечения, что препятствует пероксидации полиненасыщенных липидов клеточных мембран, усиливает нефропротективный эффект БАДа Ренотинекс®.
У пациентов, не получавших Ренотинекс®, отмечается большая степень повреждения паренхимы почек, регистрируемая по показателям β2-глобулина в моче пациентов до и после ДУВЛ, и практически нормальные показатели больных, получавших БАД.
В обеих группах деструктивных повреждений паренхимы почек субкапсулярных и паранефральных гематом не выявлено.



