Введение. Начиная с 1980-х гг. и по сегодняшний день дистанционная литотрипсия (ДЛТ) играет важную роль в лечении больных мочекаменной болезнью (МКБ) [1].
В основе метода лежит дезинтеграция конкремента посредством сгенерированных импульсов ударной волны, сфокусированных на конкремент [2]. Разрушение конкремента при помощи ДЛТ – это только первый этап в лечении больного уролитиазом.
Несмотря на то что ДЛТ многие годы активно применяется в урологической практике, считается малоинвазивным методом лечения МКБ; перед специалистами по-прежнему стоит вопрос улучшения эффективности проводимого лечения: снижения количества повторных вмешательств, количества осложнений. Не менее важно проведение терапии, направленной на борьбу с воспалительными изменениями в почке, мочеточнике и окружающих тканях, улучшение гемо- и уродинамики, уменьшение развития рубцово-склеротических процессов, а также на стимуляцию отхождения дезинтегрированных фрагментов конкремента после ДЛТ [3]. С этой целью разработаны классические схемы и подходы, предусматривающие применение α-адреноблокаторов, нестероидных противовоспалительных средств (НПВС), физиопроцедур, а также фитопрепаратов (лекарственных средств, полученных из растительного сырья: трав, целых растений или их экстрактов) [4].
Фитотерапия имеет богатую историю [5]. Первым документальным подтверждением применения лекарственных средств, созданных на основе растений, служит шумерская глиняная плита, на которой более 5000 лет назад было написано 12 рецептов. В книге «Бен-Цао», посвященной корням и травам, изданной в 2500 г. до н.э. китайским императором Шень Нун, описано 365 лекарственных средств. В папирусе Эберса (1550 г. до н.э.) насчитывалось уже 800 рецептов. Со временем количество растительных препаратов увеличивалось, в работах греческих (Гиппократ, 460–370 г. до н.э.), римских (Антонио Муса, 23 г. до н.э.), арабских (Авиценна, 980–1037 г. н.э.) врачей их насчитывается уже более тысячи. Первое упоминание о развитии травничества на Руси было в XII в. н.э., а первое российское издание, посвященное фитотерапии, – это Руководство к познанию лекарственных трав, опубликованное в 1781 г. Андреем Тимофеевичем Болотовым [6]. С тех пор фитотерапия не утратила своей значимости в лечебном процессе и ее продолжают широко применять врачи всех специальностей [7]. На сегодняшний день известно более 21 тыс. растений, используемых в качестве субстрата для приготовления медикаментозных препаратов. При этом в лечении больных МКБ используют около 30 трав: марену красильную, бруснику, петрушку, зверобой, руту, толокнянку, лопух, аир, листья березы, семена укропа, землянику, хвощ полевой и др. [8]. Кроме того, отмечается тенденция к увеличению числа работ, посвященных оценке эффективности применения фитотерапии при МКБ, в том числе на базе систем дистанционного мониторинга параметров общего анализа мочи (ОАМ) [9, 10].
Зачастую в лечебной практике урологи с целью усиления литокинетического эффекта используют препараты, представляющие комбинацию лекарственных растений [11, 12]. Одним из новых препаратов, обладающих такими свойствами, является биологически активная добавка к пище (БАД) «Ренотинекс» (OOO «Полярис», Россия).
В его состав входят смесь вкусоароматических веществ (эфирное масло [анетол]; терпены: альфа-пинен, камфен, борнеол, бета-пинен, фенхон, цинеол), витамин Е (α-токоферола ацетат), а также оливковое масло, желатин, глицерин, вода, альгинат натрия, стеариновая кислота, этилцеллюлоза, гидроксид аммония, среднецепочечные триглицериды и олеиновая кислота.
C учетом состава и новизны БАД «Ренотинекс» на фармацевтическом рынке отделом МКБ НИИ урологии и интервенционной радиологии им. Н. А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» МЗ России проведено исследование, целью которого стало изучение эффективности применения БАД «Ренотинекс» пациентами с камнями почек в качестве препарата, способствующего литокинетической терапии.
Материалы и методы. В течение 5 мес. проведено клиническое испытание БАД «Ренотинекс» в составе комплексной литокинетической послеоперационной терапии взрослых больных МКБ после ДЛТ камней почек.
В исследование вошел 41 пациент, отвечавший критериям включения. Путем рандомизации пациенты были разделены на 2 группы: основную (n=21; 8 мужчин и 13 женщин) и контрольную (n=20; 7 мужчин и 13 женщин). Средний возраст пациентов основной и контрольной групп составил 51,6 и 56,3 года соответственно.
Критерии включения:
- Наличие камня/камней почки до 15 мм без обострения хронической инфекции мочевыводящих путей;
- Возраст пациентов 18–75 лет.
Критерии исключения:
- Пациенты, которым показано экстренное оперативное вмешательство;
- Пациенты с инфекционными осложнениями;
- Пациенты со стойким болевым синдромом в поясничной области, не купируемым анальгетиками;
- Длительность локализации конкремента на одном месте более 1 мес.;
- Пациенты, имевшие непереносимость компонентов БАДа «Ренотинекс»;
- Возраст: не младше 18 лет, не старше 75 лет.
Исследование одобрено локальным этическим комитетом. Все пациенты подписали информационное согласие.
Пациенты основной группы в течение 1 мес. получали БАД «Ренотинекс» по 2 капсулы 3 раза в сутки. Наряду с БАДом, согласно клиническим рекомендациям по лечению МКБ/почечной колики (2019) [13, 14], им назначили стандартную литокинетическую терапию: НПВС диклофенак по 1 таблетке/1 свече (50 мг) при болях; α1-адреноблокатор тамсулозин по 1 капсуле (0,4 мг) утром. Пациенты контрольной группы получали только стандартную литокинетическую терапию.
Эффективность проводимой терапии оценивали по данным, полученным до начала лечения, через 2 и 4 нед. после его начала. С помощью УЗИ почек выявляли гидронефроз, определяли максимальный размер чашечек, лоханки, наличие конкремента в ЧЛС и его локализацию, а по данным обзорной урографии/компьютерной томографии без контрастного усиления определяли наличие конкремента в проекции почки или мочеточника, его размер и локализацию. Кроме того, выполняли общий анализ крови с оценкой уровня гемоглобина, содержания эритроцитов и лейкоцитов, ОАМ с оценкой количества эритроцитов и лейкоцитов. Статистический анализ полученных данных осуществляли с помощью критерия Стьюдента и метода углового преобразования Фишера посредством компьютерной программы Statistica 12.0 (StatSoft, США).
Результаты. Исходные данные по локализации и размерам конкрементов в группах были практически идентичными. Чаще всего конкременты определялись в лоханке – в 55 и 52% наблюдений в основной и контрольной группах соответственно, несколько реже – в нижней группе чашечек (в 35 и 33%), реже всего – в средней группе чашечек (10 и 14% случаев).
Показатели общего анализа крови в группах исследования были сопоставимыми. Что касается ОАМ, группы статистически значимо различались только по содержанию лейкоцитов (см. таблицу).
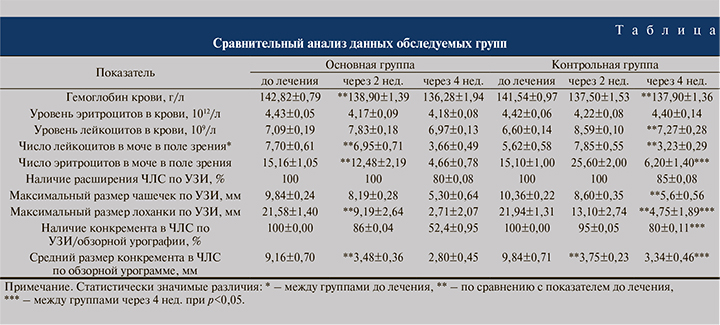
Через 2 нед. после начала лечения в основной группе зафиксировано снижение уровней гемоглобина крови, лейкоцитов и эритроцитов в моче, а также значительное уменьшение размеров лоханки с 21,58±1,40 до 9,19±2,64 мм, средний размер конкремента уменьшился на 62% – с 9,16±0,70 до 3,48±0,36 мм. В контрольной группе на фоне стандартной терапии также отмечено незначительное снижение уровня гемоглобина крови, достоверное увеличение числа лейкоцитов и эритроцитов в моче. Средний размер конкремента, по данным обзорной урографии, уменьшился на 62 % (см. таблицу).
При проведении сравнительного анализа результатов лечения в основной и контрольной группах, полученных через 2 нед. после начала исследования, выявлены различия в уровнях эритроцитурии, лейкоцитурии, а также показателях максимального расширения лоханки по данным УЗИ, которые в группе приема БАДа «Ренотинекс» оказались статистически значимо ниже (p<0,05) (см. таблицу).
 Через 4 нед. после начала исследования достоверные межгрупповые различия касались следующих параметров: числа эритроцитов в моче, размеров лоханки и наличия конкрементов в ЧЛС, зафиксированных по данным УЗИ и обзорной урографии. При этом показатель среднего размера камня был меньше в основной группе (см. таблицу).
Через 4 нед. после начала исследования достоверные межгрупповые различия касались следующих параметров: числа эритроцитов в моче, размеров лоханки и наличия конкрементов в ЧЛС, зафиксированных по данным УЗИ и обзорной урографии. При этом показатель среднего размера камня был меньше в основной группе (см. таблицу).
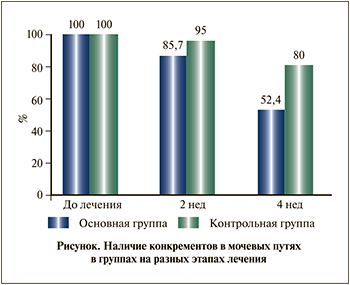
Резидуальные фрагменты конкрементов в ЧЛС в обеих группах локализовались исключительно в нижней группе чашечек, однако число оставшихся фрагментов в основной группе было почти в 1,5 раза меньше, чем в контрольной: 11 против 16 (p<0,05). В целом в результате литокинетической терапии за 4 нед. полностью очистить ЧЛС от конкрементов после ДЛТ камней почек в основной группе удалось 47,6% пациентов, в контрольной –20% (см. таблицу. Литокинетическая эффективность комбинированной терапии в сочетании с БАД «Ренотинекс» после выполненной ДЛТ оказалась выше, чем только стандартная литокинетическая терапия (см. рисунок).
Заключение. Результаты проведенного исследования позволяют сделать вывод, согласно которому эффективность комбинированного лечения с использованием БАД «Ренотинекс» по сравнению со стандартной литокинетической терапией с использованием НПВС и α-адреноблокаторов в отхождении фрагментов конкрементов почек после ДЛТ оказалась выше на 27,6%. Достоверность различий была достигнута к 4-й неделе терапии.



