Введение. Гипоспадия считается распространенным врожденным пороком развития наружных половых органов у мальчиков и встречается приблизительно c частотой 1 на 300 новорожденных. Несмотря на то что в патологический процесс могут быть вовлечены практически все ткани полового члена, один критерий, а именно расположение наружного мочеиспускательного отверстия, наиболее значим и чаще других используется для классификации. Примерно 70% пациентов имеют дистальную форму аномалии: смещение меатуса в проксимальном направлении от незначительной эктопии в пределах головки до дистальной части ствола полового члена. У 10% детей отмечается срединная форма порока – эктопия меатуса на ствол полового члена по вентральной поверхности. Еще 20% пациентов имеют проксимальную гипоспадию, когда наружное мочеиспускательное отверстие смещено на мошонку или промежность. Вторым важным фактором, который учитывается при хирургической коррекции порока, является наличие вентрального искривления полового члена. При этом чем проксимальнее смещен меатус при гипоспадии, тем больше может быть выражено искривление [1].
Впервые термин «уретральная площадка» ввел в 1954 г. английский исследователь T.W. Glenister, изучавший формирование пола, развитие клоаки и урогенитального синуса у эмбрионов человека [2]. Долгое время ткани по вентральной поверхности полового члена считали патологическими и удаляли как причину искривления полового члена при проксимальных формах гипоспадии. Чаще других использовались «укорачивающие» методы ортопластики типа операции Nesbit, когда для устранения искривления полового члена наносились плицирующие швы на противоположной от искривления дорсальной поверхности белочной оболочки кавернозных тел. Однако иссечение вентральных тканей считалось важным этапом ортопластики. В настоящее время об уретральной площадке говорят как об отдельной анатомической структуре – «полоске ткани, идущей дистально от гипоспадического меатуса к вершине головки» [3]. Первым, кто заговорил о сохранении уретральной площадки, был J. Duckett в 1987 г., предлагая использовать уретральную площадку в качестве задней стенки артифициальной уретры при дистальных и срединных формах гипоспадии без искривления полового члена [4]. Уже в 1994 г. тот же J. Duckett, обобщив опыт почти 400 пластик уретры авторским методом Onlay Island Flap (OIF), указал на изменение подходов, отказываясь видеть причину искривления полового члена в уретральной площадке и расширяя показания к операции с сохранением последней [5].
Пионером в изучении патологической анатомии полового члена при гипоспадии и морфологии уретральной площадки как отдельной анатомической структуры стал американский детский хирург L.S. Baskin. Его исследование было целиком посвящено гистологическому и иммуногистохимическому анализу тканей полового члена, при этом использовались разные методы окраски сосудов, нервов, гладкомышечных клеток и коллагеновых волокон. Однако лишь 3 половых члена из 33 исследуемых были с гипоспадией, при этом 32 были пенисами эмбрионов и лишь 1 половой член с гипоспадией от умершего новорожденного [6]. В исследуемом материале последовательно были найдены все структуры нормальной уретры, что послужило морфологическим доказательством целесообразности сохранения уретральной площадки.
Еще один сторонник сохранения уретральной площадки при пластике уретры, W. Snodgrass, почти одновременно с L.S. Baskin провел собственное исследование субдермального биопсийного материала, окрашенного гематоксилином и эозином, взятого во время операции у 17 пациентов с гипоспадией, и не обнаружил никаких патологических тканей [3].
Хирургическая коррекция гипоспадии является реконструктивно-пластическим вмешательством, что определило вектор научных исследований в этой сфере как поиск оптимальных методов перемещения тканей. Гистологическое изучение операционного материала по-прежнему не является рутинным. Становится очевидным, что после работ L.S. Baskin и W. Snodgrass фундаментальные исследования, которые были бы сфокусированы на изучении уретральной площадки, были практически прекращены. А в русскоязычной литературе подобные работы нами не были обнаружены вовсе. В то же время необходимо отметить, что методы уретропластики с сохранением уретральной площадки находят все больше сторонников во всем мире [7].
Цель исследования: изучить микроструктуру уретральной площадки у пациентов с проксимальной формой гипоспадии для обоснования использования тканей вентральной поверхности полового члена при создании артифициальной уретры.
Материалы и методы. Исследование проведено с соблюдением этических норм в соответствии с Хельсинкской декларацией Всемирной медицинской ассоциации «Этические принципы проведения научных медицинских исследований с участием человека».
В тех случаях, когда мы оперируем пациентов с гипоспадией без выраженного искривления, которое возможно устранить методами дорсальной пликации, полностью сохраняем уретральную площадку и создаем из нее артифициальную уретру методом Tubularized Incised Plate (TIP).
В ситуации, когда искривление кавернозных тел составляет более 30–40° – обычно это встречается у пациентов с проксимальными формами порока, для того чтобы провести вентральную корпоропластику, нам необходимо полностью пересечь уретральную площадку. При этом нередко для проведения первого этапа операции Bracka требуется частичное или полное удаление уретральной площадки.
Десяти пациентам с проксимальной формой гипоспадии и выраженным искривлением полового члена было выполнено полное иссечение уретральной площадки от нативного меатуса (локализованного в члено-мошоночном углу) до венечной борозды с дальнейшим гистологическим исследованием. Контрольную группу составили фрагменты нормальной уретры, полученные при аутопсии трех тел.
Операционный материал предварительно фиксировали в 10%-ном забуференном формалине, обезвоживали в батарее спиртов и заливали в парафин. Каждый образец был обработан рядом различных способов. Срезы толщиной 3–5 мкм окрашивали гематоксилином и эозином и пикрофуксином по Ван Гизону. Кроме того, проведено иммуногистохимическое (ИГХ) исследование с антителами к CD34, фибронектину, коллагенам I, III и IV типов, а также α3- и α5-субъединицам коллагена IV типа. Для ИГХ-типирования гладких миоцитов применяли α-гладкомышечный актин. Использовали мышиные и кроличьи моноклональные антитела Thermo Scientific (США).
При проведении ИГХ-исследования в качестве позитивного контроля для каждого маркера использовали ткани и органы, рекомендованные производителем антител, в качестве негативного контроля – исключение первичного антитела. Исследование проводили в соответствии с протоколами производителя, в которых для каждого первичного антитела установлены оптимальное рН, время экспозиции в демаскировочном буфере, оптимальное разведение и время экспозиции с диаминобензидином. Срезы докрашивали гематоксилином Майера. Интерпретацию результатов ИГХ-окрашивания проводили, исходя из наличия и интенсивности окрашивания ткани. Критерии балльной оценки интенсивности окрашивания: 0 баллов – негативное окрашивание, 1 балл – слабая интенсивность (+), 2 балла – умеренная интенсивность (++), 3 балла – сильная интенсивность (+++).
Оценку гистологической картины осуществляли методом световой микроскопии на микроскопах Primo Star («Carl Zeiss», Германия) и DC200 («Leica», Германия).
Результаты. Фрагменты уретральной площадки пациентов с гипоспадией имели однотипное строение. В биопсийном материале под покровным многослойным плоским эпителием обнаруживалась рыхлая волокнистая соединительная ткань, богатая кровеносными и лимфатическими сосудами. Соединительнотканные волокна тонкие, нежные, неупорядоченно расположены, образовывали крупноячеистые структуры. Тинкториальные свойства коллагеновых волокон сохранены. Соединительная ткань уретральной площадки при гипоспадии во время окрашивания гематоксилином и эозином, а также пикрофуксином по Ван Гизону не отличалась от таковой в нормальной уретре (рис. 1).
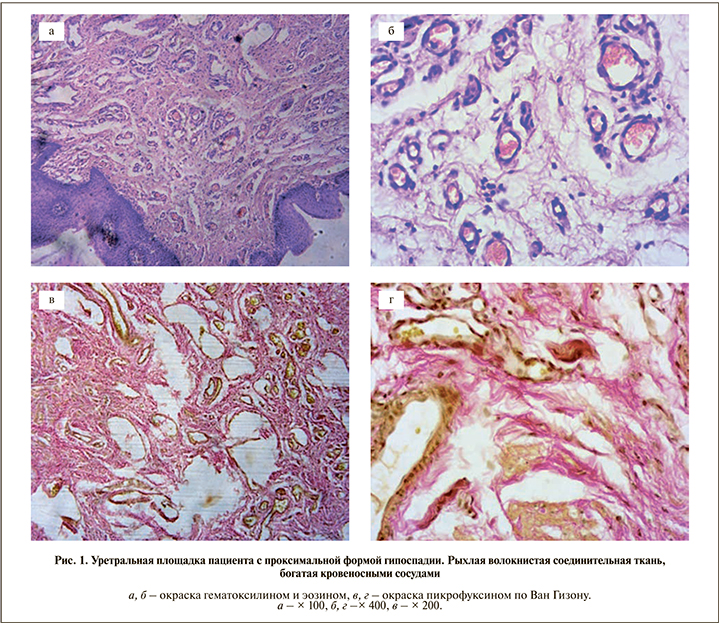
Среди соединительнотканных волокон определялись многочисленные клетки, морфологически определяемые как гладкомышечные. Пикрофуксином по ван Гизону они окрашивались в желтый цвет, при ИГХ-идентификации давали положительную реакцию на α-гладкомышечный актин. Гладкомышечные клетки формировали хаотично расположенные пучки (рис. 2).
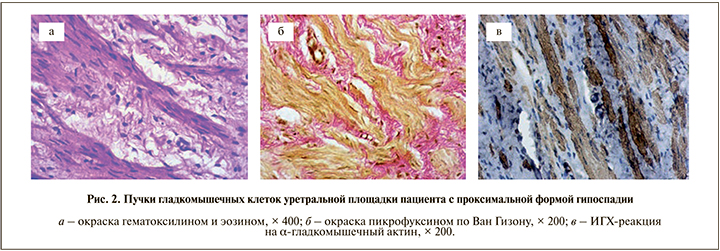
Обнаружены многочисленные кровеносные сосуды различных типов: отдельные артериолы, значительное число венул и щелевидных сосудистых полостей, выстланных эндотелиальными клетками. В стенке крупных сосудов выявлялись α-гладкомышечный актиниммунопозитивные клетки. Многие сосуды были полнокровными (рис. 1 б, рис. 3 а).
Отдельные железистые структуры округлой формы окружены соединительнотканными волокнами и гладкомышечными клетками (рис. 3 б).
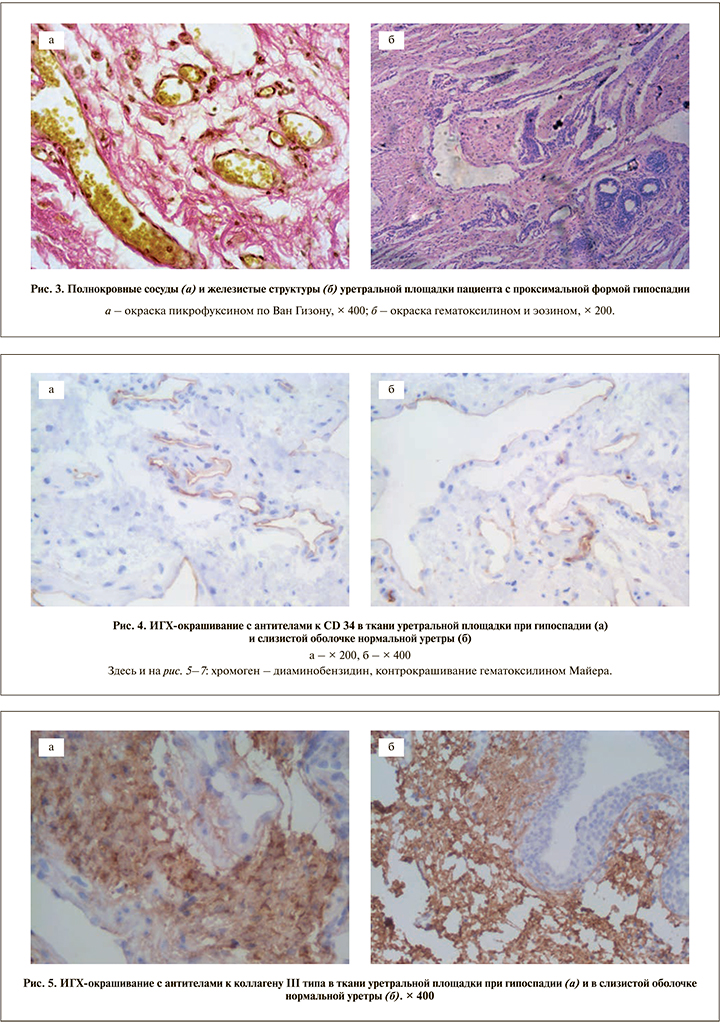
Экспрессия CD 34 характеризовалась окрашиванием в коричневый цвет эндотелиальных клеток кровеносных сосудов, что позволяло оценить их плотность. Характер васкуляризации уретральной площадки при гипоспадии не отличался от таковой в слизистой оболочке нормальной уретры (рис. 4).
При ИГХ-окрашивании характер экспрессии коллагена I, III и IV типов, α3- и α5-субъединиц коллагена IV типа и фибронектина в ткани уретральной площадки пациентов с гипоспадией и в слизистой оболочке нормальной уретры был однотипными. Экспрессия коллагена I и III типов выявлялась во всех исследованных случаях. ИГХ-окрашивание наблюдалось в рыхлой соединительной ткани собственной пластинки и подслизистой основе уретральной площадки при гипоспадии и в нормальной слизистой оболочке уретры. Экспрессия коллагена III типа была наиболее выраженной (рис. 5).
ИГХ-исследование с антителами к коллагену IV типа, а также к α3- и α5-субъединицам коллагена IV типа выявило негативное окрашивание во всех случаях как в нормальной слизистой оболочке уретры, так и в уретральной площадке (рис. 6).
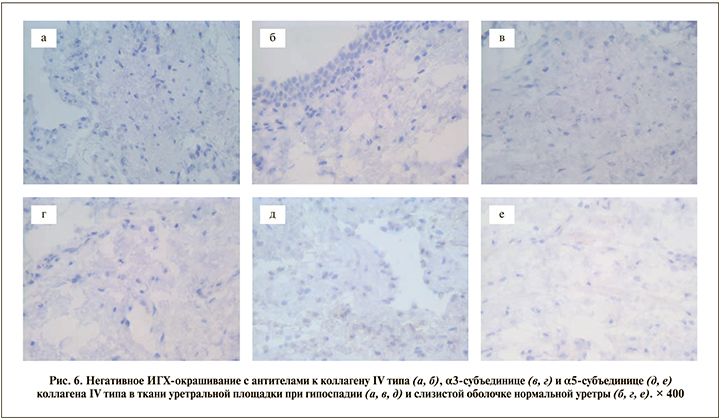
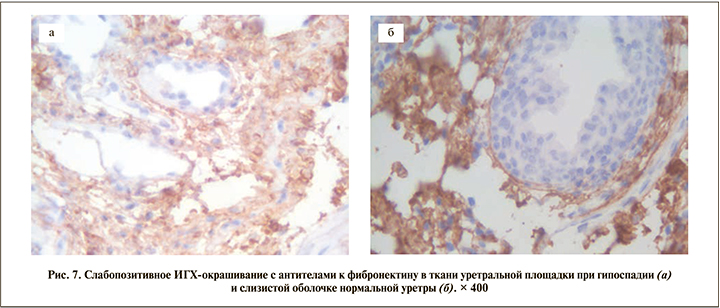
ИГХ-исследование с антителами к фибронектину (как к маркеру фиброза тканей) выявило слабопозитивное окрашивание рыхлой соединительной ткани во всех изученных образцах (рис. 7).
Таким образом, строение уретральной площадки по результатам исследования радикально отличается от простых рубцовых тканей. Несмотря на то что в микропрепаратах не определялось четкой направленности расположения гладкомышечных клеток и коллагеновых волокон, для всех образцов, полученных от пациентов, было характерно однотипное упорядоченное строение. Можно предположить, что уретральная площадка не тубуляризировалась (не замкнулась) в процессе эмбрионального развития и является расщепленным спонгиозным телом уретры, покрытым эпителием, так как имеет гомологичную цитоархитектонику.
Обсуждение. Поиск оптимального пластического материала для реконструкции уретры при гипоспадии продолжается. В разное время это были лоскуты на питающих сосудах различной локализации, тубуляризированные трансплантаты кожи, слизистой ротовой полости, мочевого пузыря и т.д. Примечательно, что история хирургического лечения начиналась с уретропластики из вентральных тканей полового члена, а значит, из уретральной площадки [8].
По нашему убеждению, для получения оптимального результата при создании артифициальной уретры необходимо использовать ткани, максимально приближенные по своим характеристикам к нормальной уретре. Однако исследования, направленные на изучение анатомии гипоспадического полового члена, крайне малы и ограничены небольшими группами пациентов. Это может быть связано с трудностями забора тканей без потери необходимого количества пластического материала. Вторая причина редкости подобных исследований, как нам кажется, связана с тем, что реконструкция уретры проводится у ребенка в раннем возрасте и краткосрочные результаты уретропластики бывают удовлетворительными, а неудовлетворенность отдаленными результатами через 15–20 лет уже наступает на приеме у хирургов другого поколения. У практикующих хирургов отсутствует ясная мотивация проводить фундаментальный поиск и ставить, в частности, перед морфологами конкретные практические задачи.
Мы обнаружили сравнительные исследования, посвященные изучению фасции dartos у пациентов с гипоспадией и нормальным половым членом [9, 10], которые теоретически могут коррелировать с исследованиями уретральной площадки. Так, у пациентов с гипоспадией в 70% случаев по сравнению со здоровыми мальчиками, кому без медицинских показаний выполнялось обрезание крайней плоти, отмечалось отклонение расположения гладкомышечных клеток в фасции dartos [9]. У пациентов с гипоспадией коллагеновые волокна оказались более толстыми, а их количество снижено по сравнению с таковым у пациентов с нормальным половым членом. При этом концентрация коллагена III типа оказалась более высокой у пациентов с гипоспадией [10].
Несмотря на вышесказанное, результаты гистологического исследования уретральной площадки свидетельствуют о наличии в ней всех компонентов нормальной уретры, а именно: эпителия, кровеносных сосудов, гладкомышечных клеток и нормальных коллагеновых волокон I и III типов, отсутствие патологического коллагена IV типа. Это позволяет сделать вывод, согласно которому уретральная площадка является расщепленным спонгиозным телом, покрытым эпителием. Наличие гладкомышечных клеток в уретральной площадке может говорить о качественно иных резистентных свойствах артифициальной уретры по сравнению, например, с тубуляризированным препуциальным лоскутом.
Заключение. Результаты последующих исследований по изучению анатомии уретральной площадки могут стать хорошей основой при разработке стратегии выбора пластического материала для уретропластики. В ходе данной работы показано, что вентральные ткани полового члена не содержат патологических или рубцовых структур. Приближенная к нормальной цитоархитектоника делает уретральную площадку предпочтительным материалом для пластики уретры с теоретически сходными биорезистентными свойствами.



