Лечение стриктур уретры остается одной из актуальных проблем современной урологии. Распространенность данного заболевания составляет 229–627 случаев на 100 тыс. мужчин [1]. «Золотым» стандартом лечения коротких (не более 2 см) стриктур бульбозного отдела уретры считается пересечение уретры в пределах здоровых тканей с последующим формированием концевого анастомоза [2]. Данное оперативное вмешательство позволяет достигать успеха более чем в 90% случаев, но требует пересечения уретральной артерии, что приводит к ухудшению кровоснабжения дистальных отделов уретры [3]. Это является существенным недостатком, так как максимальное сохранение кровоснабжения в зоне оперативного вмешательства – один из ключевых факторов успеха операции [4]. Другим негативным эффектом пересечения бульбозного отдела уретры является повреждение нервных волокон, проходящих вдоль уретры, в результате которого у 18,0–22,5% пациентов после такой операции развиваются различные сексуальные нарушения [5, 6]. Эти данные стали причиной дискуссии о преимуществах и недостатках уретропластики с пересечением уретры и продиктовали необходимость разработки способов снижения травматизации тканей при уретропластике. Впервые данный аспект был масштабно обсужден на конгрессе Американской урологической ассоциации в 2009 г. [7].
С целью снижения риска вышеуказанных побочных эффектов при пересечении спонгиозного тела уретры G. H. Jordan et al. [8 , 9] была предложена оригинальная идея уретропластики без пересечения спонгиозного тела. Настоящее исследование посвящено анализу результатов применения подобных методик в мировой практике.
В международной базе данных PubMed и Российском индексе научного цитирования (РИНЦ) осуществлен поиск источников литературы по исследованиям с применением анастомотической уретропластики без пересечения спонгиозного тела. В дальнейший анализ включали только те исследования, в которых анастомотическую уретропластику без пересечения спонгиозного тела осуществляли с использованием одной или нескольких нижеуказанных методик:
- техники уретропластики по принципу Heineke–Mikulicz, при которой уретру рассекают над областью стриктуры в продольном направлении и затем ушивают в поперечном направлении, не иссекая фиброзную ткань [10];
- сосудосберегающей анастомотической пластики по технике Jordan, при которой пораженный участок слизистой уретры циркулярно резецируют с сохранением вентральной части спонгиозного тела, а концы здоровой слизистой спатулируют и соединяют путем формирования циркулярного анастомоза [8, 9];
- техники уретропластики по Andrich и Mundy [11], согласно которой после продольного рассечения уретры по дорсальной поверхности проводят иссечение пораженной слизистой внутри просвета уретры с сохранением подлежащего спонгиозного тела и по вентральной полуокружности внутри просвета уретры формируют анастомоз между здоровыми концами слизистой уретры, а продольный разрез уретры по дорсальной полуокружности ушивают поперечно по принципу Heineke–Mikulicz.
В настоящий анализ не включены различные виды аугментационной анастомотической уретропластики без пересечения спонгиозного тела [12–15].
При указании причин образования стриктур исходили из четырех основных видов этиологии приобретенных стриктур уретры: идиопатической, ятрогенной, воспалительной и травматической [16–18]. К ятрогенным отнесены стриктуры уретры, возникшие в результате различных лечебно-диагностических манипуляций: трансуретральных операций на нижних и верхних мочевыводящих путях, травматичного введения или продолжительного нахождения катетера в уретре, операций по поводу гипоспадии, хирургического лечения и лучевой терапии рака предстательной железы, открытых операций по поводу аденомы предстательной железы, инстилляций в уретру химически агрессивных веществ по поводу заболеваний, передающихся половым путем, и др. [19–21].
В базах данных PubMed и РИНЦ найдено 14 оригинальных исследований (13 зарубежных и 1 отечественное), в которых представлен опыт применения анастомотической уретропластики без пересечения спонгиозного тела с использованием одного либо нескольких вышеуказанных техник (табл. 1). В эту серию работ вошли как исследования, посвященные обособленному изучению результатов анастомотической уретропластики без пересечения спонгиозного тела, так и работы, в которых наряду с данной операцией изучались результаты применения других техник уретропластики (анастомотической уретропластики с пересечением спонгиозного тела, аугментационной анастомотической уретропластики без пересечения спонгиозного тела и т.д.). Однако в табл. 1 общее количество прооперированных (n) обозначает число пациентов, которым в указанном исследовании была выполнена анастомотическая уретропластика без пересечения спонгиозного тела. Этиологические факторы в ряде представленных исследований были указаны не для всех, а только для части пациентов, а в одной работе были приведены данные по всей выборке пациентов, включившей помимо анастомотической уретропластики без пересечения спонгиозного тела и другие виды уретропластики. В подобных ситуациях в таблице дано пояснение об особенностях представленных сведений об этиологии стриктур уретры. Не во всех исследованиях послеоперационные осложнения были охарактеризованы в соответствии с классификацией Clavien–Dindo [22]. С учетом важности оценки влияния изучаемой техники уретропластики на развитие эректильной дисфункции (ЭД) сведения о частоте возникновения данного осложнения вычленены из общей группы осложнений и представлены отдельной графой. Показатель «0» по частоте ЭД означает отсутствие этого осложнения в послеоперационном периоде, а заключение «Нет данных» указывали в том случае, когда в исследовании специально не оценивали влияние оперативного вмешательства на эректильную функцию.
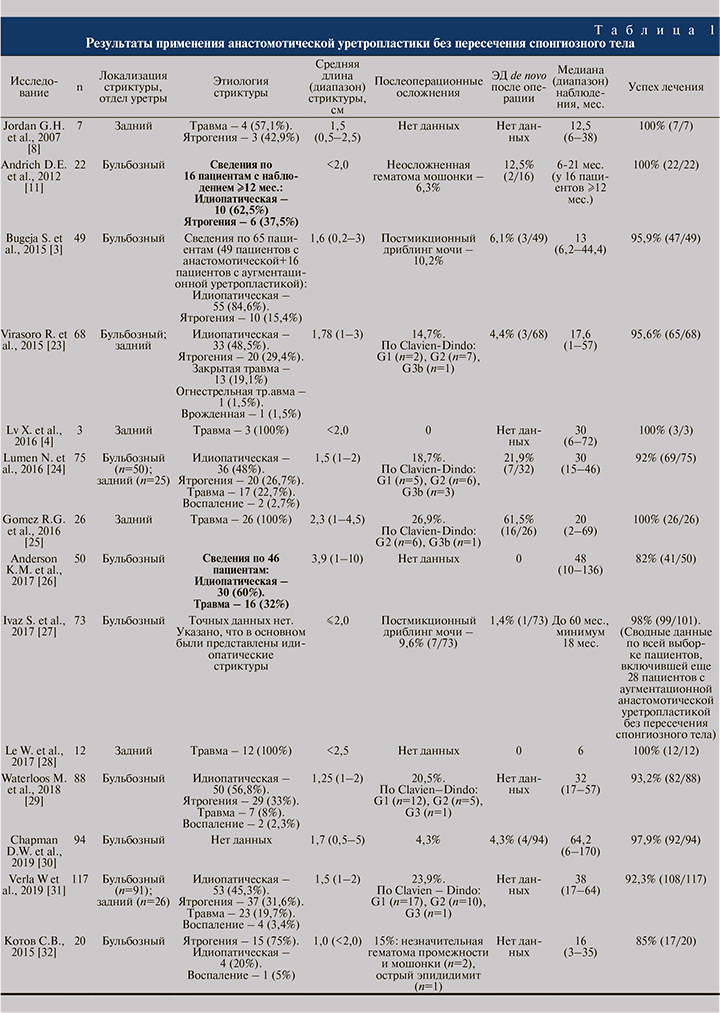
К настоящему времени мировой опыт применения анастомотической уретропластики без пересечения спонгиозного тела при стриктурах уретры суммарно составляет 704 наблюдения. При этом подавляющее большинство случаев применения такой техники приходится на стриктуры бульбозного отдела уретры (около 85% всех наблюдений), а меньшая доля (около 15%) – на стриктуры заднего отдела уретры. Средняя протяженность стриктуры уретры практически во всех исследованиях составляла менее 2 см и только в двух работах превышала этот порог, достигнув 2,3 и 3,9 см соответственно.
Анализ показал, что рассматриваемая техника уретропластики может быть успешно применена практически при всех этиологических вариантах стриктур уретры. Частота послеоперационных осложнений во всей указанной серии работ составила в среднем 13,7%. Необходимо отметить, что в основном имели место осложнения легкой степени, соответствовавшие категории G1 по классификации Clavien–Dindo. Оценку влияния данного вида оперативного лечения на развитие ЭД в послеоперационном периоде проводили в 10 из 14 исследований, по результатам которых частота ЭД de novo составила в среднем 13,4%. Успех лечения при использовании анастомотической уретропластики без пересечения спонгиозного тела оказался очень высоким, а средний показатель эффективности коррекции стриктуры уретры составил 95% при диапазоне значений от 82 до 100%. Следует добавить, что такие впечатляющие результаты были достигнуты при достаточно длительных сроках послеоперационного наблюдения – медиана наблюдения для всей серии работ составила 27 (6–64) мес.
Помимо отмеченных показателей, подтвердивших потенциальную выгоду от использования анастомотической уретропластики без пересечения спонгиозного тела, в ряде исследований получены данные о преимуществе данной техники по некоторым важным аспектам перед анастомотической уретропластикой с пересечением спонгиозного тела при их прямом сравнительном анализе. Например, W. Lee et al. [28] сравнили результаты использования этих техник при стриктурах задней уретры. При уретропластике без пересечения спонгиозного тела ни у одного пациента не отмечено рецидивов стриктуры, а также не наблюдали ухудшения показателей Международного индекса эректильной функции (IIEF-5) и индекса качества жизни (QoL). При использовании традиционной уретропластики с пересечением спонгиозного тела установлено значимое ухудшение значений IIEF-5 и QoL в целом по этой группе пациентов, а у 1 из 11 пациентов имел место рецидив стриктуры уретры (табл. 2).
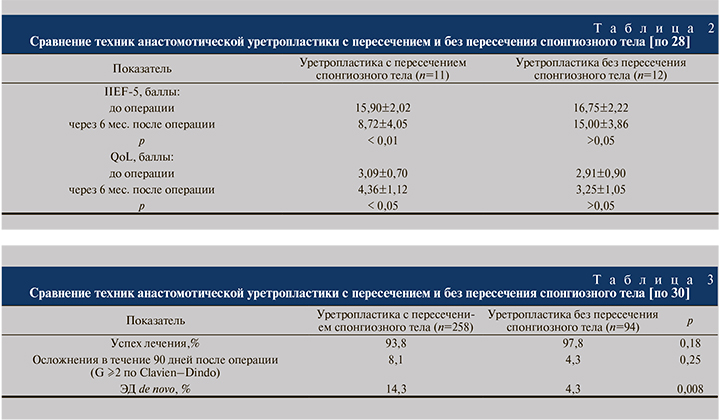
В аналогичной работе, выполненной D. W. Chapman et al. [30], при использовании методики без пересечения спонгиозного тела отмечен достоверно меньший риск возникновения сексуальных нарушений, хотя по эффективности лечения и частоте послеоперационных осложнений существенных различий между техниками установлено не было (табл. 3).
В исследовании M. Waterloos et al. [29] не выявлено статистически значимых различий между данными методиками по успеху операции и частоте осложнений, однако для техники без пересечения спонгиозного тела были характерны достоверно лучшие показатели продолжительности оперативного вмешательства, сроков госпитализации и длительности нахождения уретрального катетера (табл. 4).

В исследовании K. M. Anderson et al. [26] проведено сравнение этих двух методик только по успеху операции. Среди 102 пациентов после анастомотической уретропластики с пересечением спонгиозного тела эффективность лечения составила 83%, среди 50 пациентов без пересечения спонгиозного тела – 82% (p=0,83).
На основании полученных результатов можно заключить: анастомотическая уретропластика без пересечения спонгиозного тела за счет сохранения кровоснабжения и иннервации дистальных отделов уретры и головки полового члена позволяет обеспечить высокие показатели успешности лечения и сохранения сексуальной функции, по которым данная методика в целом превосходит анастомотическую уретропластику с пересечением спонгиозного тела. Тем не менее относительно небольшой опыт применения анастомотической уретропластики без пересечения спонгиозного тела в мировой практике и малое число научных исследований в этой области диктуют необходимость дальнейшего изучения различных аспектов использования данной перспективной методики в лечении стриктур уретры. В связи с этим актуальной задачей представляются критическая оценка указанной техники и поиск путей ее оптимизации.
Во всех описанных в мировой литературе методиках анастомотической уретропластики без пересечения спонгиозного тела используют дорсальный доступ к уретре. На наш взгляд, такой подход обладает рядом недостатков. Во-первых, выполняемые при таком доступе полная мобилизация бульбозного отдела уретры и разворачивание уретры для обнажения дорсальной поверхности сопровождаются риском повреждения артериальных сосудов, расположенных вдоль уретры, и возникновения кровотечения в ходе операции. Во-вторых, не обеспечивается полноценное выделение дорсальной поверхности из-за невозможности полного разворота уретры в данной области вследствие особенностей анатомо-топографического строения этой зоны. Отмеченные факторы обусловливают повышенную кровоточивость в ходе оперативного вмешательства и образование узкой и глубокой зон на дорсальной поверхности бульбозного отдела уретры, ограничивающей обзор операционного поля и манипуляционные действия хирурга. Вследствие этого возможности радикального иссечения пораженной части слизистой уретры и осуществления полноценного соединения здоровых концов уретры снижаются, что сопряжено с довольно высоким риском интра- и послеоперационных осложнений, а также рецидива стриктуры уретры. Исходя из этих обстоятельств, нами разработан новый подход к выполнению уретропластики без пересечения спонгиозного тела, обеспечивающий лучшие условия для обзора зоны операции, максимального иссечения пораженных тканей и полноценного соединения здоровых концов уретры.
Суть нашей методики заключается в следующем:
- доступ к спонгиозному телу в бульбозном отделе уретры осуществляется только по вентральной поверхности;
- не выполняется полная мобилизация бульбозного отдела уретры;
- проводится продольное рассечение уретры на вентральной поверхности от дистальной до проксимальной границы пораженного участка уретры;
- выполняется провизорное обшивание правого и левого краев рассеченной уретры и установка временных гемостатических зажимов типа «бульдог» на спонгиозное тело дистальнее и проксимальнее зоны стриктуры с целью профилактики кровотечения в ходе операции;
- производится иссечение рубцово измененной слизистой с полным сохранением задней полуокружности спонгиозного тела уретры;
- следующим этапом часть вентрального спонгиозного тела с наложенными на него гемостатическими швами освобождается, а при наличии спонгиофиброза данная зона спонгиозного тела иссекается;
- образовавшиеся в итоге два самостоятельных уретральных стампа (дистальный и проксимальный) ушивают на уретральном катетере, используя классическую анастомотическую технику;
- дефект спонгиозного тела ушивают поперечно или продольно в зависимости от степени его иссечения.
Данная методика нами использована в отношении 14 мужчин со стриктурой бульбозного отдела уретры при средней длине стриктуры 2,1 (1,1–3,5) см. Среди них 5 (35,7%) пациентов имели ятрогенную стриктуру, 5 (35,7%) – посттравматическую (тупая травма промежности), 4 (28,6%) – постинфекционные стриктуры. Значительная часть пациентов (10; 71,4%) ранее подвергались хирургическому лечению стриктур, включая внутреннюю оптическую уретротомию и бужирование уретры. Ни у одного пациента при среднем сроке послеоперационного наблюдения 19,3 (3–39) мес. данных за рецидив стриктуры уретры и развитие каких-либо существенных послеоперационных осложнений не получено. Безусловно, несмотря на обнадеживающие первоначальные результаты, необходимы дальнейшие исследования по изучению эффективности предложенной методики; окончательные выводы можно будет сделать только по результатам таких работ. К настоящему времени публикаций по анализу результатов применения разработанной нами техники нет, а только проведена подача заявки в Федеральную службу по интеллектуальной собственности (Роспатент) на выдачу патента на изобретение (заявление от 26.04.2019, входящий № 025134, регистрационный № 2019113026).
Таким образом, существующие методики анастомотической уретропластики без пересечения спонгиозного тела с использованием дорсального доступа и предложенная нами вентральная техника продемонстрировали высокие показатели эффективности и безопасности в лечении пациентов со стриктурой уретры. Несмотря на относительно небольшой опыт их клинического применения, они могут быть отнесены к числу основных методов лечения коротких стриктур уретры.
Анастомотическая уретропластика без пересечения спонгиозного тела в различных вариациях показала себя перспективной методикой при коротких стриктурах бульбозного и заднего отделов вне зависимости от этиологического фактора развития стриктуры. Накопленный относительно небольшой мировой опыт по применению данной методики подтверждает возможность достижения очень высокого процента устранения стриктуры уретры при минимальном негативном влиянии оперативного вмешательства на дальнейшую сексуальную функцию пациентов. Более того, по ряду ключевых аспектов анастомотическая уретропластика без пересечения спонгиозного тела превосходит аналогичную методику с пересечением спонгиозного тела. Все вышеперечисленное дает основание рекомендовать данную технику к широкому клиническому применению. В числе таких методик может быть рассмотрена и разработанная нами техника с использованием вентрального доступа.



