Введение. Стриктура уретры считется распространенной и сложной урологической патологией. Протяженные и субтотальные поражения диагностируются в 15–18% случаев стриктурной болезни уретры [1].
Основным ориентиром при выборе того или иного варианта уретропластики при стриктурах уретры служит протяженность рубцового поражения. В случае сложных и протяженных стриктур уретры применение одноэтапных аугментационных методик часто лимитировано наличием «критической» узкой уретральной площадки. Фиксация трансплантата из ротовой полости к краям слизистой пораженной уретры приводит к моделированию тубуляризации графта, что значимо увеличивает риски неудачи операции [2].
Первые результаты применения аугментационной анастомотической уретропластики описали Guralnick и Webster в 2001 г. Welk и Kodama в 2012 г. описали модификацию данной операции и назвали ее аугментационной анастомотической уретропластикой без пересечения спонгиозного тела [3].
Хотя в работе Welk и Kodama была получена высокая эффективность данной методики, в современной мировой и отечественной литературе за последние 6 лет было опубликовано немногочисленное число работ с данной техникой выполнения уретропластики, оценки ее эффективности и отдаленных результатов.
Цель исследования: показать оригинальную технику выполнения аугментационной анастомотической уретропластики без пересечения спонгиозного тела, предложенной Welk и Kodama в 2012 г., оценить отдаленные клинические результаты и эффективность данной методики.
Материалы и методы. В университетской клинике урологии РНИМУ им. Н. И. Пирогова проведен анализ результатов лечения 17 пациентов с первичными стриктурами уретры, перенесших аугментационную анастомотическую уретропластику без пересечения спонгиозного тела (операция Kodama), выполненную одним хирургом в период с 2013 по 2017 г. (см. таблицу). Ни у одного пациента не было цистостомического дренажа и никому ранее не проводилось лечения по поводу стриктуры уретры.
Перед оперативным вмешательством всем пациентам выполняли микционную цистуретрографию и ретроградную уретрографию (рис. 1).
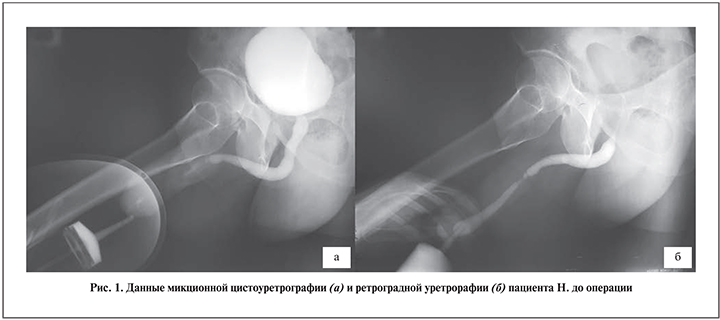
Медиана наблюдения составила 14 (6–42) мес. Контрольное обследование в объеме урофлоуметрии выполняли через 3, 6 и 12 мес. после операции, ретроградную уретрографию и уретроскопию – через 6 мес. после операции. Рецидивом стриктуры считали возникновение сужения мочеиспускательного канала, требующее инвазивного вмешательства (бужирование, внутренняя оптическая уретротомия, повторная уретропластика).
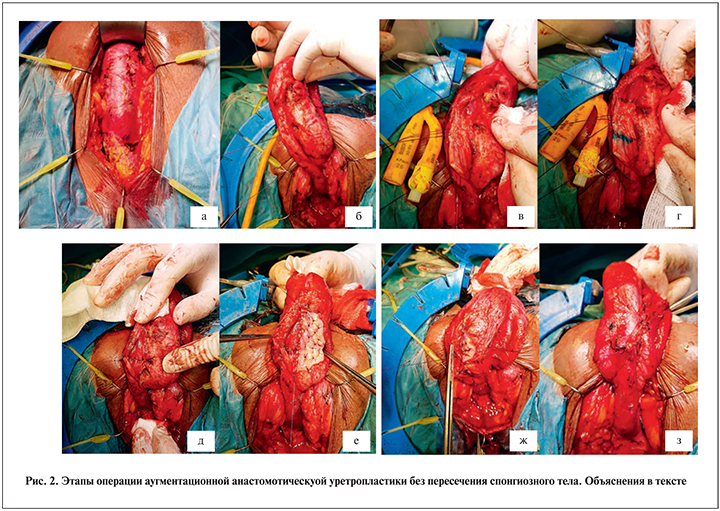
Техника операции. Пациента укладывали в литотомическую позицию. Из срединного промежностного доступа (рис. 2, а) рассекали бульбоспонгиозную мышцу до бульбозного отдела уретры. Если локализация стриктуры была в пенильном отделе уретры, то также использовался промежностный доступ при этом половой член вывихивали в рану. Мобилизацию уретры проводили по вентральной, одной (обычно слева) латеральной стороне и наполовину по дорсальной поверхности, сохранив кровоснабжение с противоположной латеральной стороны спонгиозного тела (рис. 2, б).
Мочеиспускательный канал разворачивали на 90–120°. Ретроградно в мочеиспускательный канал вводили 20 мл раствора индигокармина для прокрашивания здоровой слизистой. Ориентируясь на катетер Фолея № 20 Сh, введенный в уретру до дистального конца стриктуры, по краю мобилизации уретры по дорсальной поверхности выполняли уретротомию, зайдя на 1,5–2 см проксимальнее и дистальнее стриктуры (рис. 2, в). Наиболее узкое место уретральной площадки (рис. 2, г) иссекали с сохранением подлежащего спонгиозного тела (иссечение только пораженной слизистой) с последующим анастомозом краев слизистой внутри просвета уретры (рис. 2, д). Выполняли забор слизистой внутренней поверхности щеки по стандартной методике. Фиксировали буккальный графт к белочной оболочке кавернозных тел (рис. 2, е). Выполняли анастомоз краев рассеченной уретры с краями фиксированного буккального графта (рис. 2, ж). При достаточной ширине спонгиозного тела выполняли второй ряд швов последнего с белочной оболочкой кавернозных тел (рис. 2, з). Послойно ушивали рану.

С целью проверки герметичности швов ретроградно вводили раствор индигокармина. При определении места экстравазации жидкости накладывали дополнительный шов.
Мочевой пузырь дренировали силиконовым уретральным катетером № 14–16 Сh. Далее восстановили целостность бульбоспонгиозной мышцы и послойно ушили рану. Дренирование послеоперационной раны проводили по необходимости.
Все пациенты были активизированы вечером в день операции. Для купирования боли использовались нестероидные противовоспалительные средства. Всем пациентам проводилась стандартная антибиотикопрофилактика. Антибактериальная терапия не назначалась.
Статистическая обработка данных выполнена на индивидуальном компьютере с помощью электронных таблиц Microsoft Excel и пакета программы «Prism 6 for Windows» v 6.04 (GraphPad Software, Inc). Все полученные анамнестические, клинические, лабораторные и инструментальные данные вносили в базу данных Microsoft Excel, разработанную автором, и обработаны методом вариационной статистики. Для каждого количественного параметра были определены среднее значение (М), среднеквадратическое отклонение (δ), ошибка среднего (m), медиана (Ме), 95% доверительный интервал, для качественных данных – частоты (%).
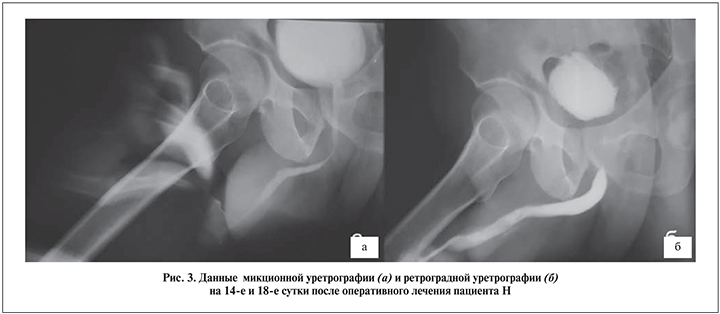
Результаты. Время пребывания пациентов после операции в стационаре составило от 2 до 4 дней. Всех пациентов выписывали из стационара с уретральным катетером. Амбулаторно в назначенный день выполнили ретроградную перикатетерную уретрографию (14–18-е сутки). В отсутствие затека контрастного вещества удаление уретрального катетера совмещали с выполнением микционной цистоуретрографии (рис. 3, а). В тот же или на следующий день пациент выполнял урофлоуметрию, на 18-е сутки – ретроградную уретрографию (рис. 3, б).
Средний срок дренирования мочевого пузыря уретральным катетером составил 14 (7–30) дней. После удаления уретрального катетера самостоятельное мочеиспускание восстановилось у всех пациентов.
У одного пациента длительное время сохранялся затек при ретроградной перикатетерной уретрографии, с целью более эффективного заживления уретральный катетер был удален, выполнена троакарная цистостомия, после которой произошло полное заживление анастомоза.
У одного пациента в раннем послеоперационном периоде возникло инфицирование послеоперационной раны, была назначена антибактериальная терапия, а также хирургическая обработка раны, в результате рана полностью зажила.
За время наблюдения рецидив стриктуры уретры диагностирован у 2 (11,8%) пациентов с посттравматической этиологией стриктуры уретры. Рецидив возник через 6 мес. после оперативного лечения. Одному пациенту выполнен 1-й этап многоэтапной пластики уретры, второму планируется выполнение внутренней оптической уретротомии.
Эффективность операции составила 88,2%.
Среднее значение показателя максимальной скорости мочеиспускания до и после операции составило 5,4 и 23,1 мл/с соответственно (p<0,05).
Недержания мочи и эректильной дисфункции de novo не отмечено ни у одного пациента.
Обсуждение. Эффективность аугментационной уретропластики зачастую зависит от правильного принятия пред- и интраоперационного решения о выборе того или иного метода операции. Наиболее сложная и дискутабельная ситуация возникает при наличии очень узкого («критического») просвета уретры в области стриктуры, т.е. выраженного поражения слизистой уретры и сужения уретральной площадки. Для такой ситуации существует несколько рекомендаций, и на сегодняшний день предложено несколько новых вариантов уретропластик [2].
Первым вариантом может быть выполнение операции иссечения измененного участка и наложение анастомоза здоровых концов уретры, т.е. пластики «конец в конец». Однако при протяженности иссекаемого участка более 2 см или локализации стриктуры в дистальной части уретры возможно натяжение в анастомозе, что может значимо увеличить риски рецидива стриктуры. Протяженность рубцового поражения уретры, при котором возможно выполнение подобного рода вмешательства, по-прежнему дискутабельна.
Другим вариантом лечения может быть применение стандартной методики аугментационного анастомоза. Данная методика при нетравматической стриктуре влечет все негативные последствия резекционного варианта уретропластики из-за нарушения антеградного кровотока по уретре. Нарушение последнего может значимо и не влиять на частоту рецидива, особенно при хорошо выраженном ретроградном кровоснабжении уретры, но может приводить к развитию сексуальных нарушений в виде снижения кровенаполнения и чувства холода головки полового члена. Это может негативно сказываться на качестве половой жизни пациентов после операции [2].
Третьим вариантом может быть операция Palminteri (сочетание методик inlay [Asopa] и ventral onlay). Несмотря на описанную автором высокую эффективность (89,6%) [4], операция имеет ряд недостатков. Во-первых, при ее выполнении наносится максимальная травма спонгиозному телу в области стриктуры в связи с его рассечением по широкой вентральной поверхности, затем – изнутри по дорсальной поверхности. Это нарушает кровоток по спонгиозному телу бульбозного отдела уретры. Во-вторых, используя два графта на одном уровне и фиксируя их к уретральной площадке с минимальной шириной, по существу моделируется трубчатый графт, который характеризуется более высоким риском рецидива стриктуры [2].
Как вариант возможно выполнение первого этапа многоэтапной уретропластики или перинеостомии. Данные методики используются при выраженном периуретральном фиброзе. При стриктурах нетравматического генеза выраженного спонгиофиброза нет, и вариант многоэтапной уретропластики оказывается излишне травматичным для мочеиспускательного канала.
В связи с развитием высоких технологий, тканевой инженерии актуальность стала набирать уретропластика с применением различных матриц, обладающих оптимальными биомеханическими свойствами. П. В. Глыбочко и соавт. [5] описали экспериментальное применение тканеинженерной уретропластики с помощью викриловой матрицы, выполненной на экспериментальных животных с высокой эффективностью до 92%. Однако пока достоверных исследований применения в клинической практике не опубликовано [5].
Welk и Kodama опубликовали результаты уретропластики под названием «аугментационная анастомотическая уретропластика» без пересечения спонгиозного тела. Подобная методика предлагается авторами как альтернатива аугментационной анастомотической уретропластике, позволяющая избегать пересечения спонгиозного тела и, следовательно, ухудшения кровотока по нему. При сравнении операции Kodama и стандартной операции Bаrbagli (dorsal onlay) эффективность их была сопоставимой – 95,3 и 91,3% соответственно [3].
В работе [6] был проведен сравнительный анализ уретропластики с пересечением спонгиозного тела и без него. В группе пациентов с аугментационной анастомотической уретропластикой без пересечения спонгиозного тела эффективность составила 87%, дриблинг наблюдался у 31% пациентов, перманентная эректильная дисфункция – только у одного пациента, постоянной формы эректильной дисфункции не было ни у одного пациента [6].
G. Barbagli et al. [7] представили свой взгляд на проблему узкой уретральной площадки и хирургический выход из этой ситуации, проанализировав 214 операций по методу ventral onlay при стриктуре бульбозного отдела нетравматического генеза. Пациенты были разделены на группу с «узкой» (n=98) и «широкой» (n=116) уретральными площадками в зависимости от возможности проведения ригидного уретероскопа диаметром 7 Fr через стриктуру уретры. Авторы указывают, что нет необходимости анастомозировать оба края буккального графта с тонкой уретральной площадкой, а сделать это нужно только с одной стороны, с другой – фиксировать край слизистой щеки к спонгиозному телу. Объясняют они положительный результат эпителизацией неприкрытой части спонгиозного тела, что было продемонстрировано в более ранних экспериментальных работах. Эффективность уретропластики при «узкой» и «широкой» уретральных площадках составила 84,7 и 86,2% соответственно.
Cчитаем, оптимальным вариантом уретропластики при протяженных стриктурах нетравматического генеза и наличии «узкой» уретральной площадки с целью сохранения антеградного кровотока является аугментационная анастомотическая уретропластика без пересечения спонгиозного тела. Принципиальное отличие данной техники в иссечении непротяженного участка уретральной площадки с минимальной шириной внутри просвета и сохранением подлежащего спонгиозного тела. Далее между краями уретральной площадки выполняется анастомоз, и операция заканчивается аугментацией уретры буккальным графтом.
Как показало наше исследование, данная методика уретропластики демонстрирует очень обнадеживающие результаты – эффективность операции составила 88,2%. Ни у одного из оперированных нами пациентов на этапах доступа и мобилизации бульбозного отдела уретры не было отмечено признаков спонгиофиброза в виде изменения цвета, уплотнения спонгиозного тела по вентральной поверхности, спаянности последнего с бульбоспонгиозной мышцей, рубцовых изменений периуретральных тканей, т.е. с потенциально сохраненным кровотоком в спонгиозном теле и минимально выраженным спонгиофиброзом. Интраоперационно это подтверждалось обильным кровотечением из спонгиозного тела в просвет уретры после иссечения измененного участка слизистой. В 4 случаях была выполнена аугментационная пластика уретры без пересечения спонгиозного тела пациентам с посттравматической этиологией стриктуры, так как интраоперационно признаков выраженного спонгиофиброза не было выявлено.
Представленный в данной работе метод уретропластики имеет ряд преимуществ:
- иссечение наиболее узкой, не пригодной для пластики части слизистой уретры, аугментация последней с использованием уретральной площадки достаточной ширины;
- сохранение самой широкой (вентральной) части спонгиозного тела, а следовательно, и антеградного кровотока по нему, что снижает риск сексуальной дисфункции у мужчин;
- отсутствие натяжения в анастомозе слизистой. Протяженность иссекаемого участка не должна превышать 2 см;
- отсутствие косметических дефектов кожи гениталий;
- более раннее выздоровление пациентов по сравнению с двухэтапными методиками уретропластики;
- возможность использования для уретропластики буккального графта меньшего размера, так как часть измененной слизистой иссекается и не требует аугментации.
Заключение. Первые результаты аугментационной анастомотической пластики уретры без пересечения спонгиозного тела демонстрируют высокую эффективность. Операция – надежный одноэтапный метод хирургического лечения пациентов со стриктурой уретры с узкой уретральной площадкой и без выраженного спонгиофиброза. Сохранение антеградного кровотока делает ее оптимальным и высокоэффективным методом уретропластики для пациентов с протяженной стриктурой уретры нетравматического генеза, сохраненной эректильной функцией, но ограниченной до 2 см протяженностью «критического» сужения зоны стриктуры.



