Введение. В настоящее время отмечается тенденция к росту заболеваемости склероатрофическим лихеном (САЛ), что неблагоприятно сказывается на качестве жизни пациентов трудоспособного и репродуктивного возраста [1, 2].
В ряде случаев развивается рубцово-облитерирующий процесс в стенках уретры, вызывающий нарушение оттока мочи с присоединением бактериальной инфекции. Это обусловлено формированием фиброзно-склеротических изменений, приводящих к уретральному стенозу и нарушению уродинамики [3].
В научных публикациях редко сообщается вопрос о вовлечении уретры в патологический процесс при САЛ, однако в своей практике мы нередко сталкивались с наличием стойких протяженных стриктур уретры, обусловленных разрастанием соединительной ткани и рубцеванием кожи, внутреннего листка крайней плоти и собственных тканей уретры.
У пациентов с САЛ клинические симптомы наблюдаются в течение длительного времени, что способствует прогрессированию заболевания с присоединением вторичных осложнений и рецидивов в виде стриктур уретры, требующих оперативной коррекции [4]. Основным критерием при выборе хирургической тактики для лечения стриктур уретры является их этиология, а основным критерием для установления диагноза при САЛ – биопсия рубцовых тканей [5].
Актуальность проблемы оперативного лечения пациентов со стриктурами уретры при САЛ обусловлена отсутствием «золотого» стандарта в выборе метода лечения, решением которого является необходимость замещения рубцово-измененного участка уретры свободным или васкуляризированным лоскутом [6]. В настоящее время наблюдается тенденция к расширению показаний к заместительной уретропластике с использованием трансплантата из слизистой оболочки щеки [7, 8]. Опираясь на предыдущие работы специалистов в генитальной хирургии, буккальная уретропластика является подходящей методикой лечения стриктурной болезни уретры, вызванной САЛ [9].
С учетом отсутствия единого подхода к тактике ведения пациентов со стриктурами уретры в зависимости от локализации, протяженности и этиопатогенетических аспектов требуется дальнейшая разработка и совершенствование способов комплексного лечения, которые уменьшали бы инвазивность и в свою очередь повышали бы качество жизни больных САЛ.
Цель исследования: оценить правильность постановки диагноза САЛ с оценкой осложнений в виде стриктур уретры и обеспечить длительный мониторинг ведения и лечения больных во избежание рецидивирования рубцовых осложнений и восходящего инфицирования при нарушении оттока мочи из нижних мочевыводящих путей.
Материалы и методы. В Республиканском Научном центре урологии Национального госпиталя при Министерстве Здравоохранения Кыргызской Республики в период с 2010 по 2020 г. проведено обследование 55 мужчин в возрасте от 17 до 85 лет с генитальной формой склероатрофического лихена (САЛ), осложненного стриктурой уретры.
Всем пациентам проведено комплексное урологическое обследование, включившее общеклинические анализы крови и мочи, бактериологическое исследование мочи, ультразвуковое исследование мочевыводящих путей, уро-флоуметрию, восходящую уретрографию, микционную цистоуретрографию, уретроцистоскопию, гистологическое исследование резецированных участков тканей.
На основании обследования определена локализация стриктур уретры на фоне САЛ: в переднем отделе уретры – у 52 (94,5%) пациентов, в заднем отделе – у 3 (5,5%). Из них протяженность стриктур уретры у 32 (58,2%) больных составила 2–4 см, у 11 (20%) – 4–6, у 9 (16,4%) – 6–10, у 3 (5,5%) – 10–15 см.
Восмнадцать (32,7%) больных ранее перенесли различные виды уретропластики и поступили с рецидивами стриктуры уретры с необходимостью повторного оперативного вмешательства. Из числа всех прооперированных 12 (66,7%) больным установлены протяженные стриктуры уретры более 4 см, 6 (33,3%) – от 10 до 15 см.
Результаты и обсуждение. Локализация стриктур уретры при САЛ превалировала в бульбозном отделе у 36 (65,5%) больных, у 16 (29,1%) – в пенильном отделе и ладьевидной ямке, у 3 (5,5%) – в простатическом отделе (рис. 1).
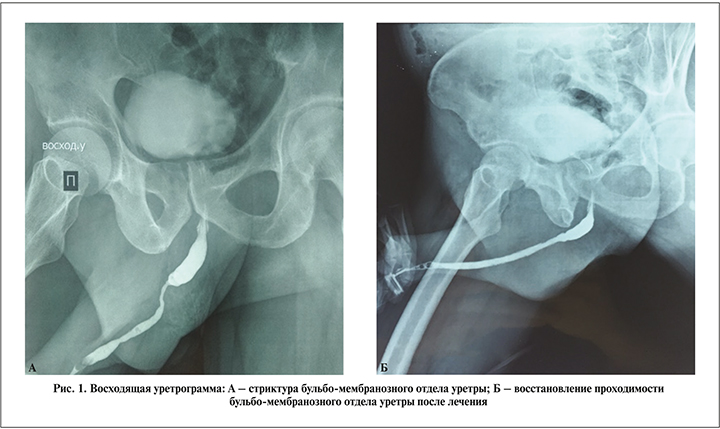
Возрастная характеристика и длительность САЛ представлены в табл. 1.

Из данных таблицы видно, что высокий удельный вес составили больные со стриктурами уретры в возрасте от 30 до 49 лет (60,0%), т.е. мужчины наиболее трудоспособного и репродуктивного возраста.
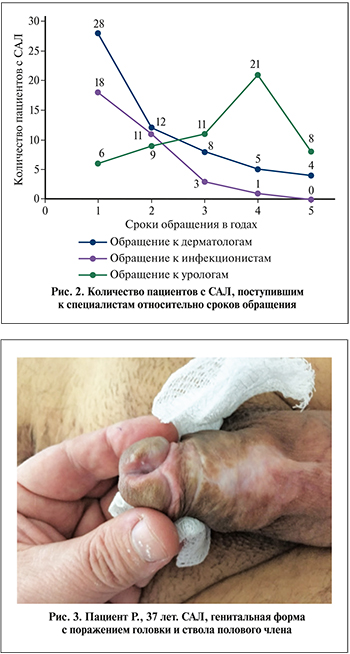 C учетом полиморфизма клинических симптомов при САЛ, отмечено превалирование первичного обращения пациентов за консультациями к врачам-дерматологам, инфекционистам и др. Таким образом, поздняя интерпретация клинического диагноза и отсутствие своевременной лечебной коррекции показывают, что к врачам урологического профиля поступают больные уже с осложненными и рецидивными формами заболевания (рис. 2).
C учетом полиморфизма клинических симптомов при САЛ, отмечено превалирование первичного обращения пациентов за консультациями к врачам-дерматологам, инфекционистам и др. Таким образом, поздняя интерпретация клинического диагноза и отсутствие своевременной лечебной коррекции показывают, что к врачам урологического профиля поступают больные уже с осложненными и рецидивными формами заболевания (рис. 2).
Таким образом отмечено, что 70,2% лиц с САЛ из числа обратившихся к врачам-дерматологам осмотрены в сроки до 1–2 года, 29,8% – от 3 до 5 лет. Из общего числа пациентов, обратившихся к инфекционистам, 87,9% лиц консультированы в сроки до 1–3 лет, 12,1% – от 3 до 5 лет.
27,2% пациентов с САЛ, обратившихся за урологической помощью, пролечены в сроки от 1 до 2 лет, 72,7% – в сроки от 3 до 5 лет. Соответственно, в этот временной промежуток у всех пациентов уже была обнаружена стриктурная болезнь уретры различной степени выраженности.
Нами проведен ретроспективный анализ этиологических причин возникновения стриктур уретры, вызванных САЛ, и установлены следующие причинно-следственные факторы: инфекционно-воспалительный генез – у 26 (47,3%), травматический – у 9 (16,4%), аутоиммунный и гормональный – у 4 (7,3%), идиопатический – у 16 (29,1%).
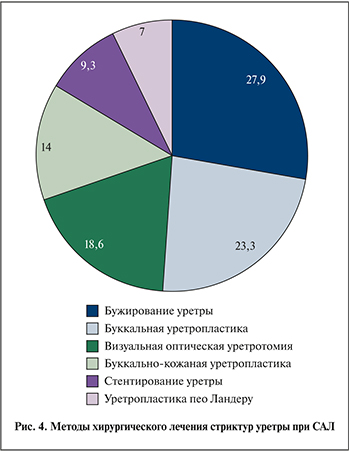
При определении клинических симптомов у пациентов со стриктурами уретры на фоне САЛ (генитальная форма) превалировали жалобы на затрудненное мочеиспускание с чувством неполного опорожнения мочевого пузыря, разбрызгивание струи мочи, прерывистое мочеиспускание, снижение эластичности и подвижности кожи в области головки полового члена и внутреннего листка крайней плоти, появление белесоватых пятен в аногенитальной области с участками рубцевания кожных покровов (рис. 3), зуд, диспаурению, эректильную дисфункцию, депрессию.
Метод лечения пациентов с САЛ подбирался на основе комплексного обследования с учетом клинической картины, локализации и протяженности стриктуры уретры, степени выраженности инфравезикальной обструкции.
Консервативная терапия проведена 12 (21,8%) пациентам с непротяженными стриктурами переднего и заднего отделов уретры (до 2 см) с использованием препаратов:
1. Бовгиалуронидаза азоксимер 3000 МЕ 1 раз в 5 дней внутримышечно, на курс – 5 инъекций, и так до 5 курсов терапии, между 2 курсами терапии пауза в течение 1 мес.
2. Препараты группы топических глюкокортикостероидов (0,05% клобетазола пропионат в форме крема) в виде аппликаций 2 раза в день ежедневно в течении 4 нед., далее через день еще 4 нед., и далее в последующие 4 нед. через каждые 3–4 дня.
3. Антибиотикотерапия после результатов бактериологического посева мочи.
Перед началом лечения всем пациентам исключали инфекции, передаваемые половым путем, а также проводили санацию уретры антисептическими растворами.
Оперативное лечение проведено 43 (78,2%) больным с протяженными стриктурами уретры от 2 до 15 см.
Оперативное лечение также применяли всем пациентам с рецидивированием стриктур уретры, перенесшим ранее уретропластику в различных методиках.
 Следует отметить, что все методы оперативного лечения сочетались с применением консервативной терапии.
Следует отметить, что все методы оперативного лечения сочетались с применением консервативной терапии.
Перед выбором метода оперативного вмешательства диагностика САЛ подтверждалась данными гистологического исследования кожи полового члена. При наличии участков здоровой ткани, подтвержденных морфо-гистологическим исследованием, применяли заместительную кожную уретропластику, в отсутствие здоровой ткани – уретропластику с использованием буккального лоскута, сочетанную буккально-кожную уретропластику.
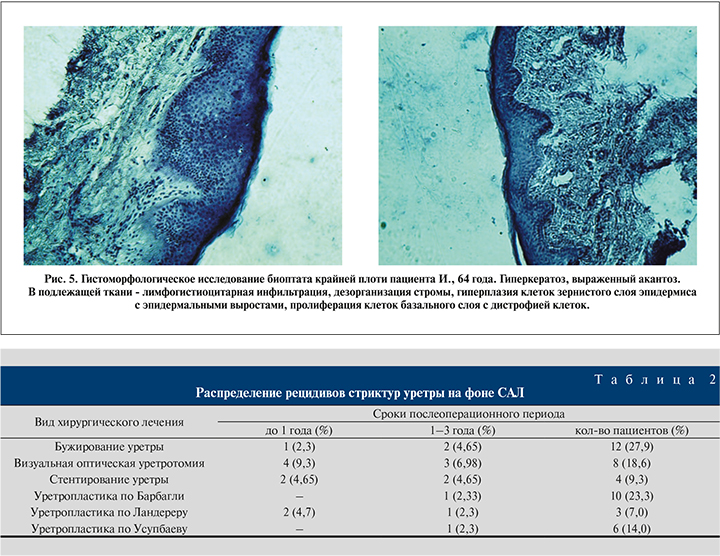
Оперативное лечение включало: бужирование уретры – у 12 (27,9%), визуальную оптическую уретротомию – у 8 (18,6%), стентирование уретры – у 4 (9,3%), уретропластику по Усупбаеву – у 10 (23,3%) больных, буккально-кожную уретропластику – у 6 (14,0%), уретропластику по Ландереру - у 3 (7,0%) (рис. 4).
К сожалению, следует отметить, что 18 пациентам с протяженными стриктурами уретры при САЛ ранее были произведены реконструктивно-восстановительные операции с неудовлетворительным результатом, причем 5 (11,6%) больным дважды, 6 (14,0%) – трижды, 7 (16,3%) – более 3 раз. Мы считаем, что данный момент может быть связан с неправильной трактовкой заключения основного заболевания и, соответственно, выбором тактики ээтиопатогенетического лечения с отсутствием тактических подходов к ведению пациентов с САЛ в послеоперационные сроки, в итоге приведших к рецидивированию и возникновению стойких рубцовых стриктур уретры.
При анализе сроков, прошедших после первого хирургического вмешательства на уретре, выяснено, что менее 1 года оперированы 4 (9,3%) больных, от 1 года до 3 лет – 11 (25,6%), более 3 лет – 3 (7,0%).
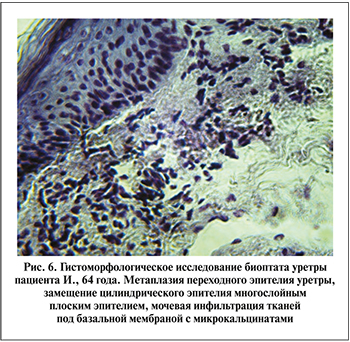
Основным методом верификации диагноза САЛ стала биопсия пораженных тканей кожи головки полового члена, внутреннего листка крайней плоти, а также тканей уретры из резецированных участков стриктур, взятых интраоперационно.
Гистоморфологическая картина пациентов с САЛ характеризовалась очаговой атрофией эпидермиса, замещением цилиндрического эпителия многослойным плоским с явлениями гиперкератоза и акантоза, гистио-лимфоцитарной инфильтрацией клеток, а также образованием микрокальцинатов под базальной мембраной (рис. 5–7).
В послеоперационном периоде 1–3 лет оценены методы оперативного лечения с анализом осложнений в виде рецидивирования стриктур уретры и изучены параметры восстановления пассажа мочи из нижних мочевыводящих путей. Следует отметить, что наряду с оперативной коррекцией все пациенты получали консервативную терапию САЛ препаратами бовгиалуронидаза азоксимер 3000 МЕ в виде внутримышечных инъекций и препараты группы топических глюкокортикостероидов (0,05%-ный клобетазола пропионат в форме крема) в виде аппликаций по ранее указанной схеме (табл. 2).
 Основываясь на комплексном подходе к диагностике и лечению стриктур уретры, всем пациентам с САЛ на дооперационном этапе, а также в ближайшем послеоперационном периоде через 1–3 мес. и в отдаленные сроки – через 6 мес., 1 и 2 года проводилось уродинамическое обследование в рамках урофлоуметрии (УФМ).
Основываясь на комплексном подходе к диагностике и лечению стриктур уретры, всем пациентам с САЛ на дооперационном этапе, а также в ближайшем послеоперационном периоде через 1–3 мес. и в отдаленные сроки – через 6 мес., 1 и 2 года проводилось уродинамическое обследование в рамках урофлоуметрии (УФМ).
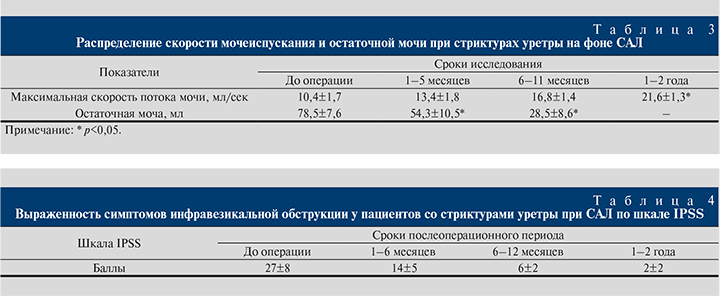
Максимальная скорость потока мочи по данным УФМ до консервативного лечения составила 10,4±1,7 мл/с, после лечения – 22,3±1,4 мл/с. После уретропластики отмечено увеличение максимальной скорости потока мочи спустя 1–3 мес., и уже через 6 мес. выявлено достоверное восстановление адекватного акта мочеиспускания в пределах 21,6±1,3 мл/с.
Определение остаточной мочи по данным ТРУЗИ позволило наблюдать через 3 мес. после операции уменьшение остаточной мочи в мочевом пузыре на 33% и через 6 мес. добиться полного ее исчезновения (табл. 3).
Оценивая выраженность симптомов инфравезикальной обструкции у пациентов со стриктурами уретры при САЛ по шкале IPSS отмечено выраженное нарушение уродинамики в 72,2% наблюдений (табл. 4).

Таким образом, своевременное и комплексное лечение стриктур уретры доказало свою эффективность ввиду восстановления адекватного пассажа мочи из нижних мочевыводящих путей, уменьшения числа рецидивирования стриктурной болезни уретры и улучшения качества жизни пациентов, страдавших САЛ.
Заключение. Правильность верификации диагноза и выбора метода лечения стриктур уретры, вызванных САЛ, значительно влияет на благоприятный исход лечения пациента. Проведя сравнительный анализ примененного нами комплексного подхода к лечению пациентов со стриктурами уретры при САЛ, мы пришли к выводу: его эффективность достаточно высока.
Методы консервативного лечения стриктур уретры на фоне САЛ служат большим подспорьем к хирургическому лечению и должны быть применимы в комплексной тактике ведения пациентов. Методы оперативного лечения стриктур уретры при САЛ достаточно сложны и трудоемки, в связи с чем необходим постоянный и длительный мониторинг послеоперационного ведения пациентов с САЛ для профилактики и лечения прогрессирования склеротических изменений с формированием повторных, более стойких рубцовых изменений в стенках мочеиспускательного канала.



