Введение. Стриктура уретры является относительно распространенным и одним из самых древних заболеваний, известных в урологии. Исторически уретриты и травма уретры определены как основные причины стриктур уретры у мужчин. В наше время частое выполнение трансуретральных операций и катетеризаций мочевого пузыря привело к тому, что ятрогенное повреждение уретры стало ведущим этиологическим фактором развития стриктуры мочеиспускательного канала у мужчин в развитых странах и вторым после травматического повреждения – в развивающихся [1, 2]. Под термином «ятрогенная стриктура уретры» объединяются стриктуры мочеиспускательного канала у мужчин, имеющие одинаковую этиологию заболевания (развитие стриктуры вследствие медицинского вмешательства), но различный патогенез. Это определяет необходимость изучения ятрогенных стриктур уретры для выбора оптимального метода лечения.
Целью исследования было определить виды ятрогенных стриктур уретры и оценить результаты их лечения.
Материалы и методы. С 2011 по 2016 г. в университетской клинике урологии РНИМУ им. Н. И. Пирогова проведено лечение 321 пациента со стриктурой уретры. Ятрогенные стриктуры уретры диагностированы в 140 (43,6%) наблюдениях. Из этого количества были исключены все пациенты, нарушившие протокол послеоперационного наблюдения, и пациенты с постлучевыми стриктурами ввиду малого их числа. Таким образом, ретроспективно были проанализированы результаты лечения 133 пациентов с ятрогенной стриктурой уретры. Медиана возраста пациентов составила 69 (25–86) лет.
У всех пациентов собирали анамнез (в том числе с целью выявления возможной этиологии стриктуры), выполняли физикальный осмотр, урофлоуметрию, оценку объема остаточной мочи, ретроградную и микционную уретрографию, на основании результатов которых определялся рецидив стриктуры и необходимость повторного оперативного вмешательства.
В зависимости от предшествовавших вмешательств, ставших причиной образования стриктуры уретры, пациенты были разделены на четыре группы. В 1-ю группу вошли 72 (54%) пациента после транс(интра)уретральных вмешательств (трансуретральная резекция предстательной железы [ТУР ПЖ] или мочевого пузыря [ТУР МП], бужирование уретры, травматичная катетеризация и т.д.), во 2-ю – 45 (34%) пациентов с посткатетерными стриктурами (ишемические/поствоспалительные), в 3-ю – 7 (5%) пациентов, перенесших неудачное лечение гипоспадии, и в 4-ю – 9 (7%) человек после открытой аденомэктомии.
В зависимости от клинической ситуации пациентам выполнены следующие оперативные вмешательства: одноэтапная пластика уретры с использованием буккального графта (29 пациентов), одноэтапная уретропластика с использованием кожного лоскута (6), многоэтапная буккальная уретропластика (9), анастомотическая пластика уретры «конец в конец» с или без пересечения спонгиозного тела (33), внутренняя оптическая уретротомия (ВОУТ; 46), одноэтапная пластика ладьевидной ямки с использованием слизистой оболочки щеки (2), меатотомия (6) и промежностная простатэктомия (2).

Контрольная урофлоуметрия выполнена через 1, 3, 6 и 12 мес. после операции; ретроградная уретрография или уретроскопия – через 6 мес. после операции. Рецидивом стриктуры считалось возобновление симптомов обструктивного мочеиспускания, значение максимальной скорости мочеиспускания менее 12 мл/с в сочетании со следующими факторами: наличие уретрографических или уретроскопических данных за сужение просвета и необходимость в инвазивном вмешательстве (аутокатетеризация, бужирование уретры, ВОУТ, уретропластика).
Статистическая обработка данных выполнена на индивидуальном компьютере с помощью электронных таблиц Microsoft Excel и пакета программы «Prism 6 for Windows» v 6.04 (GraphPad Software, Inc). Все полученные анамнестические, клинические, лабораторные и инструментальные данные вносили в базу данных Microsoft Excel, разработанную автором, и обработаны методом вариационной статистики. Для каждого количественного параметра были определены среднее значение (М), среднеквадратическое отклонение (δ), ошибка среднего (m), медиана (Ме), 95% доверительный интервал, для качественных данных – частоты (%).

Результаты. В группе I (пациенты после транс(интра)уретральных вмешательств) средняя протяженность стриктуры составила 2 см. У большинства пациентов локализация стриктуры выявлена в бульбозном отделе уретры (рис.1 а, б). Меньшая часть группы была представлена поражением пенильного отдела, пануретральной стриктурой, меатостенозом.
В группе пациентов со стриктурами, возникшими после длительных катетеризаций (II группа), средняя протяженность стриктуры была немного длиннее (2,4 см) по сравнению c I группой. Основной локализацией стриктуры также оказался бульбозный отдел (рис. 2 б). С равной частотой выявлены пануретральная стриктура (рис. 2 а), меатостеноз и стриктура пенильного отдела уретры.
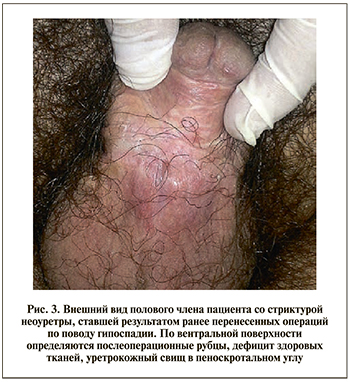 В III группу включили пациентов после перенесенной коррекции гипоспадии (рис. 3). В данной группе средняя протяженность сужения составила 6 см.
В III группу включили пациентов после перенесенной коррекции гипоспадии (рис. 3). В данной группе средняя протяженность сужения составила 6 см.
Повреждения мочеиспускательного канала у пациентов после аденомэктомии (группа IV) были выявлены в мембранозном и простатическом отделах уретры (рис. 4). Характеристика ятрогенных стриктур уретры приведена в табл. 1.
Результаты хирургического лечения ятрогеных стриктур уретры в целом были признаны удовлетворительными: эффективность эндоскопического лечения, ВОУТ, составила 52%, эффективность уретропластики в зависимости от метода колебалась от 83 до 100%.
Для оценки эффективности реконструктивных операций все варианты примененных уретропластик в зависимости от их принципа (резекция или увеличение просвета при помощи свободного трансплантата или васкуляризированного лоскута, замещение уретры) были объедены в группы (табл. 2).
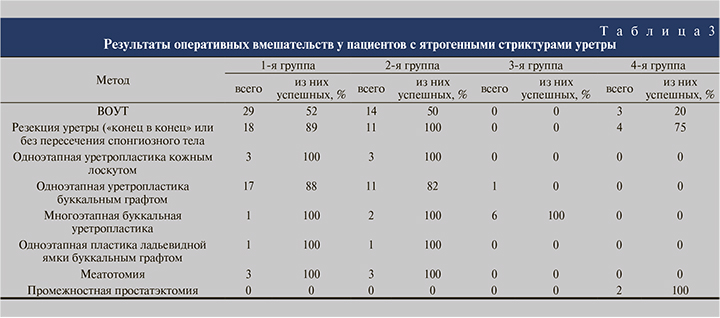
Следующим этапом был проведен анализ эффективности оперативного лечения по группам для выявления зависимости успеха от этиологического фактора, вызвавшего стриктуру (табл. 3). Внутренняя оптическая уретеротомия была применена в отношении пациентов 1-й, 2 и 4-й групп со стриктурами бульбозного отдела протяженностью менее 1 см. Для пациентов со стриктурами после транс(интра)уретральных вмешательств и посткатетерными стриктурами результаты ВОУТ были сопоставимыми – 52 и 50% соответственно. В 4-й группе пациентов после аденомэктомии успешными оказались только 20% вмешательств.
Анастомотические варианты уретропластик продемонстрировали 89%-ную эффективность у пациентов 1-й группы, 100% – 2-й и 75% – 4-й. Выполненная у части пациентов 1-й и 2-й групп анастомотическая пластика уретры без пересечения спонгиозного тела (рис. 5) имела сопоставимые результаты с традиционной пластикой «конец в конец».
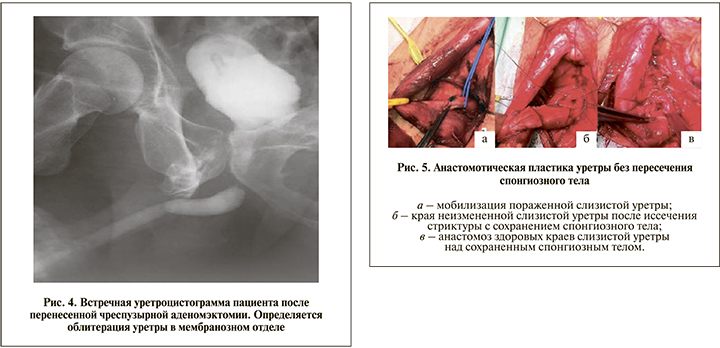
Анастомотическая пластика уретры без пересечения спонгиозного тела выполнена по описанной нами ранее методике [3].
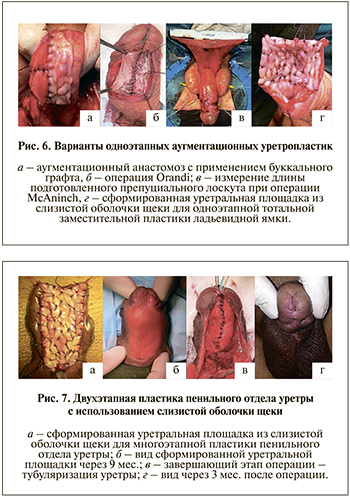
Пластика уретры кожным лоскутом (методики Orandi и McAninch) была выполнена 6 пациентам 1-й и 2-й групп и продемонстрировала 100%-ную эффективность (рис. 6, б, в). Одноэтапная пластика уретры буккальным трансплантатом (рис. 6, а) оказалась эффективной для 88% пациентов после транс(интра)уретральных вмешательств, в 82% случаев – при посткатетерных стриктурах и была признана неэффективной для 1 пациента после ранее перенесенной коррекции гипоспадии.
В отличие от одноэтапной многоэтапная заместительная уретропластика, применявшаяся в отношении пациентов 1–3-й групп, продемонстрировала 100%-ную эффективность (рис. 7). Пластика ладьевидной ямки (рис. 6, г) и меатотомия, которые использовали в первых двух группах, также оказались успешными во всех случаях.
У ряда пациентов 4-й группы стриктура локализовалась в мембранозном отделе уретры, в связи с чем анастомотическая пластика заключалась в формировании бульбопростатического анастомоза.

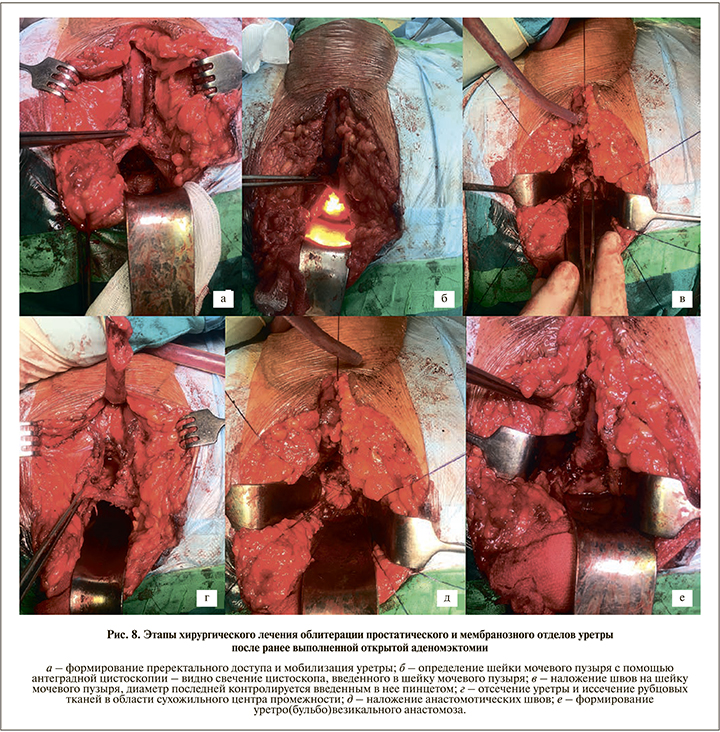
Больные с облитерацией простатического и мембранозного отделов уретры после ранее выполненной аденомэктомии считаются одной из наиболее сложных групп пациентов, которым мы вынуждены предлагать этапное лечение. Первым этапом выполняли простатэктомию промежностным доступом по Янгу (преректальный доступ, используемый при радикальной промежностной простатэктомии). Удаляли предстательную железу с иссечением окружающих рубцовых тканей (включая наружный сфинктер), сформировали уретро(бульбо)везикальный анастомоз (рис. 8).
 Данное вмешательство в 100% случаев приводит к тотальной инконтиненции, в связи с чем вторым этапом лечения становится имплантация искусственного мочевого сфинктера. В нашем исследовании выполненная 2 пациентам 4-й группы промежностная простатэктомия оказалась успешной в обоих случаях.
Данное вмешательство в 100% случаев приводит к тотальной инконтиненции, в связи с чем вторым этапом лечения становится имплантация искусственного мочевого сфинктера. В нашем исследовании выполненная 2 пациентам 4-й группы промежностная простатэктомия оказалась успешной в обоих случаях.
Обсуждение. Лечение стриктур уретры ведет свою историю еще со времен Древнего Египта. Запечатленный на стенах египетских пирамид процесс бужирования уретры, несомненно, подтверждает этот факт. Многие авторы конца XIX – первой половины XX вв. указывают на высокую распространенность стриктур уретры, развитие которой традиционно связывается с травмой или воспалительным процессом (чаще гонореей). Достижения медицины, рост уровня жизни и сокращение военных конфликтов способствовали снижению показателя распространенности стриктуры уретры в промышленно развитых странах к концу прошлого века с 1,4 до 0,9% [4]. Однако развитие медицинских технологий и повышение доступности медицинской помощи в свою очередь стали причиной роста частоты формирования ятрогенных стриктур уретры. Сегодня ятрогения является ведущим этиологическим фактором в развитии стриктур уретры у мужчин старше 45 лет в развитых странах. По данным зарубежных авторов, ятрогенная этиология стриктуры уретры наиболее распространена, составив до 45% среди всех причин стриктуры мочеиспускательного канала [5, 6].
Так, E. Palminteri et al. [6] оценили этиологию и особенности стриктур уретры у мужчин, проанализировав 1439 пациентов, проходивших лечение с 2000 по 2010 г. Частота ятрогенных стриктур составила 38,6%, из них посткатетерные имели место в 16,3% (средняя протяженность стриктуры – 4,4 см), постгипоспадийные – в 12,2% (средняя протяженность стриктуры – 4,43 см), после трансуретральных вмешательств – в 9,1% [6].
N. Lumen et al. [2] подвергли проспективному анализу данные 268 пациентов, страдавших стриктурой уретры и прооперированных с 2001 по 2007 г. Ятрогенная этиология заболевания была определена у 45,5% пациентов.
Согласно данным S. Tritschler et al. [10], которые проанализировали оригинальные статьи и мета-анализы, посвященные этиологии, диагностике и лечению стриктур уретры, опубликованные в базе данных PubMed за период с 1995 по 2012 г., 45% стриктур уретры имели ятрогенную этиологию, преимущественно были следствием трансуретральных вмешательств и длительной катетеризации.
S. Zhou et al. [5], изучив этиологию стриктур уретры у 172 пациентов, показали, что трансуретральные вмешательства явились причиной заболевания в 46,51% случаев. При этом средняя длина стриктуры составила 3,3 см.
В работах многих авторов было отмечено существенное различие в этиологии стриктур уретры среди пациентов, живущих в странах с различным экономическим уровнем развития. Исследователи [1] ретроспективно оценили влияние географических (региональных) факторов на этиологию и локализацию стриктур уретры у мужчин, проанализировав 2589 пациентов, перенесших уретропластику в период с 2000 по 2011 г. Оказалось, что среди жителей Италии (1646 человек) и США (228 человек) ятрогенные стриктуры встречались в 35% случаев (из них 49% – после неудачной коррекции гипоспадии), травматические – в 16%. В группе пациентов, проживающих в Индии (n=715), травматические стриктуры вышли на первое место и составили 36%, ятрогенные – лишь 16% (из них 16% – постгипоспадийные).
Анализ работы 2 госпиталей за 6 мес. показал, что частота травматичной катетеризации мочевого пузыря составила 6,7 на 1000 случаев. При этом у 81% пациентов это было сопряжено с развитием осложнений II степени и выше по шкале Clavien–Dindo [11].
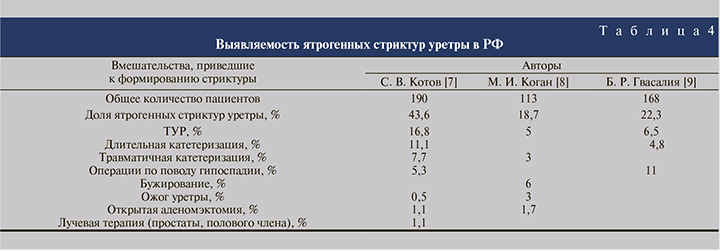
В Российской Федерации на долю ятрогенных приходится 21–44% всех стриктур уретры у мужчин (табл. 5) [7–9].
Полученные нами данные, равно как и работы других российских авторов, сопоставимы с результатами зарубежных коллег и подтверждают превалирующую роль ятрогенных повреждений в генезе стриктур уретры.
Также наше исследование показало, что основной причиной ятрогенных стриктур служат перенесенные трансуретральные вмешательства (54%) и длительные катетеризации мочевого пузыря (34%). В 85% случаев указанные стриктуры располагались в бульбозном отделе уретры. Следует отдельно отметить и тот факт, что у 4,5% пациентов ятрогенное повреждение уретры ограничивалось меатостенозом и такая простая манипуляция, как меатотомия, обеспечила всем этим пациентам удовлетворительное качество мочеиспускания, при этом меатостеноз на догоспитальном этапе диагностирован не был, что, вероятно, могло быть следствием пренебрежения осмотром наружных половых органов.
Быстрое развитие медицинских технологий, стремление к малоинвазивному лечению и расширение спектра выполняемых операций ведут к экспоненциальному росту числа госпитализаций и операций у пациентов, относящихся к группе риска развития ятрогенных стриктур: имеющих тяжелый коморбидный фон, особенно сердечно-сосудистые заболевания. Поскольку любое трансуретральное вмешательство сопряжено с риском развития стриктуры уретры, с ростом количества пролеченных больных увеличится и абсолютное количество пациентов с ятрогенными повреждениями уретры, которые уже сегодня занимают лидирующее положение в этиологии этого заболевания.
Внутренняя оптическая уретротомия по-прежнему остается наиболее часто выполняемой операцией при стриктурах уретры в мире. В нашей работе эффективность данной операции не превысила 52% ни в одной группе пациентов. Следует упомянуть, что ВОУТ в нашем исследовании выполнялась исключительно при первичных непротяженных (<1 см) стриктурах в бульбозном отделе уретры. Ранее проведенное нами исследование показало, что эффективность данного вида операции в лечении стриктур уретры была ниже и составила 46% [12]. Это указывает на более обоснованное применение ВОУТ в отношении пациентов с ятрогенными стриктурами (особенно после трансуретральных вмешательств) по сравнению с пациентами со стриктурами мочеиспускательного канала другого этиогического фактора. По данным М. Ф. Трапезниковой и соавт. [13], частота рецидива стриктуры уретры после ВОУТ была равной 16,8%. Однако авторы отмечали, что пациенты после эндоскопического вмешательства подвергались в течение года регулярному бужированию уретры. Подобные результаты позволяют предложить ВОУТ только тщательно отобранной группе пациентов с первичным непротяженным поражением уретры (<1 см) в бульбозном отделе и без выраженного спонгиофиброза, информированных об ожидаемой эффективности вмешательства (~50%) и готовых к, возможно, более объемным хирургическим вмешательствам в случае рецидива стриктуры после ВОУТ.
Исходя из полученных данных, считаем целесообразным учитывать этиологический фактор при выборе метода хирургической коррекции стриктуры уретры.
Простота выполнения и малая инвазивность не должны становиться причиной повсеместного применения ВОУТ как первого метода в лечении стриктуры уретры. Выполненная не по показаниям ВОУТ может служить фактором риска неудачи последующей уретропластики.
При стриктурах бульбозного отдела уретры, развившихся как после трансуретральных вмешательств, так и на фоне воспалительного процесса, лучшие результаты демонстрирует пластика уретры. При этом результаты анастомотической и аугментационной методик сопоставимы. Анализируя группу пациентов с поствоспалительными стриктурами уретры, следует отметить их большую протяженность относительно 1-й группы пациентов и снижение ожидаемой эффективности анастомотической пластики; таким пациентам следует чаще рекомендовать проведение аугментационной пластики уретры, к выполнению которой хирург должен быть готов.
Несмотря на ятрогенный характер стриктуры, зачастую предполагающий протяженное сужение, наличие сопутствующей патологии, спонгиофиброза и нозокомиальной флоры, при правильном выборе оперативного пособия можно достичь хороших результатов (82–100%), сопоставимых с таковыми у пациентов со стриктурами уретры без предшествовавших вмешательств.
Отдельного внимания заслуживают повреждения заднего отдела уретры. В генезе подобных повреждений мочеиспускательного канала ведущую роль играет не только открытая аденомэктомия, но и различные фокальные методы лечения рака предстательной железы и доброкачественной гиперплазии, активно набирающие популярность. Выраженный рубцово-спаечный процесс, сложность хирургического доступа, частое сочетание со стриктурами бульбозного отдела и необходимость восстановления функции удержания мочи в последующем делают эту хирургию исключительно прерогативой хирургов и центров с достаточным опытом уретральной и промежностной хирургии.
Заключение. Доля ятрогенных стриктур уретры в крупных мегаполисах растет и может достигать 45%. Наиболее часто встречаются стриктуры после длительного нахождения уретрального катетера и после трансуретральных вмешательств. Высокая частота ятрогенных стриктур уретры диктует необходимость информировать пациента о возможном нарушении мочеиспускания после транс(интра)уретральных вмешательств, а также целесообразность оценки мочеиспускания в послеоперационном периоде. Для каждой подгруппы ятрогенных стриктур характерна своя локализация, протяженность и степень спонгиофиброза. При правильном выборе метода лечения эффективность уретропластики составляет 83–100%. Эффективность ВОУТ составляет 52%, и об этом необходимо предупреждать пациентов, предлагая данную операцию. Хирургическое лечение стриктур уретры целесообразнее проводить в медицинских учреждениях с достаточным опытом хирургии уретры.



