Введение. Цистит является самым распространенным заболеванием мочевого пузыря, и в течение жизни его переносит до 25% взрослого населения. По статистике, в России регистрируют 26–36 млн случаев заболевания острым циститом в год [1–3]. Это одно из немногих заболеваний, которое характеризуется высокой частотой перехода в хроническую форму – до 50%. При наличии от трех и более обострений в год специалисты говорят о рецидивирующем характере течения цистита. Хронический посткоитальный цистит рассматривается как одна из разновидностей хронического цистита.
Ведущими факторами-провокаторами, вызывающими посткоитальный цистит, являются:
1. Анатомические особенности строения уретры и расположения наружного отверстия уретры у женщин,
2. Использование спермицидов,
3. Смена полового партнера,
4. Сексуальная активность – половой акт может приводить к восходящему инфицированию мочевого пузыря,
5. Несоблюдение правил общей и интимной гигиены,
6. Дефицит витамина D (характерно для регионов с коротким световым днем, практически вся РФ) троекратно повышает риск развития инфекции мочевыводящих путей (ИМВП).
Профилактика рецидивирующей ИМВП направлена на изменение образа жизни и питьевого режима, устранение урологических факторов риска и коррекцию сопутствующих заболеваний. Согласно клиническим рекомендациям Российского общества урологов (РОУ) и гайдлайнам Европейской ассоциации урологов (ЕАУ), антибактериальную профилактику посткоитального цистита рекомендовано назначать в случае неэффективности поведенческой терапии и мер неантимикробной профилактики [4, 5]. Особый интерес вызывают препараты, cодержащие проантоцианидины, D-маннозу, пробиотики, витамин D3. Функции витамина D в профилактике хронического цистита многообразны – это влияние на физиологические процессы в организме, включающие пролиферацию, дифференцировку, апоптоз, клеточный рост, нервно-мышечную проводимость, иммунитет, экспрессию генов и воспаление как защитную реакцию организма [6]. Впервые на связь между рецидивирующим циститом у женщин в пременопаузе и дефицитом витамина D указали W. Nseir et al. [7]. Исследование, проведенное в Нидерландах vander Starreetal [8], показало, что у большинства взрослых пациентов с ИМВП имелся дефицит витамина D и его уровень у респондентов был ниже, чем в контрольной группе.
Исследования in vitro показали, что эпителий мочевого пузыря у женщин, проходивших лечение с использованием витамина D3, обладает способностью вырабатывать большее количество кателицидина и β-дефензинов, которые являются антимикробными пептидами и оказывают защитное иммунопротективное действие, предотвращая развитие ИМВП [9, 10].
Таким образом, в клинических исследованиях подтверждена обоснованность назначения витамина D3 в лечении и профилактике воспалительных заболеваний нижних мочевыводящих путей. Более эффективная профилактика ИМВП возможна при использовании сочетания нескольких компонентов, каждый из которых показал в клинических исследованиях свою эффективность. В частности, являясь природным антибактериальным агентом, D-манноза препятствует бактериальной адгезии к уротелию основных возбудителей инфекционно-воспалительного процесса, таких как E. coli, Klebsiella spp., P. аeruginosa и др. Исследования in vitro продемонстрировали, что D-манноза связывается с фимбриями типа I энтеробактерий, препятствуя их адгезии к клеткам уротелия, а снижение уровней бактериурии подтверждено результатами исследований in vivo на моделях животных [11, 13–15].
По данным рандомизированного клинического исследования, регулярный прием порошка D-маннозы в дозировке 2000 мг привел к сокращению частоты рецидивов ИМВП в 4 раза по сравнению со стандартной профилактикой нитрофурантоином [16]. Таким образом, полученные результаты позволяют рекомендовать D-маннозу как средство профилактики хронического посткоитального цистита [17]. Хотелось бы отметить, что D-манноза в дозировке 2000 мг вызывает интерес Европейского урологического сообщества и, как отмечено выше, была упомянута в последних руководствах и рекомендациях как перспективное вещество при лечении и профилактике ИМВП.
Способность клюквы (Vaccinium macrocarpon, дикая североамериканская клюква) ингибировать адгезию E. сoli к уротелию связана с присутствием танинов (проантоцианидинов и антоцианидинов), которые обладают выраженными антиоксидантными свойствами, ингибируют синтез фимбрий E. сoli и снижают выброс медиаторов воспаления, оказывая противовоспалительное действие, тем самым улучшая трофику слизистой оболочки уретры и мочевого пузыря [18–20].
Для профилактики ИМВП целесообразнее использовать комбинации веществ, обладающих иммунопротективным действием, улучшающих трофику уротелия и оказывающих противомикробное действие. Применение комбинации активных компонентов D-маннозы, проантоцианидина и витамина D3 подтвердило свою эффективность и отличный профиль безопасности в рамках международных клинических исследований и показало снижение частоты рецидивов цистита в 4 раза [21]. Так, например, биологически активная добавка Уронекст (ООО «НПО ПетроваксФарм», Россия) содержит D-маннозу 2000 мг, проантоцианидины 36 мг (или 500 мг брендированного концентрата экстракта клюквы Cran-Max), витамин D3 1 мкг. Имея в составе необходимую стандартизированную дозировку проантоцианидинов (36 мг), Уронекст отличается повышенной биодоступностью экстракта клюквы за счет запатентованной формулы высвобождения: лигнин-целлюлозные волокна защищают активные молекулы клюквы от деградации в тонком кишечнике, действуя как естественная система доставки.
Приняв во внимание сходный генез и хроническое течение бактериальных и посткоитальных циститов, нами предложено применение Уронекста в виде однократных приемов после половых контактов в качестве профилактики рецидивов заболевания.
Цель исследования: оценить эффективность биологической добавки Уронекст в профилактике посткоитального цистита у женщин.
Материалы и методы. В исследование были включены 86 пациенток, ведущих активную половую жизнь. С помощью типологического отбора они были разделены на две группы, сопоставимые по возрасту, клиническим проявлениям и давности заболевания, по 43 человека в каждой группе. Средний возраст пациенток первой группы составил 29±11,24 года, второй – 27±12,5 лет. Давность заболевания у пациенток обеих групп составила более 5 лет. Пациентки первой группы получали Уронекст – 1 саше однократно после каждого полового акта. Пациентки второй группы профилактического лечения не получали.
Критерии включения:
- Женщины в репродуктивном возрасте от 18 до 45 лет.
- Документированный анамнез ИМВП (3 эпизода за предыдущие 12 мес. или 2 эпизода за предыдущие 6 мес.
- Возникновение обострений цистита после полового акта.
- Гетеросексуальные женщины, живущие регулярной половой жизнью.
- Отсутствие патогенной микрофлоры в моче при бактериологическом исследовании.
- Информированное согласие на участие в исследовании.
Критерии невключения:
- Применение антибактериальной терапии по поводу ИМВП в течение последнего месяца.
- Пролапс органов тазового дна ≥III стадии.
- Отягощенный аллергологический анамнез.
- Нейрогенная дисфункция нижних мочевыводящих путей.
- Интерстициальный цистит.
- Камни в мочевыводящих путях.
- Анамнез или признаки опухолевых заболеваний мочевыводящих путей.
- Пациентки с врожденными аномалиями развития мочеполовых органов (экстрофия мочевого пузыря, гипоспадия, эписпадия).
- Почечная недостаточность.
- Сахарный диабет.
- Текущее использование кортикостероидов и иммуносупрессивные заболевания.
- Гиперчувствительность к любому из компонентов, входящих в состав препарата исследуемых препаратов.
- Пациентки после перенесенных оперативных вмешательств на органах мочеполовой системы.
- Беременность, лактация, планирование беременности в период проведения исследования.
Критерии исключения:
- Отзыв пациенткой информированного согласия.
- Прекращается исследования досрочно по решению спонсора.
- Продолжение участия пациентки в данном исследовании не соответствует интересам ее здоровья, по мнению исследователя.
- Ошибочное включение пациентки в исследование.
- Любое медицинское событие, которое, по мнению исследователя, требует исключения пациентки из исследования.
- Применение запрещенной терапии.
До включения в исследование всем пациенткам проведена диагностика заболевания на основании совокупности анамнестических и объективных клинических данных, лабораторно-инструментальных методов, а также уродинамического исследования.
При первом обращении на каждую пациентку заводилась специальная карта, в которой отмечались особенности анамнеза жизни и заболевания, данные дополнительных методов обследования. При сборе жалоб уделяли внимание интенсивности и выраженности болевого синдрома, частоте мочеиспусканий, наличию чувства неполного опорожнения мочевого пузыря. Анамнез заболевания включал длительность заболевания, предшествовавшие возникновению заболевания факторы, виды проводимого ранее лечения, а также их эффективность и длительность безрецидивного периода. Тщательно анализировался гинекологический статус. Отмечали наличие очагов хронической инфекции как возможного источника инфицирования мочевого пузыря.
Всем женщинам двукратно до курса приема и после проводилось исследование показателей клинического анализа крови по общепринятой методике; общего анализа мочи; бактериологического исследования мочи с определением чувствительности к антибиотикам. Биохимический анализ крови включал определение мочевины и креатинина.
Важным звеном в обследовании пациенток оказалось уродинамическое исследование. Диагностика проводилась на аппарате Delphis IP, посредством которого выполнялась урофлоуметрия и цистометрия для оценки функционального состояния детрузора и выявления расстройств мочеиспускания. Для исключения ошибочных результатов уродинамический мониторинг выполнялся перед цистоскопией. Неотъемлемой частью обследования стала цистоскопия для определения состояния слизистой мочевого пузыря. Эндоскопическое исследование выполняли всем пациенткам эндоскопом фирмы Storz. При осмотре слизистой мочевого пузыря обращали внимание на наличие зон гиперемии, кровоизлияний, эрозивных и язвенных дефектов, состояние слизистой в зоне треугольника Льето и шейки мочевого пузыря, на выраженность сосудистого рисунка.
Многим пациенткам обеих групп ранее проводилось медикаментозное лечение по поводу посткоитального цистита. Наиболее часто при этом применялись антибактериальные препараты нитрофуранового ряда (13 пациенток 1-й группы и 15 – 2-й), фторхинолоны (12 пациенток 1-й группй, 11 – 2-й) и фитопрепараты (9 пациенток 1-й группы, 7 – 2-й). Данные о предшествовавшей медикаментозной терапии посткоитального цистита у пациенток, включенных в исследование, представлены в табл. 1.

По протоколу исследование проводилось в ходе трех визитов.
Во время визита «1» исследователь получал письменное согласие на участие пациентки в исследовании, производилась выдача опросника симптомов острого цистита (ACSS); опросника качества жизни SF-36; шкалы по оценке боли в области малого таза и частоты мочеиспусканий (PUF). После этого оценивались соответствие пациента критериям включения/невключения, выдача препарата, инструктаж. Полученные данные заносились в ИРК (страницы визита 1). Визит «2» проводился на 90±7-й день от начала исследования. В ходе визита исследователь проводил регистрацию нежелательных явлений, возникавших во время проведения исследования, регистрацию симптоматики заболевания; проводилось физикальное обследование с измерением артериального давления (АД), частоты сердечных сокращений (ЧСС), частоты дыхания (ЧД) и температуры (аксиллярной); оценка дневника мочеиспусканий, опросника симптомов острого цистита (ACSS), опросника качества жизни SF-36, шкалы по оценке боли в области малого таза и частоты мочеиспускания (PUF).
В ходе визита «3» (на 180±7-й день) исследователь проводил регистрацию нежелательных явлений, возникших во время проведения исследования, регистрацию симптоматики заболевания; проводились физикальное обследование с измерением АД, ЧСС, ЧД и температуры (аксиллярной), оценка дневника мочеиспусканий, опросника симптомов острого цистита (ACSS), опросника качества жизни SF-36; шкалы по оценке боли в области малого таза и частоты мочеиспускания (PUF).
Отдельно в ИРК заносились данные о дополнительном визите при рецидиве, в ходе которого исследователь проводил регистрацию нежелательных явлений, возникших во время проведения исследования, регистрацию симптоматики заболевания; проводились физикальное обследование с измерением АД, ЧСС, ЧД и температуры (аксиллярной), оценка дневника мочеиспусканий, опросника симптомов острого цистита (ACSS), опросника качества жизни SF-36; шкалы по оценке боли в области малого таза и частоты мочеиспускания (PUF).
Основным показателем, отражающим эффективность профилактики посткоитальных циститов, является частота рецидивов инфекции НМВП. Первичной конечной точкой было количество обострений ИМВП в течение 6 мес. курса приема терапии. Первичная точка – отсутствие рисков обострений.
Вторичные критерии эффективности:
- Изменение показателя по шкале PUF относительно исходного значения.
- Изменение показателя по шкале ACSS относительно исходного значения.
- Изменение показателя по шкале SF-36 относительно исходного значения.
Сравнительный анализ количественных переменных, характеризующих клинико-лабораторное и функциональное состояние мочевыделительной системы, проводился методом описательной статистики с использованием непараметрического критерия Уилкоксона Манна– Уитни. Обработка и графическое представление данных проводились с помощью компьютерных программ Statisticа, 6.0 и Excel, 2003. В работе использованы различные методы статистической обработки в зависимости от типа случайных величин и поставленной задачи исследования [21].
Исследование одобрено локальным этическим комитетом (ЛЭК) ЧУЗ «Клиническая больница “РЖД-Медицина” города Барнаул».
Результаты. Клиническая картина у больных посткоитальным циститом проявлялась симптомами, указанными в табл. 2.

Все пациентки в течение последних 6 мес. до включения в исследование отмечали дизурию, многие из них указывали на боли над лоном, наличие примеси крови в моче, мутную мочу и некоторые из них отмечали примесь крови в моче (табл. 2).
При оценке уровня лейкоцитурии у всех больных обеих групп до лечения отмечалось отсутствие патогенной флоры в моче при проведении бактериологического исследования. При оценке основных показателей периферической крови у всех пациенток обеих групп клинически значимых изменений не выявлено.
Основным первичным критерием эффективности стало количество обострений (рис. 1).
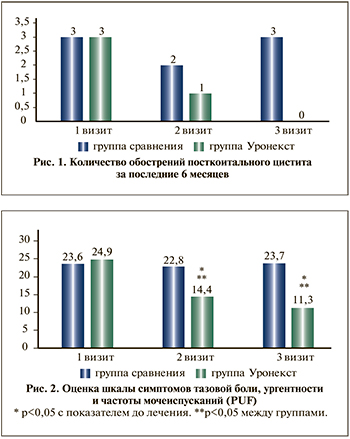
На фоне приема Уронекста в ходе наблюдения количество обострений прогрессивно снижалось и к концу исследования равнялось нулю, в то время как в группе сравнения за весь период наблюдения у 43 пациенток отмечено в общей сложности 129 обострений. Это было нами расценено как отличный результат проводимого профилактики. Один только этот факт позволяет рекомендовать Уронекст в качестве профилактики посткоитального цистита. В группе сравнения количество обострений в ходе наблюдения не менялось. В качестве вторичных критериев оценки эффективности применялся ряд шкал. Анкетирование по шкалам PUF, SF 36 и ACSS проводили трижды всем участникам исследования с интервалом в 3 мес. Одна из них – общепризнанная шкала PUF [22] (рис. 2–4).

До начала исследования у пациенток обеих групп отмечалось повышение общего балла (рис. 2) по шкале PUF за счет увеличения балла по оценке симптомов и увеличения балла по оценке беспокойства (рис. 3, 4). В ходе наблюдения у пациенток 1-й группы на фоне приема БАД Уронекст имело место значимое снижение общего балла (более чем в 2 раза) через 6 мес. наблюдения (рис. 2), балла по оценке симптомов цистита (в 2 раза, с 14,7 ± 2,9 до 7,2±1,1 к 3-му визиту, р<0,05) (рис. 3) и оценке беспокойства (рис. 4) (более чем в 2 раза относительно исходного значения и относительно показателей 2-й группы, не получивших лечение (с 10,2±1,6 по 4,1±0,6; р<0,05). Сумма баллов анкеты PUF высоко достоверно коррелировала с наличием/отсутствием симптомов: учащение мочеиспусканий днем (p=0,009), учащение мочеиспусканий ночью (p<0,001), императивные позывы на мочеиспускание (p=0,002), жалобы на болезненное мочеиспускание (p<0,001) и боль в области мочевого пузыря (p<0,001), что подтверждает достоверность полученных результатов. У пациенток 2-й группы данные показатели сохранялись примерно на исходном уровне в ходе всего наблюдения.
Данные изменения коррелировали с основными показателями анкеты качества жизни SF-36 (табл. 3).
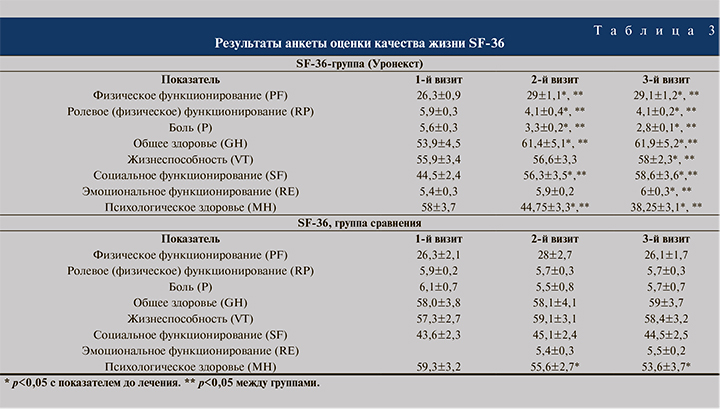
У пациенток первой группы на фоне приема Уронекста отмечено повышение качества жизни по всем основным параметрам, представленным в табл. 3. Физическое функционирование с 26,3±0,9 ко 2-му визиту повысилось до 29±1,1 (на 9,4%), и данный балл сохранялся на достигнутом уровне к 3-му визиту. Аналогичным образом менялись параметры общего здоровья (на 13%), жизнеспособности (на 3,7%), социального (на 24%), эмоционального (на 10%) функционирования и психического здоровья (34%), что нами было также расценено как отличный результат. Параметр боли значительно уменьшился с 5,6±0,3 до 2,8±0,1 балла через 6 мес., данный параметр был ниже этого показателя 2-й группы более чем в 2 раза (50%)! У пациенток 2-й группы в ходе наблюдения качество жизни не менялось (табл. 3).
Одним из вторичных критериев эффективности стало изменение показателя по шкале ACSS относительно исход ного значения. При оценке результатов данной шкалы выявлены схожие с предыдущими шкалами изменения, указывающие на достоверную эффективность профилактики рецидивов посткоитального цистита с помощью биологически активной добавки Уронекст.
При оценке типичных симптомов (Typical) до лечения у пациенток обеих групп отмечен сопоставимо высокий балл (11,5±1,3 и 10,3±1,4 соответственно у первой и второй групп), что указывало на значимые клинические проявления цистита. В ходе наблюдения у пациенток 1-й группы отмечено прогрессивное снижение уровня данного показателя (до 1,3±0,4 ко 2-му визиту и 0,6±0,1 к 3-му [на 94%! от исходного показателя]), что указывало на купирование типичных для цистита симптомов. У пациентоr 2-й группы данный показатель достоверно не менялся (рис. 5).
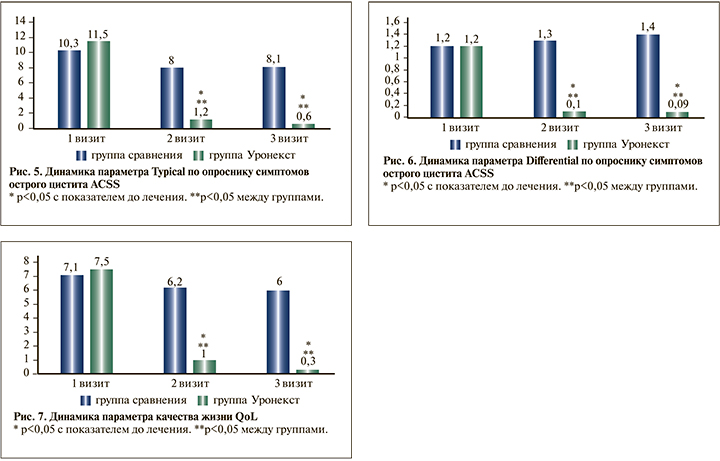
Подобные изменения имели место и при оценке дифференциальных симптомов (Differential) (рис. 6).
Раздел «Динамика» (Dynamics) шкалы ACSS подтверждает положительный эффект от приема Уронекста, что выражалось уменьшением данного показателя в 1-й группе (с 1,04±0,4 на 1-м визите до 0,4±0,3 на 2-м [на 61,6%!]), в то время как во 2-й группе данный показатель достоверно не менялся (на 20-м визите 2,7±0,3, на 3-м – 2,9±0,4). Положительный эффект от приема Уронекста выражался и в повышении качества жизни пациенток 1-й группы, на что указывало снижение уровня QoL с 7,5±0,4 до 0,3±0,7 (на 96%!!) к 6-му месяцу наблюдения, качество жизни пациенток 2-й группы в ходе наблюдения не наблюдалось (рис. 7).
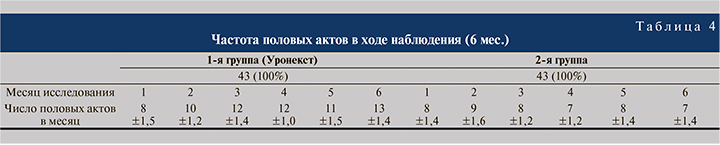
Одно из интересных наблюдений выявлено в ходе исследования: при оценке частоты половых актов на фоне приема Уронекста выявлено увеличение их количества, что было расценено как отсутствие страха перед половым актом на фоне уменьшения количества рецидивов. Во второй группе в ходе наблюдения число половых актов не менялось (табл. 4).
Оценка переносимости:
За время исследования аллергических реакций ни у одной из пациенток не отмечено.
Негативные изменения в общем состоянии пациенток, возникновение новых жалоб, патологические отклонения лабораторных показателей (клинического и биохимического исследования крови и клинического исследования мочи) в ходе исследования фиксировались как нежелательные явления. У пациенток обеих групп в ходе лечения клинически значимых нежелательных явлений зафиксировано не было.
Обсуждение. Посткоитальный цистит у женщин – это заболевание, возникающее с момента начала половой жизни, имеющее рецидивирующее течение, значимо снижающее качество жизни пациенток.
Компоненты в составе Уронекста способны снижать риск рецидивов посткоитального цистита.
Полученные результаты указывают на высокую эффективность применения БАДа Уронекст в профилактике возникновения посткоитальных циститов. По данным нашего исследования, Уронекст способен снижать частоту рецидивов посткоитального цистита в 3 раза, причем ни у одной из пациенток на фоне приема Уронекста за 6 мес. наблюдения рецидива заболевания отмечено не было. Действие Уронекста подтверждается полученными лабораторными и клиническими результатами. Отмечена прямая корреляционная связь между купированием лейкоцитурии и клиническими проявлениями заболевания (r=0,7, p<0,001). Помимо снижения частоты рецидивов отмечена еще одна важная особенность профилактического приема БАДа Уронекст: в тех случаях, когда у женщин, принимавших БАД, все-таки развивался посткоитальный цистит, выраженность его симптомов была достоверно меньше, чем в контрольной группе, и ниже исходных данных до начала лечения. Указанные эффекты профилактического приема БАДа Уронекст достоверно улучшали качество жизни женщин. Это дало нам основание прийти к выводу, согласно которому профилактика с помощью БАДа Уронекст позволяет избегать применения антибактериальных препаратов, которые неизбежно несут негативные последствия для организма. Прием одного саше Уронекста в течение 6 ч после полового акта обладает достоверным защитным эффектом в отношении рецидивов посткоитального цистита.
Заключение. На основании полученных данных мы пришли к следующему заключению: применение Уронекста по схеме одного саше однократно после полового акта в течение 6 мес. дает возможность эффективно воздействовать на основные звенья патогенеза посткоитального цистита, сокращать частоту обострений заболевания, тем самым значительно повышать качество жизни пациенток. Уронекст хорошо переносится пациентками и не вызывает нежелательных явлений.



