Введение. Рак почки (представленный преимущественно почечноклеточным раком) входит в десятку наиболее часто диагностируемых видов рака у мужчин и женщин [1]. Благодаря повсеместному распространению методов компьтерной и магнитно-резонансной томографии возросла доля злокачественных новообразований почки, выявляемых на ранней стадии [2]. Имеющиеся данные свидетельствуют о том, что опухоль почки небольших размеров может иметь низкий злокачественный потенциал и низкий темп прогрессирования [3]. Но в то же время не существует надежных инструментов, позволяющих уверенно предсказать риск развития метастатического рака у конкретного пациента. Несмотря на наличие различных опций системной терапии метастатического рака почки, результаты лечения остаются не самыми благоприятными [4]. Поэтому на ранних стадиях у пациентов без серьезных сопутствующих хронических заболеваний предпочтение отдается агрессивной, а не выжидательной тактике [5].
Все существующие на сегодняшний момент опции лечения рака почки стадии T1 – это радикальная нефрэктомия, резекция почки, активное наблюдение. В отношении техники хирургического органосохраняющего вмешательства можно выделить три основных направления: открытая операция, малоинвазивная хирургия и аблационные методики.
На сегодняшний день робот-ассистированные операции заняли определенную нишу в сфере малоинвазивных вмешательств. По официальным данным компании Intuitive Surgical (Intuitive Surgical, Inc., США), начиная с 1998 г. опубликовано около 15 тыс. работ (в том числе рандомизированные исследования и систематические обзоры), посвященных технологии DaVinci. Лидирующей областью хирургии по количеству публикаций стабильно остается урология.
Традиционные методы визуализации перед операцией включают компьютерную либо магнитно-резонансную томографию. Однако необходимо учитывать, что КТ и МРТ не позволяют отличать злокачественную опухоль почки от онкоцитомы или ангиомиолипомы с невыраженным жировым компонентом. В определенных случаях при затруднении в диагностике новообразования почки может быть рекомендовано выполнение ультразвукового исследования с контрастным усилением [6].
Абсолютными противопоказаниями к проведению робот-ассистированной или же лапароскопической операции являются повышенное внутричерепное давление, коагулопатия. К относительным противопоказаниям относятся желудочко-перитонеальный шунт, застойная сердечная недостаточность, хроническая обструктивная болезнь легких высокой степени тяжести [7].
В нашей практике перед роботическим хирургом на этапе предоперационного консультирования и подготовки в большинстве случаев поставлен ряд следующих задач:
 1. Оценка сложности резекции почки по нефрометрической шкале RENAL или PADUA.
1. Оценка сложности резекции почки по нефрометрической шкале RENAL или PADUA.
2. Анализ компьютерной томографии с целью оценки архитектоники почечных сосудов и сосудов, питающих опухоль.
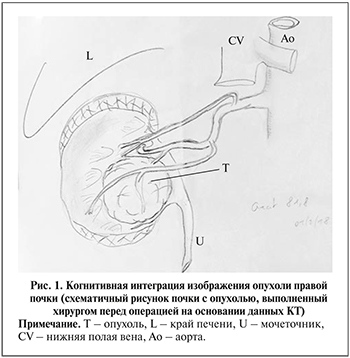
3. 3D-моделирование изображения компьютерной томографии. В отсутствие специального программного обеспечения для анатомической визуализации мы используем технику простого рисунка, позволяющую осуществлять когнитивную «интеграцию» изображения оперируемой почки (рис.1).
4. Обсуждение алгоритма операции внутри роботической хирургической команды накануне вмешательства.
Для успешного выполнения высокотехнологичной операции и повышения уровня хирургической безопасности необходимо совершенствовать качество предоперационной подготовки хирурга к операции. Одним из таких методов, позволяющим прогнозировать уровень сложности предстоящей операции, является нефрометрия. Система нефрометрии RENAL была первоначально описана в 2009 г. Kutikov и Uzzo [8]. Система классификации PADUA представлена Ficarra и соавт. также в 2009 г. [9].
Применение нефрометрии несет две основные задачи: методологическую и прогностическую. В клинической практике нефрометрия помогает прогнозировать удачный исход органосохраняющей операции, оценить риски послеоперационных осложнений [10, 11], а в некоторых случаях – определить целесообразность того или иного метода ишемии. Так, например, при сумме баллов по шкале RENAL менее 6, опухоли почки с экзофитным ростом, расположенной по передней поверхности нижнего полюса у пациента с единственной или единственной функционирующей почкой, снижением функции контрлатеральной почки выбор может быть сделан в пользу off-clamp метода (отсутствие наложения сосудистого зажима на почечную артерию) [12].
Еще одним эффективным средством обеспечения хирургической безопасности является система чек-листов, заполняемых перед проведением оперативного вмешательства непосредственно в условиях операционной. В 2013 г. Song и соавт. опубликовали чек-лист проверки безопасности, применяемый при длительных роботических операциях через 3 или 4 ч после начала операции. Указанный чек лист может быть рекомендован клиникам, находящимся в начале пути освоения роботической хирургии [13].
Тем не менее, несмотря на все преимущества робот-ассистированной резекции почки [14], мы убеждены, что лапароскопическая резекция почки остается и впредь останется актуальным и востребованным методом органосохраняющего лечения при опухолях почки.
Цель исследования: провести сравнительный анализ клинических особенностей двух методов органосохраняющего лечения опухоли почки: робот-ассистированной и лапароскопической резекций почки.
Материалы и методы. Мы выполнили ретроспективный сравнительный анализ двух групп пациентов с опухолями почек, которым с 2012 по 2019 г. была сделана робот-ассистированная (РАЛРП) либо лапароскопическая резекция почки (ЛРП).
Пациенты были обследованы в необходимом объеме, предоперационное обследование включило стандартный набор лабораторных и инструментальных исследований.
Оперативные вмешательства, описанные в нашем исследовании, были выполнены хирургами, обладающими серьезным опытом выполнения лапароскопических и робот-ассистированных урологических операций.
В ходе исследования мы проанализировали ряд следующих параметров в обеих группах: возраст, уровень сывороточного креатинина до и после операции, количество баллов по шкале нефрометрии RENAL, продолжительность операции и тепловой ишемии, объем кровопотери, размер опухоли, характер роста опухоли, продолжительность госпитализации, тип опухоли по данным гистологического исследования (злокачественный или доброкачественный), применение метода раннего снятия зажима с почечной артерии (тепловая ишемия до 15 мин), наличие осложнений по классификации Clavien–Dindo. Послеоперационная оценка уровня сывороточного креатинина осуществлялась через 6 мес. после операции.
Статистическая обработка цифрового материала была выполнена с использованием компьютерной программы Statistica 10. Мы провели сравнительный статистический анализ параметров двух групп пациентов, которым была выполнена робот-ассистированная (63 пациента) и лапароскопическая резекция почки (36 пациентов) с использованием критериев Стьюдента для параметров возраста и времени операции, критериев Манна–Уитни и Уилкоксона – для остальных параметров.
Результаты. В группе робот-ассистированной лапароскопической резекции почки (РАЛРП) средний возраст пациентов составил 56,63±11,94 года (p 0,155). Медиана балла по шкале нефрометрии RENAL – 6 баллов (5; 7,5, p<0,001). Медиана уровня креатинина сыворотки крови до операции – 89,65 мкмоль/л (82,275; 100, p 0,009). Время операции в среднем составило 184,4±55,8 мин (p 0,371). Медиана продолжительности тепловой ишемии – 15 мин (10; 20, p 0,022). Медиана объема интраоперационной кровопотери – 150 мл (100; 325, p<0,001). Размер удаленной опухоли в среднем равнялся 34,4±18,9 мм. В 22 (34,92%) случаях опухоль имела экзофитный рост, в 4 (6,35%) полностью эндофитный, преобладали новообразования, имевшие смешанный тип роста (37 случаев – 58,73%). Средняя продолжительность госпитализации – 3,3±1,5 к/д. Раннее снятие зажима выполнено 34 (53,9%) пациентам, 7 (11,1%) пациентам выполнена резекция почки без тепловой ишемии.
В целом послеоперационные осложнения по классификации Clavien–Dindo отмечены в 53,1% случаев. Классификация Clavien–Dindo включает пять групп осложнений разной степени тяжести – от легкой (I) до летального исхода (V). К осложнению IIIb-степени мы отнесли случай пациентки с подозрением на послеоперационное кровотечение. В раннем послеоперационном периоде нами была выполнена лапаротомия и ревизия брюшной полости и забрюшинного пространства, интраоперационно данных за продолжающееся кровотечение получено не было, в дальнейшем послеоперационный период протекал гладко.
 В большинстве случаев были отмечены осложнения I (легкой) степени (67,6%), доля осложнений II и III степеней – 29,4 и 2,9% соответственно. Осложнений IV и V степеней зарегистрировано не было. Медиана уровня креатинина после операции составила 94,3 мкмоль/л (85,4; 103,6, p 0,012). Результаты гистологического исследования резецированных опухолей в группе роботических резекций распределились следующим образом: у 51 (79,7%) пациента был выявлен почечноклеточный рак, в 5 (7,8%) случаях ангиомиолипома, в 4 (6,2%) – онкоцитома, у 3 (4,7%) пациентов верифицирована простая киста почки и в 2 (3,1%) случаях – метанефрогенная аденома. Среди резецированных злокачественнх опухолей 35 (68,6%) составили образования стадии pT1а, 12 (23,5%) – pT1b, 1 (1,9%) – pT2a, 2 (3,9%) – pT3a. Что касается стадии pT3a, в одном случае опухолевый тромб в почечной вене был выявлен интраоперационно, во втором случае органосохраняющая операция на стадии T3a была выполнена пациентке с единственной почкой, контрлатеральная почка была удалена пятью годами ранее по поводу почечноклеточного рака (ПКР). У 11 (21,5%) пациентов с почечноклеточным раком был диагностирован папиллярный вариант ПКР, у 32 (62,7%) – светлоклеточный, у 5 (9,8%) – хромофобный, у 2 (3,9%) – мультилокулярный кистозный вариант светлоклеточного рака и в 1 (1,9%) случае – почечно-клеточный рак, ассоциированный с MITF-TFE-транслокацией. Положительный хирургический край не был выявлен ни в одном случае. На момент публикации у оперируемых пациентов не выявлены как местный рецидив, так и рецидив в контралатеральной почке, а также не получено данных о наличии отдаленных метастазов.
В большинстве случаев были отмечены осложнения I (легкой) степени (67,6%), доля осложнений II и III степеней – 29,4 и 2,9% соответственно. Осложнений IV и V степеней зарегистрировано не было. Медиана уровня креатинина после операции составила 94,3 мкмоль/л (85,4; 103,6, p 0,012). Результаты гистологического исследования резецированных опухолей в группе роботических резекций распределились следующим образом: у 51 (79,7%) пациента был выявлен почечноклеточный рак, в 5 (7,8%) случаях ангиомиолипома, в 4 (6,2%) – онкоцитома, у 3 (4,7%) пациентов верифицирована простая киста почки и в 2 (3,1%) случаях – метанефрогенная аденома. Среди резецированных злокачественнх опухолей 35 (68,6%) составили образования стадии pT1а, 12 (23,5%) – pT1b, 1 (1,9%) – pT2a, 2 (3,9%) – pT3a. Что касается стадии pT3a, в одном случае опухолевый тромб в почечной вене был выявлен интраоперационно, во втором случае органосохраняющая операция на стадии T3a была выполнена пациентке с единственной почкой, контрлатеральная почка была удалена пятью годами ранее по поводу почечноклеточного рака (ПКР). У 11 (21,5%) пациентов с почечноклеточным раком был диагностирован папиллярный вариант ПКР, у 32 (62,7%) – светлоклеточный, у 5 (9,8%) – хромофобный, у 2 (3,9%) – мультилокулярный кистозный вариант светлоклеточного рака и в 1 (1,9%) случае – почечно-клеточный рак, ассоциированный с MITF-TFE-транслокацией. Положительный хирургический край не был выявлен ни в одном случае. На момент публикации у оперируемых пациентов не выявлены как местный рецидив, так и рецидив в контралатеральной почке, а также не получено данных о наличии отдаленных метастазов.
Статистически значимых различий по возрастным характеристикам в двух группах не выявлено (56,6±11,94 года в группе РАЛРП vs 60,17±11,99 года в группе ЛРП). Продолжительность оперативного вмешательства в группе РАЛРП превысила длительность лапароскопической операции (184,4±55,8 vs 125,56±25,57 мин, p<0,001) (рис. 2).
Медиана значения балла нефрометрии RENAL совпала в обеих группах и составила 6 баллов, p 0,77 (рис. 3).
Не отмечено также статистических различий в группах в отношении средних значений продолжительности тепловой ишемии (медиана 15 vs 17 мин в группах РАРП и ЛРП соответственно, p 0,102).
Больший объем кровопотери был отмечен в группе РАЛРП (медиана 150 vs 100 мл в группе ЛРП, p 0,014). Максимальный объем кровопотери в роботической группе составил 1500, в лапароскопической – 500 мл.
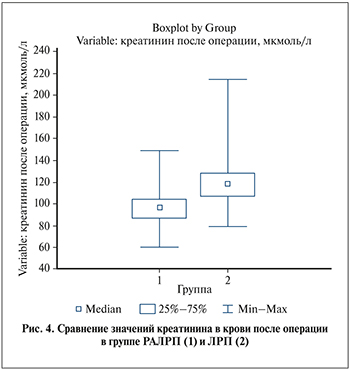 Медиана диаметра удаленной опухоли в группе РАЛРП и ЛРП совпали (30 мм [20; 44,5] vs 30 мм [24,3; 35,5[ соответственно, p 0,545). Медиана уровня креатинина в сыворотке крови после хирургического лечения – параметр, который оказался статистически достоверно выше в групе ЛРП (94,3 мкмоль/л в 1-й группе vs 117,5 мкмоль/л во 2-й группе, p 0,004). Исходный уровень сывороточного креатинина в группах до операции был незначительно ниже в основной (роботической) группе, но статистически значимых различий отмечено не было (89,65 vs 94, p 0,581) (рис. 4).
Медиана диаметра удаленной опухоли в группе РАЛРП и ЛРП совпали (30 мм [20; 44,5] vs 30 мм [24,3; 35,5[ соответственно, p 0,545). Медиана уровня креатинина в сыворотке крови после хирургического лечения – параметр, который оказался статистически достоверно выше в групе ЛРП (94,3 мкмоль/л в 1-й группе vs 117,5 мкмоль/л во 2-й группе, p 0,004). Исходный уровень сывороточного креатинина в группах до операции был незначительно ниже в основной (роботической) группе, но статистически значимых различий отмечено не было (89,65 vs 94, p 0,581) (рис. 4).
Медиана продолжительности госпитализации также статистически значимо отличалась в группе пациентов РАЛРП – 3 к/д (vs 9 к/д в группе ЛРП, p<0,001). Раннее снятие зажима с почечной артерии (до 15 мин) в лапароскопической группе применялось значительно реже, чем в роботической (25,0% vs 53,9% соответственно, p<0,05). Тепловая ишемия не применялась («off-clamp» метод) в 11,1% случаев в группе РАРП и в 27,7% в группе ЛРП (p<0,05).
В группе лапароскопической резекции почки осложнения по классификации Clavien–Dindo затронули 52,8% случаев (доля осложнений I–III степеней – 47,36%, 47,36 и 5,28% соответственно). Статистически значимых различий в отношении осложнений в группах не выявлено (p 1,00).
В группе ЛРП по сравнению с роботическими резекциями преобладали опухоли с экзофитным ростом (83,4 vs 34,9%, p<0,001). Для группы РАЛРП были более характерны опухоли с эндофитным и смешанным ростом (65,08 vs 16,6%, p<0,001).
По данным патогистологического исследования доли злокачественных и доброкачественных новообразований, что составили 91,7 и 8,3% соответственно, в группе лапароскопической резекции почки оказались схожими с аналогичными показателями в группе робот-ассистированной резекции, статистически значимых различий не выявлено (p 0,259).
Обсуждение. Сравниваемые нами группы роботической и лапароскопической резекций почки оказались эквивалентыми в отношении возраста пациентов, среднего балла по шкале нефрометрии RENAL, уровня креатинина до операции, размеру опухоли, продолжительности тепловой ишемии. Различия коснулись таких показателей, как продолжительность операции, объем кровопотери, уровень креатинина после операции, продолжительность госпитализации, применение техники раннего снятия зажима с почечной артерии, применение метода резекции без наложения сосудистого зажима («off-clamp»), доля опухолей с экзофитным характером роста.
Средняя продолжительность операции 184,4 мин в группе РАЛРП превысила время операции в группе ЛРП (125,6 мин). С одной стороны, мы связываем этот факт с тем, что серия роботических операций включила операции, выполнявшиеся хоть и опытным роботическом хирургом, но на этапе инсталляции хирургической системы DaVinci и формирования новой роботической команды. С другой стороны, указанная продолжительность операции не противоречит данным наиболее крупных серий робот-ассистированных резекций почки [15–18].
Объем кровопотери также оказался выше в группе роботических операций (150 vs 100 мл, p 0,014), однако полученные нами значения оказались близкими к результатам вышеупомянутых серий робот-ассистированной резекции почки. В нашей серии РАЛРП объем интраоперационной кровопотери в пределах 1000–1500 мл был отмечен у 6 пациентов. Среди них у одного пациента опухоль по данным предоперационной оценки имела 10 баллов по шкале RENAL, у четырех – 8 и у одного – 7 баллов.
У 3 из 6 пациентов диагностирован рак почки стадии T1b, у одного – T2b, в одном случае – T1a, и у одного пациента по данным гистологического исследования была выявлена метанефрогенная аденома. В то же время, по результатам исследования Benway и соавт. [19] в группе робот-ассистированных резекций почки был отмечен меньший объем кровопотери по сравнению с группой лапароскопических операций (155 vs 196 мл; p<0,03). В той же работе было продемонстрировано, что продолжительность госпитализации после роботических операций короче по сравнению с лапароскопическими. В отношении данного параметра нами были получены аналогичные результаты (3 vs 9 к/д; p<0,001). Кроме того, по данным мета-анализа, опубликованного в 2015 г., для группы РАЛРП при сравнении с ЛРП были характерны такие отличия, как более низкий процент конверсий в открытую хирургию или нефрэктомию, меньшая продолжительность тепловой ишемии, меньшие изменения СКФ в послеоперационном периоде, а также более короткие сроки пребывания в стационаре [20].
Уровень креатинина сыворотки крови в ближайшем послеоперационном периоде был выше в группе ЛРП (117,5 vs 94,3 мкмоль/л, p 0,004). В отношении данного результата требуется дальнейшее наблюдение пациентов и оценка динамики изменения СКФ. Так, например, в исследовании, посвященном сравнительному анализу лапароскопической и открытой резекции почки, большее снижение СКФ в группе ЛРП было характерно для раннего послеоперационного периода, но через 3,5 года наблюдения различий между группами не наблюдалось [21].
В отличие от роботической резекции почки техника раннего снятия зажима с почечной артерии при выполнении лапароскопической операции использовалась лишь в 9 случаях (53,1 vs 25% соответственно; p<0,05). Опубликованы данные [22], согласно которым указанная техника снижает риск развития такого осложнения, как псевдоаневризма почечной артерии. Это редкое, но серьезное послеоперационное осложнение, в большинстве случаев требующее проведения ангиоэмболизации [23]. Мы стараемся применять метод раннего снятия зажима с почечной артерии при выполнении РАЛРП как можно чаще именно с целью уменьшения продолжительности тепловой ишемии. Метод резекции почки без наложения сосудистого зажима чаще встречался в группе лапароскопических операций (27,7 vs 11,1%; p 0,043). При выполнении робот-ассиcтированной резекции мы редко используем технику off-clamp, предпочитая сохранять наилучшую визуализацию краев резекции в максимально «сухом» операционном поле. Не исключено, что здесь играет роль фактор «разобщенности» консольного хирурга и ассистента в аспекте стерильности, заставляющий избегать потенциально плохо контролируемых интраоперационных ситуаций без ущерба для успешного исхода операции.
Доля опухолей с преимущественно экзофитным характером роста преобладала в группе ЛРП (83,4 vs 34,92%, p<0,001). Полученных нами данных недостаточно, чтобы сделать окончательные выводы. Однако мы считаем, что все имеющиеся уникальные преимущества роботической хирургической системы позволяют выполнять минимально-инвазивную резекцию почки в наиболее технически сложных случаях, в том числе при опухолях с маскимальным баллом по шкале нефрометрии.
В то же время поиск ответа на вопрос, какой метод все-таки предпочтительнее, еще не завершен.
Ретроспективное исследование 18 724 случаев робот-ассистированной резекции почки, опубликованное в British Journal of Urology в 2018 г., продемонстрировало, что основным прогностическим фактором, влияющим на исход РАЛРП, является количество таких операций, регулярно выполняемых в клинике [24]. Схожие результаты получены и в исследовании французских авторов во главе с Peyronnet, включившем 1222 случая робот-ассистированных резекций почки [25]. С учетом данных публикации Arora от 2018 г. минимальный порог количества роботических операций в клинике – это 18–20 случаев ежегодно [26].
Как видно, данный госпитальный объем вполне достижим. В пользу робот-ассистированной хирургии говорит и исследование Hanzly [27], посвященное сравнению кривой обучаемости. Для роботических операций кривая обучаемости оказалась значительно короче, чем для лапароскопических (25 и 200 случаев соответственно).
Заключение. Мы считаем, что роботическая платформа интуитивно удобна для выполнения резекции почки, позволяя выбирать потенциально более сложные случаи и расширяя показания к органосохраняющей операции. Несмотря на неочевидность экономической целесообразности робот-ассистированной хирургии, требуются дальнейшие исследования для того, чтобы оценить экономические последствия предполагаемых преимуществ РАЛРП в виде снижения продолжительности госпитализации и улучшения функциональных результатов. Говоря о преимуществах и недостатках роботизированной хирургии, нам стоит также принимать во внимание тот факт, что все возможности роботической технологической экосистемы в силу ряда причин пока не доступны, но в обозримом будущем могут быть оценены по достоинству, став частью рутинной хирургической практики.



