Актуальность. Патогенез образования мочевых камней сложен и до конца не изучен. Несмотря на внедрение современных высокотехнологичных методов лечения и препаратов для патогенетической терапии, частота рецидивов не снижается [1–4]. Патогенез заболевания условно разделен на два типа – каузальный и формальный [5]. Первый из них учитывает как внешние, так и внутренние причины заболевания. Второй основан на интерпретации только местных факторов патогенеза, в частности МФЛ – диурез, рН мочи, промоутеров (Са, Ох, Ur, P) и ингибиторов (Cit, Mg, THP, UP, OP и т. д.) камнеобразования [6]. Оценивая эти параметры, обычно проводят селективную профилактику, т.е. исходно выполняется биохимическое исследование мочи и оценка диуретической способности почек, затем подбирается медикаментозное лечение. Согласно исследованиям С. Pak et al. [7], при подобной коррекции улучшение состояния наблюдается у 88% больных, в 99% случаев предупреждается повторное камнеобразование. В то же время при неселективном подходе эти показатели составляют только 70 и 89% соответственно [7]. Причем расходы на неселективное лечение значимо больше, чем на селективное.
Между тем выполнение функциональных и метаболических исследований сегодня не является рутинным вследствие затратности как по цене, так и по расходу времени.
В связи с этим возникает вопрос о проведении неселективной эмпирической терапии по аналогии с выбором антибактериального препарата при инфекциях мочевыводящих путей согласно эпидемиологии возбудителя.
Состояние МФЛ в различных регионах разнообразно [1, 8, 9], так как оно зависит от многочисленных внешних и внутренних факторов. Вследствие этого компоненты медикаментозной профилактики можно выбирать, опираясь на среднестатистические показатели МФЛ в каждом регионе, а значит, их исследование в различных регионах представляется актуальным и целесообразным.
Цель исследования: изучить особенности МФЛ кальциевого уролитиаза в Ташкенте и оценить результаты их эмпирической коррекции.
Материалы и методы. Для изучения состояния диуреза и МФЛ использованы данные обследования 779 жителей Ташкента с кальциевым типом мочевого камнеобразования неосложненного течения. Среди пациентов было 446 (57,25%) мужчин и 333 (42,75%) женщины, их возраст варьировался от 17 до 79 лет.
У 99 больных неосложненным кальций оксалатным уролитиазом оценены результаты трех вариантов медикаментозной коррекции. Кальциевый тип уролитиаза у этих больных был подтвержден анализом состава камня, наличием оксалатной кристаллурии и рН мочи менее 5,8. Пациенты были разделены на три группы, согласно выбранному лечению.
В 1-й группе проведено лечение щелочным цитратом (ЩЦ; К-Na-цитрат) (Литрен, «ATM PHARM», Узбекистан) 21 больного, средний возраст которого составил 39,1±4,1 года (21–62 года). Препарат назначали по 1 пакетику 3 раза в день под контролем рН мочи. Продолжительность курса лечения составила 1 мес. Один пакетик массой 3 г содержит лимонную кислоту 1197 г, калия гидрокарбоната – 967,5, натрия цитрата – 835,5 мг. В каждой коробке есть тест-полоски для измерения реакции мочи и дневник регистрации.
Во 2-й группе, которую составили 56 пациентов в возрасте от 18 до 65 лет (средний возраст – 36,3±5,2 года), назначали фитотерапию комплексным растительным препаратом (Канефрон Н «Бионорика CЕ», Германия) по 50 капель 3 раза в день до еды. Продолжительность курса лечения составила 2 мес. Контрольные исследования проводили на 30-е и 60-е сутки. Канефрон Н – экстракт из лекарственного растительного сырья, в 100 мл раствора которого содержатся золототысячника трава 0,6 г, любистока лекарственного корни – 0,6 г, розмарина листья – 0,6 г.
В 3-й группе проводили комбинированное лечение ЩЦ+ФП (Литрен+Канефрон Н). Средний возраст 22 пациентов составил 38,8±4,4 года (22–61 год). Продолжительность курса лечения составила 1 мес.
Диурез контролировали путем заполнения пациентами дневников диуреза до начала, далее на 30-е и 60-е сутки лечения.
Для диагностики состояния МФЛ проводили биохимическое исследование мочи на анализаторе Humalyzer 2000 («Human GmbH», Германия). Определяли содержание в моче: кальция, магния, оксалата, мочевой и лимонной кислот. Затем рассчитывали их суточную экскрецию (СЭ).
Величину рН мочи в клинике измеряли в течение 5 мин после забора образца при помощи иономера ЭВ-74.
В домашних условиях пациенты регистрировали реакцию мочи при помощи тест-полосок.
До включения пациентов в группы лечения кристаллурию оценивали по методике, предложенной Ф. А. Кле-пиковым [10].
Для оценки эффективности коррекции метаболических нарушений рассчитывали индекс ионной активности мочевого камнеобразования кальций-оксалатного соединения – АP[СаОх] [11].
Статистическая обработка выполнена при помощи общепринятых статистических программ «Microsoft Excel 2013», «Microsoft Access 2013», а также пакета статистических программ «R for Windows 2.15.0». Статистическая значимость полученных измерений при сравнении средних величин определена по критерию (t) Стьюдента.
Результаты. Анализ показателей базового исследования диуреза и МФЛ у пациентов с кальциевым типом мочевого литогенеза выявил, что самой распространенной патологией является гипоцитратурия, которая имела место в 96,92% наблюдений (у 755 больных). Вторым по частоте был сниженный объем суточного диуреза – 96,53% (у 752 больных). Также значимой по встречаемости патологией оказалась гипероксалурия, которая наблюдалась в 92,94% случаев (у 724 больных). Другие виды нарушений регистрировали несколько реже. Так, кальциурия, требующая коррекции, – более 5 ммоль/сут (не путать с гиперкальциурией, когда суточная экскреция превышает 8 ммоль/сут) отмечена в 73,68% случаев (у 574 больных). Реакция мочи ниже 5,8, требующая ее коррекции [12], встречалась только в ¾ случаев (72,66%; 566 больных). Снижение магнийурии зафиксировано в 71,76% (у 559 больных). Уровень СЭ Ur>4,0 ммоль/сут расценивается как гиперурикозурия. Медикаментозная коррекция показана уже при СЭ Ur>3,6 mmol/24h. Среди наших пациентов с кальциевым уролитиазом гиперурикозурия наблюдалась в 21,05% (у 164 больных).
С учетом выявленных фактов лечение в трех группах было направлено на различные МФЛ. В 1-й группе проведена коррекция цитратурии, во 2-й – стимулировали диурез, в 3-й группе осуществлено сочетанное воздействие на цитратурию и диурез. В связи с тем что ЩЦ назначают для подщелачивания мочи, показатель рН также был выбран в качестве критерия оценки.
В 1-й группе пациентов, получавших терапию Литреном (табл. 1), обнаружено достоверное увеличение цитратурии на 54,14% от исходного уровня и реакции мочи на 18,63%. Диурез в течение месяца не изменился. Риск камнеобразования, согласно снижению величины AP[CaOx], снизился на 50,63%. В процессе лечения 2 пациента в связи с диспепсическими расстройствами при длительном приеме (на 3-й и 4-й неделях) самовольно прекратили лечение и выбыли из исследования.

Во 2-й группе больных, получавших терапию Канефроном Н (табл. 2), в первую очередь констатировали достоверное увеличение диуреза на 32,17% к 30-м суткам и на 26,96% – к концу 2-го месяца фитотерапии по отношению к исходному показателю (р<0,05). Цитратурия имела только тенденцию к росту на 1,67% (р>0,05) к 30-м суткам и на 6,11% (р>0,05) – к концу 2-го месяца фитотерапии (на 3,88% в среднем за 2 мес.). Реакция мочи изменилась на 10,82% (р<0,05) к 30-м суткам и на 6,21% (р>0,05) – к концу 2-го месяца фитотерапии. Риск камнеобразования уменьшился на 32,59 и 31,2% в соответствующие сроки (р<0,05).

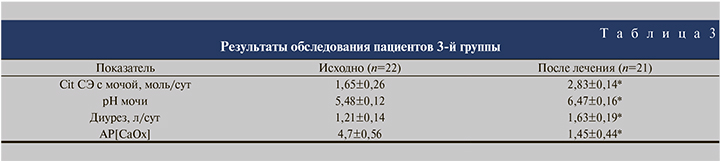
В 3-й группе комбинированного лечения (табл. 3) к 30-м суткам лечения наблюдали увеличение цитратурии на 71,52% (р<0,05), рН мочи на 18,07% (р<0,05) и диуреза на 34,71% (р<0,05). Риск камнеобразования снизился на 69,15 %. Курс лечения завершил 21 пациент: 1 пациента также в связи с диспепсическими расстройствами самопроизвольно прекратил прием препаратов и выбыл из исследования на 4-й неделе лечения.
Обсуждение. Селективная терапия по сравнению с неселективной имеет лучшие результаты, поскольку, исходно владея информацией о состоянии МФЛ, можно индивидуально подбирать лечение. Однако, учтя дороговизну и временную затратность метаболического обследования, мы решили провести медикаментозную профилактику, руководствуясь региональными среднестатистическими показателями, которые отличаются в различных регионах мира [9, 13]. У больных кальциевым уролитиазом в Ташкенте патологические отклонения по частоте распределились в следующем порядке: гипоцитратурия (96,92%), снижение диуреза (96,53%), гипероксалурия (92,94%), повышенная кальциурия (73,68%), снижение pH мочи (72,66%) и гипомагнийурия (71,76%). Следовательно, в первую очередь таким пациентам необходимо проводить коррекцию цитратурии и стимуляцию диуреза, после этого – коррекцию оксалурии, но с предварительным определением причины ее повышения (первичная или вторичная). Далее необходимо обратить внимание на нормализацию экскреции Ca с мочой и величину pH мочи.
Для коррекции цитратурии и рН выбран ЩЦ отечественного производства Литрен. Проведенное ранее клиническое исследование [14] подтвердило его способность подщелачивать мочу пациентов с кислой реакцией, растворять мочекислые камни и конгломераты, а также его эффективность для метафилактики рецидивного камнеобразования у больных с мочекислым, цистиновым и кальциевым типами камнеобразования. В том же исследовании зафиксировано скорое избавление от камней и их фрагментов после дистанционной ударноволновой литотрипсии, чрескожной нефролитотрипсии и при комбинированной терапии после эндоскопических вмешательств, что позволило сократить срок потери трудоспособности и способствовало скорейшему возвращению пациентов к нормальной, полноценной трудовой деятельности и социальной активности.
В данном исследовании Литрен назначали для увеличения цитратурии. Согласно инструкции, ЩЦ показаны для повышения рН мочи. Поэтому параллельно с цитратурией происходит изменение в реакции мочи, хотя необходимость в коррекции рН существует, как было указано выше, только в 72,66%.
Во 2-й группе больным назначали ФП Канефрон Н в каплях. Препарат является умеренным мягким диуретиком, кроме того, влияет на ряд параметров мочи, непосредственно участвующих в формировании конкрементов.
Для третьего варианта, сочетанной коррекции цитратурии и стимуляции диуреза, выбрали те же препараты –
Литрен и Канефрон Н, так как этот вариант доступнее, проще в выполнении и легко контролируем, чем коррекция оксалурии.
Более детальный анализ подтвердил, что выраженное увеличение экскреции цитратов наблюдается у больных с исходно пониженным их уровнем (гипоцитратурия). Эффективность по коррекции цитратурии составила 80,95% в 1-й группе (у 17 из 21 больного) и 86,4% в 3-й (у 19 из 22 больных). Во 2-й группе цитратурия имела тенденцию к росту в 73,2% случаев (у 41 из 56 больных). Наблюдаемое достоверное усиление цитратурии у пациентов 1-й и 3-й групп непосредственно связано с приемом препарата Литрен.
Эффективность по коррекции рН мочи составила 18,63% в 1-й группе и 8,52% во 2-й (в среднем за весь 2-месячный курс фитотерапии). В 3-й группе показатель рН изменился на 18,07%. Это также подтверждает прямую связь изменения реакции мочи с препаратом Литрен.
Изменения диуреза наблюдали только во 2-й и 3-й группах, т.е. при использовании Канефрона Н. К 30-м суткам лечения диурез в группах соответственно повысился на 32,17 и на 34,71% от исходного уровня. Щелочной цитрат на данный параметр влияния не оказывает, в связи с чем и возникает необходимость в комбинации с диуретиками.
В процессе изготовления комплексных фитопрепаратов производство ориентировано не на выделение действующего вещества, а на сохранение всего комплекса активных веществ растения, приближенного к естественным формам. Растения содержат множество биохимических ингредиентов, влияние которых на организм как по отдельности, так и в сочетаниях зачастую неизвестно. Преимущество синтетических препаратов, даже изначально обнаруженных в растениях, состоит в том, что их состав постоянен. А в случае ФП приходится иметь дело с многообразными и непредсказуемыми сочетаниями химических соединений из лекарственных растений [15].
Экспериментальными и клиническими исследованиями была подтверждена способность Канефрона Н (капли) при длительном применении кроме стимуляции диуреза изменять экскрецию промоутеров и ингибиторов литогенеза, а также подщелачивать мочу [16]. Такое многофакторное влияние ФП наиболее подходящее для профилактики рецидивов [17].
Повышение рН коррелирует с концентрацией цитрата в моче [7]. Менее 1% цитрата, поступающего с пищей, выделяется с мочой в неизмененном виде (как цитрат). Согласно данным C. Y. Pak [18], после фильтрации в почке 75% цитрата реабсорбируется главным образом в проксимальном канальце, а остальная часть выводится с окончательной мочой. При назначении Канефрона Н повышение цитратурии и рН мочи может быть обусловлено усилением клубочковой фильтрации и умеренным снижением канальцевой реабсорбции. С другой стороны, это может быть и результатом воздействия биохимических ингредиентов лекарственных растений, входящих в состав препарата, на метаболизм МФЛ. Каждое из лекарственных растений имеет сложный биохимический состав. При этом эти вещества как в отдельности, так и в сочетании с другими оказывают разнообразные и порой непредсказуемые эффекты. Известно [19, 20], что некоторые органические кислоты, как малат, фумарат, сукцинат и тартрат, способны усиливать экскрецию цитрата, обеспечивая щелочную нагрузку и увеличенный субстрат для синтеза внутрипочечного цитрата. Тем не менее для подтверждения этих гипотез необходимы отдельные углубленные специализированные исследования.
Согласно данным литературы, при значениях AP[CaOx] менее 1,6 риск камнеобразования низкий, 2,8 и более – высокий [10]. Исходное состояние всех 99 пациентов по данному критерию следует оценивать как тяжелое. После проведенного лечения наблюдали достоверное снижение индекса в каждой группе. В 1-й и 2-й группах он снизился только до уровня умеренного риска (1,6<AP[CaOx]<2,8). При сочетанном назначении ЩЦ и ФП индекс снизился до низкого уровня (AP[CaOx]<1,6), т.е. наиболее существенно удалось улучшить состояние пациентов 3-й группы. Литрен нормализовал цитратурию и реакцию мочи, Канефрон Н – в первую очередь диурез, а также, обладая комплексным многофакторным действием, изменил экскрецию Са, Ох и Мg [13]. При расчете в формулу наряду с диурезом и цитратурией входят и кальциурия, и магниурия, и оксалурия. Следовательно, индекс больше всего и должен был снизиться в 3-й группе комплексной терапии ЩЦ+ФП (на 69,15%). Выраженный цитратуретический эффект Литрена при этом усиливался многофакторным эффектом Канефрона Н.
Длительный прием ЩЦ нередко сопряжен с развитием нежелательных эффектов (НЭ) этой группы препаратов.
В частности, мы наблюдали расстройство функции желудочно-кишечного тракта. У 3 больных он проявился по прошествии 3–4 нед. лечения. При монотерапии НЭ наблюдался у 2 (9,5%) пациентов, при сочетании ЩЦ и ФП – только у 1 (4,5%). Возможно, комбинация ЩЦ с ФП позволила в определенной степени компенсировать нежелательное действие и улучшить переносимость длительного применения: в 3-й группе она составила 95,5 против 90,5% во 2-й группе.
Заключение. В Ташкенте у больных кальциевым уролитиазом патологические отклонения по встречаемости (в порядке убывания) распределены следующим образом: гипоцитратурия–снижение диуреза–гипероксалурия–патология кальциурии–снижение pH мочи–гипомагнезиурия. В связи с этим профилактическое лечение при кальциевом уролитиазе желательно начинать с коррекции экскреции цитрата и стимуляции диуреза.
Полученные результаты подтверждают потенциал эмпирической терапии на основе специфики среднестатистических показателей региона. Особо эффективно сочетание препаратов с целью нормализации нескольких параметров литогенеза. В частности, ЩЦ со специфическим узким эффектом и ФП, обладающего многофакторным действием. Так, сочетание Литрена и Канефрона Н оказалось наиболее подходящим, при этом активность мочевого литогенеза снизилась до низкого уровня (AP[CaOx]<1,6). Также удалось компенсировать НЭ длительного приема синтетического препарата. Тем не менее считаем, что для подтверждения обоснованности подобного подхода необходимы длительные контролируемые исследования, а полученные результаты следует расценивать как перспективные.



