Введение. Доброкачественная гиперплазия предстательной железы (ДГПЖ) – распространенное возрастзависимое хроническое заболевание, возникающее в результате прогрессирующего увеличения предстательной железы вследствие незлокачественной пролиферации эпителиальных и гладкомышечных клеток. [1] Разрастание тканей вокруг уретры сужает ее просвет, что приводит к появлению симптомов нижних мочевыводящих путей (СНМП).
К данным симптомам относятся учащенные позывы к мочеиспусканию, ощущение неполного опорожнения мочевого пузыря, ноктурия и снижение скорости потока мочи. Хронический простатит (ХП), в основе которого лежит воспаление, также является состоянием, значительно снижающим качество жизни мужчин [2]. Точная этиология ХП до сих пор полностью не установлена. В различных источниках литературы упоминаются нераспознанная бактериальная инфекция, психогенные факторы, ретроградный поток мочи в протоках предстательной железы или дисфункция тазового дна [3]. Хронический простатит может наблюдаться у взрослых мужчин независимо от их возраста. Однако чаще такой диагноз встречается у молодых мужчин с жалобами на боль при мочеиспускании и сексуальные проблемы. Характер сексуальных расстройств весьма неоднороден, и во многих сообщениях зафиксирована высокая распространенность эректильной дисфункции среди больных ХП [4]. Существует множество стратегий лечения СНМП в зависимости от степени тяжести симптомов, а также предпочтений пациента. Они включают модификацию образа жизни, медикаментозную терапию и хирургическое лечение. Альфа-1-адреноблокаторы (α1-АБ) являются общепризнанным вариантом медикаментозной терапии первой линии выбора [5–7].
Отдельного внимания заслуживают работы, посвященные критериям неэффективности монотерапии α1-АБ. Так, B. S. Kim и соавт. используют в качестве интегрального показателя длину простатического отдела уретры. Согласно результатам исследования, при длине простатического отдела уретры более 45 мм и длине переходной зоны более 35 мм монотерапия оказалась неэффективной, и оперативное пособие было оказано в течение первого года. Чувствительность данных прогностических критериев составила 83,3%, а специфичность длины переходной зоны оказалась выше: 77,9 против 61,6% для длины простатического отдела уретры [8]. Поэтому одним из самых актуальных направлений в консервативном лечении СНМП при ДГПЖ и ХП является комбинированная терапия, которая, по мнению многих авторов, дает значительное преимущество в выборе персонифицированного подхода к лечению [9].
E. J. Kruep и соавт. в ретроспективном анализе за 4 года на базе данных MarketScan, включавшего 8617 мужчин, сравнили исходы ранней (через 30 сут. после начала приема α1-АБ) и отсроченной комбинированной терапии (между 30 и 180 сут. после начала приема α1-АБ) препаратами ингибиторов 5-альфа редуктазы (5-АРИ) и α1-АБ. В своем исследовании авторы пришли к выводу, что раннее назначение комбинированной терапии 5-АРИ и α1-АБ пациентам с симптоматической формой ДГПЖ значительно снижает риск развития острой задержки мочи (ОЗМ) и прогрессии ДГПЖ, требующей оперативного лечения [10].
В настоящее время не существует стандартного метода лечения СНМП, подходящего любому больному. Выбор метода лечения должен осуществляться врачом индивидуально с учетом всех сопутствующих факторов (медицинских и социальных) и при активном участии самого пациента. Последующие исследования должны быть направлены на создание алгоритма, предназначенного для отбора пациентов к проведению комбинированной терапии СНМП.
В последнее время определяется растущая тенденция к использованию препаратов биологического происхождения при различных заболеваниях. Одним из лекарственных препаратов, вызывающих наибольший интерес к применению в лечении СНМП у мужчин, является Аденопросин®. Из биомассы насекомых вида непарный шелкопряд (Lymantria dispar) получают субстанцию, оказывающую противовоспалительное специфическое антиоксидантное действие [11].
Целью данного наблюдательного исследования являлось изучение и оценка эффективности применения Аденопросин® в комбинации с другими препаратами по сравнению с монотерапией препаратом Аденопросин®.
Материалы и методы. Данное когортное наблюдательное исследование было проведено на базе 221 лечебно-профилактического учреждения в 39 городах Российской Федерации. В рамках наблюдательного исследования, проведенного с ноября 2020 по декабрь 2022 г., были проанализированы данные 6442 пациентов. От каждого пациента было получено письменное информированное согласие на участие в исследовании. В исследование были включены мужчины старше 45 лет с диагностированными СНМП в течение 6 мес., с IPSS (международная шкала оценки симптомов простаты) ≥10 баллов и максимальной скоростью потока мочи (Qmax) от 5 до 15 мл/с. К критериям невключения относили нейрогенные заболевания (рассеянный склероз, болезнь Паркинсона, поражения спинного мозга, полинейропатия), хирургическое лечение органов малого таза (онкологические операции на органах малого таза, нижних мочевыводящих и половых путях), рак простаты, обострение инфекционных заболеваний мочевыводящих путей, нарушения функции почек.
Препарат Аденопросин® 150 мг в форме ректальных суппозиториев был назначен в качестве монотерапии I группе и в комбинации с другими препаратами (α1-АБ, нестероидные противовоспалительные препараты [НПВП], антибактериальные и другие препараты для лечения урологических заболеваний) – II группе. Перед началом лечения проводились: сбор анамнеза, антропометрических показателей, установление диагноза, подбор и назначение терапии в зависимости от тяжести заболевания. По завершении 30 дней терапии оценивались динамика состояния, эффективность и переносимость проведенного лечения. Регистрация показателей массы тела и индекса массы тела (ИМТ), физикальный осмотр, урофлоуметрия, объем предстательной железы (по данным УЗИ) и объем остаточной мочи (по данным УЗИ) оценивались до и после лечения. Также выполнялась оценка состояния пациента с использованием шкалы симптомов хронического простатита Национального института здоровья (NIH-CPSI), Международного индекса эректильной функции (МИЭФ-5), The International Prostate Symptom Score (IPSS) и оценка качества жизни (QoL).
Статистический анализ данных. База данных была полностью валидирована перед началом анализа. Анализ данных производился в программном пакете IBM SPSS v 26.0.
В данном исследовании были использованы методы описательной статистики (параметрические и непараметрические тесты). Большинство анализируемых переменных были дискретными, кроме переменной группы (номинальная переменная).
Нормальность распределения изначально определялась методами Колмогорова–Смирнова и Шапиро-Уилка.
В случае расхождении результатов этих двух тестов для принятия верного решения в отношении нормальности или неоднородности распределения проводилось два дополнительных теста: Kurtosis-test и Skew-test – тесты эксцесса и асимметрии. В упомянутых тестах происходило сравнение эксцесса и асимметрии по изучаемому параметру с нормально распределенной выборкой (сгенерированной математически симуляцией нормальной выборки) и имеющейся выборкой значений изучаемой переменной. Н0 – нулевая гипотеза состояла в том, что значения эксцесса или асимметрии (в зависимости от выполняемого теста) были взяты из нормально распределенной выборочной совокупности при p≥0,05. Следовательно, меньшие значения p отвергали Н0 (аналогично тестам Колмогорова–Смирнова и Шапиро–Уилка) и свидетельствовали, что значения асимметрии и эксцесса, вероятно, получены из неоднородного (отличного от нормального) распределения. Так как тесты асимметрии и эксцесса также подвержены ложноположительным и ложноотрицательным результатам и для принятия финального взвешенного решения в отношении нормальности или неоднородности распределения – выводились гистограммы распределения по соответствующим «спорным» параметрам.
Для нормально распределенных данных применялся t-критерий Стьюдента. Для данных, имевших распределение, отличное от нормального, применялись непараметрические методы: межгрупповое сравнение и субпопуляционный анализ проводились с использованием критериев Манна–Уитни (U-критерий), Краскела–Уоллиса (h-критерий). Внутригрупповые сравнения (анализ динамики показателей) проводились с использованием критерия Вилкоксона (W-критерий). Визуальное представление данных выполнено с помощью столбчатых диаграмм и таблиц.
Результаты. Валидированный диагноз был установлен 6375 мужчинам, остальные пациенты не вошли в исследование из-за несоответствия критериям. 1498 имели ДГПЖ, 3060 – ХП, 1817 – ДГПЖ и ХП.
Завершил исследование 6341 пациент. 34 человека не явились по разным причинам, не связанным с безопасностью и переносимостью назначенной терапии. В результате 3580 пациентов получали монотерапию препаратом Аденопросин®, 2761 – комбинированную терапию. В большинстве случаев врачи назначали комбинированную терапию пациентам с более тяжелым течением заболевания.
В табл. 1 представлены характеристики пациентов, получавших лечение препаратом Аденопросин® в комбинации с другими препаратами и в качестве монотерапии.
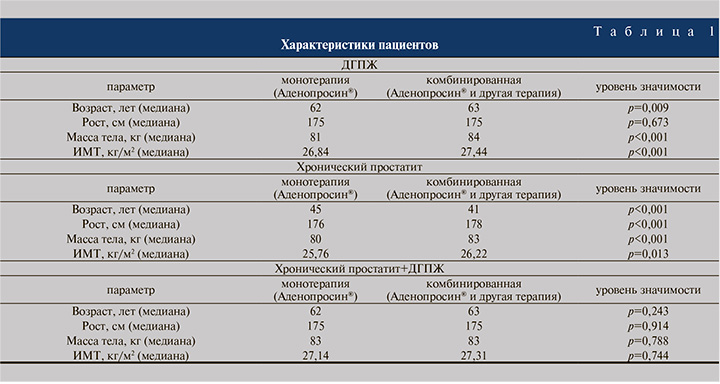
Во второй группе в комбинации с препаратом Аденопросин® назначали: α1-АБ (Тамсулозин, Доксазозин, Теразозин, Силодозин), препараты с экстрактом простаты, антибактериальные препараты (фторхинолоны, сульфаниламиды, тетрациклины, цефалоспорины III поколения, макролиды, нитрофураны), антисептики противопротозойные и бовгиалуронидазу азоксимер.
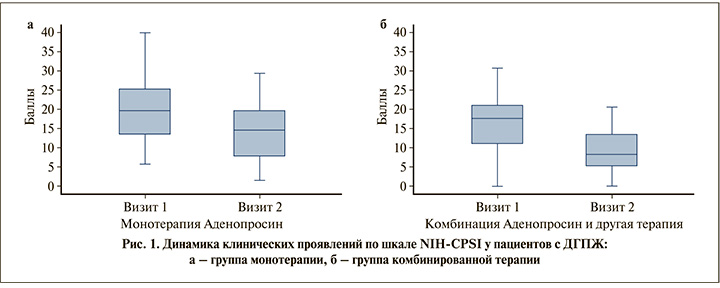
Результаты пациентов с ДГПЖ в обеих группах продемонстрировали значительное улучшение, однако баллы по шкале NIH-CPSI были ниже при комбинированной терапии (p=0,005) (рис. 1), что связано с более тяжелой стадией заболевания у пациентов в группе с комбинированной терапией. У пациентов с ДГПЖ после лечения отмечены положительные изменения в пользу I группы по критериям оценки объема остаточной мочи (p<0,001), объема предстательной железы (рис. 2). Также группа с монотерапией показала статистически более значимые результаты при оценке баллов по шкале МИЭФ-5 (p<0,001). Qmax статистически достоверно увеличилась в обеих группах: в I группе с 14 до 17 мл/с, во II – с 12 до 14 мл/с (рис. 3).
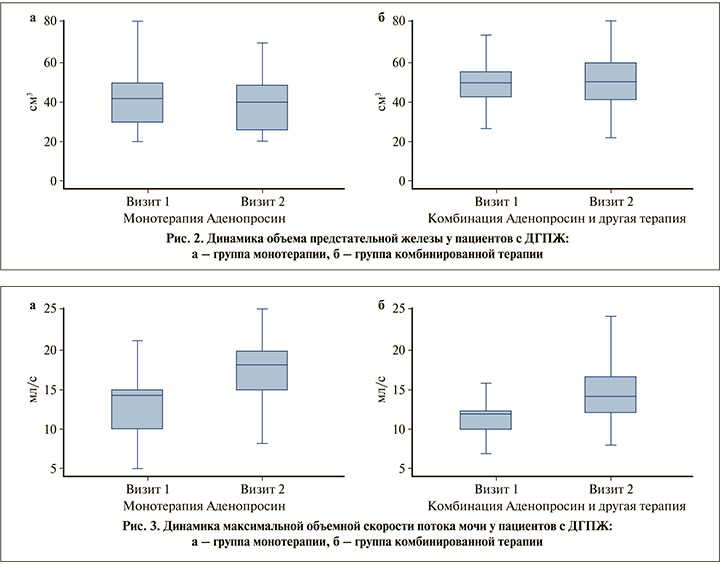
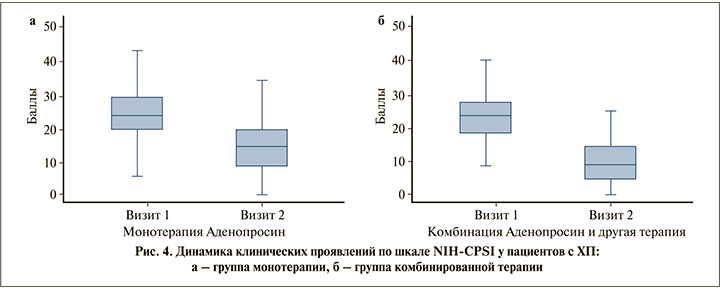
У пациентов с ХП монотерапия и комбинированная терапия продемонстрировали статистически значимые положительные изменения при оценке баллов по шкале NIH-CPSI (p=0,005) (рис. 4), по шкале IPSS (p<0,001) и средней объемной скорости потока мочи (p<0,001). Обращает на себя внимание, что после лечения была отмечена более выраженная положительная динамика в I группе при оценке баллов по шкале QoL (p<0,001) и значительное улучшение максимальной объемной скорости потока мочи (p<0,001).
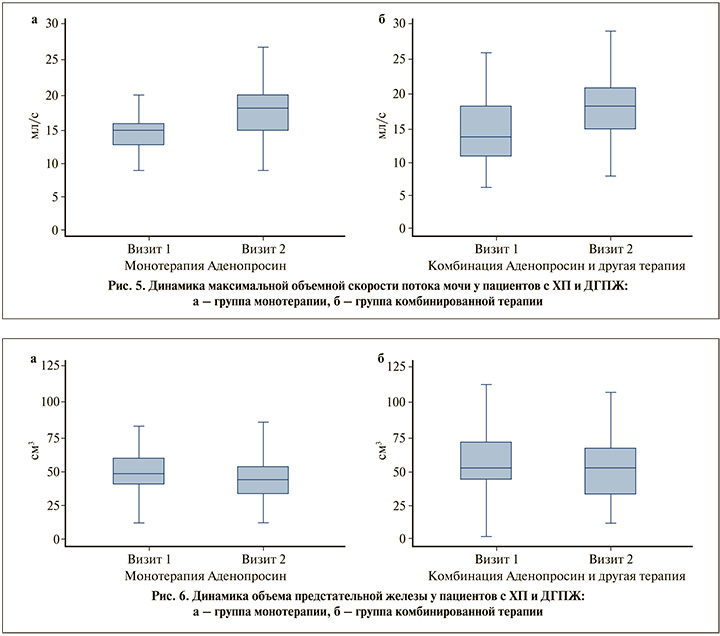
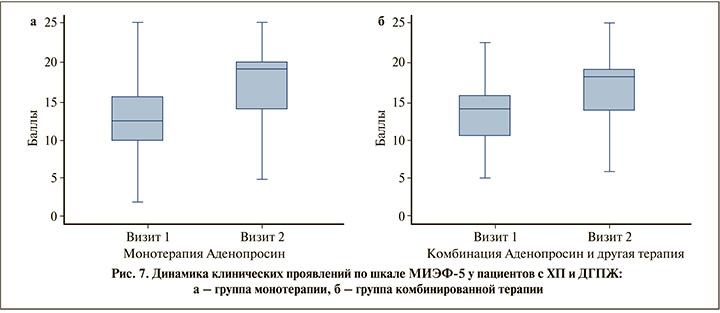
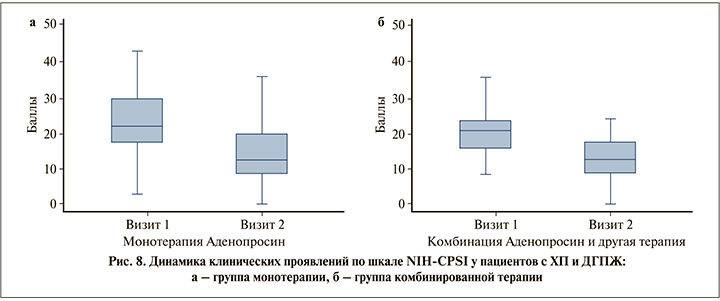
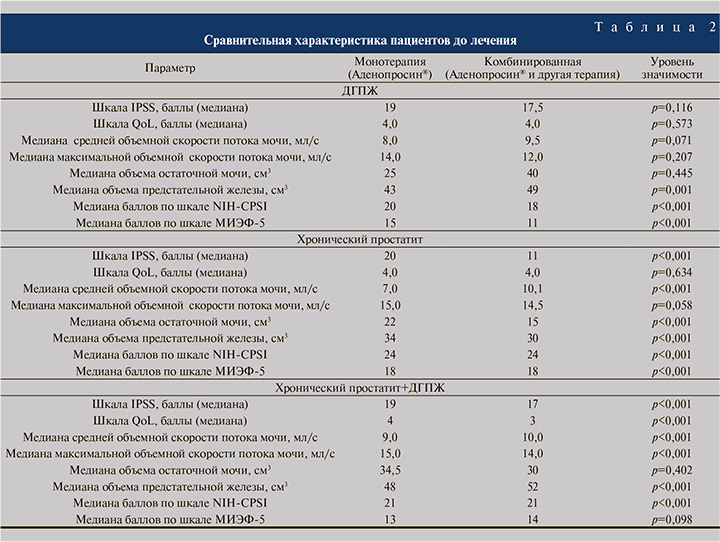
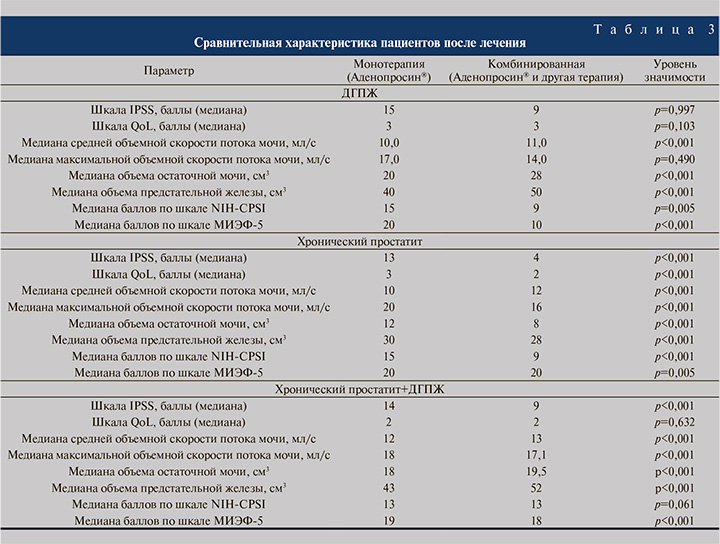
Пациенты с ДГПЖ и ХП после лечения показали статистически значимое улучшение максимальной объемной скорости потока мочи (p<0,001) (рис. 5), меньший объем остаточной мочи (p<0,001) и уменьшение объема предстательной железы (p<0,001) (рис. 6), в I группе показатели были более значимыми. Также монотерапия продемонстрировала преимущество по шкале МИЭФ-5 (p<0,001) (рис. 7), однако уступила комбинированной терапии при оценке баллов по шкале IPSS (p<0,001). Назначение препарата Аденопросин® в схеме терапии было эффективным в обеих группах (в монорежиме и в комбинации): была продемонстрирована статистически значимая положительная динамика при оценке баллов по шкале NIH-CPSI (p=0,005) (рис. 8). В табл. 2–3 представлены подробные сравнительные характеристики обеих групп пациентов до и после лечения.
Обсуждение. Результаты проведенного наблюдательного исследования демонстрируют клиническую эффективность применения препарата Аденопросин® в качестве монотерапии, а также в комбинации с другими препаратами.
В результате монотерапии отмечены статистически значимые положительные изменения по сравнению с комбинированной терапией в показателях объема предстательной железы, объема остаточной мочи и баллов по шкале МИЭФ-5 у пациентов с ДГПЖ и у пациентов с ДГПЖ и ХП. У пациентов с ХП в обеих группах отмечена статистически значимая положительная динамика при оценке баллов по шкале QoL и показателя максимальной объемной скорости потока мочи. В то же время комбинированная терапия продемонстрировала статистически значимые положительные изменения по сравнению с монотерапией в оценке баллов по шкале NIH-CPSI у пациентов с ДГПЖ и пациентов с ХП; баллов по шкале IPSS у пациентов с ХП и ДГПЖ+ХП, а также средней скорости мочеиспускания у мужчин с ХП. Для пациентов с ДГПЖ в группе комбинированной терапии эффективность и динамика были выше, что может быть связано с преобладанием более тяжелой клинической симптоматики.
Тщательный сбор анамнеза, использование валидированных опросников, инструментальных методов диагностики и правильно установленный диагноз являются основополагающим принципом для выбора наиболее эффективного метода терапии. Стоит отметить, что некоторое количество пациентов не прошли исследование полностью по различным причинам, таким как отсутствие заполненных данных опросников, отзыв согласия или неявка на контрольный осмотр.
В последнее время Аденопросин® вызывает большой клинический интерес как препарат для лечения СНМП. Результаты ряда исследований продемонстрировали высокую эффективность и безопасность данного препарата.
В работе В. Л. Медведева и соавт. (2020) [12] было доказано противовоспалительное действие на предстательную железу, уменьшение болевого синдрома, снижение общего балла NIH-CPSI, улучшение эректильной функции пациентов с хроническим бактериальным простатитом. В публикации 2021 г. Ю. Л. Демидко и соавт. [13] оценили результаты применения Аденопросина в клинической практике. Авторы заключили, что общая оценка эффекта уменьшения суммы баллов по шкале СНМП достоверна (р<0,0001) при применении препарата в комбинированной и монотерапии.
В исследовании А. С. Аль-Шукри и соавт. (2021) [14] оценили применение препарата Аденопросин® в комбинации с тамсулозином по сравнению с монотерапией тамсулозином. Было отмечено значительное снижение баллов по шкале IPSS, уменьшение объема остаточной мочи, увеличение скорости потока мочи и улучшение качества жизни.
Проспективное наблюдательное исследование П. С. Кызласова и соавт. (2023) было направлено на оценку эффективности и безопасности препарата Аденопросин® в качестве дополнения к стандартной терапии. Шестьдесят пациентов с установленным диагнозом ХП были разделены на две группы. Основной группе были назначены Аденопросин®, α1-АБ в стандартных дозировках и антибактериальная терапия. Пациенты контрольной группы принимали α1-АБ (тамсулозин) и антибактериальный препарат (левофлоксацин). Период наблюдения составил 3 мес. В основной группе наблюдалась более выраженная положительная динамика при оценке данных опросника IPSS (p=0,0267), NIH-CPSI (p=0,0201). Авторы пришли к выводу, что Аденопросин® обладает выраженным противовоспалительным действием у пациентов с ХП и может быть рекомендован в рамках комплексной терапии [15].
Важно отметить, что на данный момент существует небольшое количество публикаций с большой выборкой пациентов, посвященных изучению применения Аденопросин®. Участие более 6000 пациентов в данном исследовании является преимуществом и имеет большое клиническое значение в дальнейшем изучении эффективности и безопасности препарата.
Заключение. Лечение ДГПЖ, ХП и их сочетания является сложной клинической задачей. Множественный характер жалоб часто диктует необходимость одновременного назначения двух и более лекарственных препаратов. Комбинированная терапия включает использование нескольких терапевтических стратегий для лечения различных аспектов ДГПЖ и ХП.
Для терапии ДГПЖ показано, что комбинированный подход более эффективен, чем использование любого класса препаратов по отдельности, так как он снижает риск прогрессирования заболевания, острой задержки мочи и необходимости хирургического вмешательства. Однако комбинированную терапию следует рассматривать в индивидуальном порядке с учетом симптомов у конкретного пациента, размера простаты и общего состояния здоровья. Универсального метода лечения ДГПЖ, подходящего любому больному, не существует. Выбор метода/методов лечения должен осуществляться врачом-урологом индивидуально с учетом всех сопутствующих медицинских и социальных факторов.
Все сказанное в значительной степени относится и к лечению ХП и ХП+ДГПЖ. По результатам проведенного исследования Аденопросин® продемонстрировал эффективность как в качестве монотерапии, так и в комбинации с другими традиционными препаратами при лечении мужчин с СНМП.



