Введение. Хронический простатит (ХП) – это широко распространенное заболевание, частота симптомов которого в популяции, по разным оценкам, может достигать 9–25% [1, 2]. Следует отметить, что ХП не представляет непосредственной угрозы жизни, но существенно снижает ее качество [3], [4], за счет чего относится к социально значимым заболеваниям. Для ХП характерна полиморфная симптоматика: помимо боли, симптомов нижних мочевыводящих путей (СНМП), ухудшения эректильной функции у пациентов могут отмечаться бессонница, повышенная утомляемость и депрессивные эпизоды [5, 6]. На сегодняшний день предложено множество вариантов терапии ХП: антибиотики широкого спектра действия, ингибиторы 5-α редуктазы, альфа-адреноблокаторы, НПВП, модуляторы невропатической боли, препараты природного происхождения и др. [7, 8]. Точный механизм действия некоторых из них пока не установлен. Несмотря на широкий выбор препаратов и предложенные эффективные схемы многокомпонентной длительной терапии, ХП склонен к рецидивированию. Ввиду этого научное сообщество продолжает искать новые и альтернативные методы лечения [9].
Одним из перспективных направлений в лечении ХП является применение препаратов биологического происхождения [10]. Среди их преимуществ: минимальное количество побочных эффектов и патогенетический подход.
В ряде работ было доказано, что они обладают противовоспалительным, иммуномодулирующим эффектами, влияют на метаболические процессы в ПЖ, усиливают синтез антигистаминовых и антисеротониновых антител, а также улучшают микроциркуляцию в ПЖ [11]. Препараты на основе экстракта простаты крупного рогатого скота снижали выраженность болевого синдрома и других симптомов хронического простатита [12,13]. Экстракт Serenoa repens, изначально предложенный для профилактики прогрессирования ДГПЖ, также нашел свое применение в терапии простатита [10].
В 2010 г. на фармацевтическом рынке появился новый энтомологический препарат, Аденопросин, действующее вещество которого получают из биомассы личинок насекомых вида Непарный шелкопряд (Lymantria dispar) [14]. Препарат представлен в виде суппозиториев. Основным терапевтическим эффектом Аденопросина является выраженное противовоспалительное и антиоксидантное действия [15]. На сегодняшней день проведено достаточно много клинических исследований, демонстрирующих его эффективность в лечении пациентов с ХП и ДГПЖ, однако эти сведения еще не были должным образом обобщены. Цель данной работы – оценить в рамках систематического обзора и мета-анализа эффективность и безопасность Аденопросина в лечении больных ХП и/или ДГПЖ.
Стратегия поиска, отбор статей
Cистематический обзор и мета-анализ были проведены в соответствии с протоколом PRISMA. Для поиска статей использовались базы данных MEDLINE, Elibrary, Google Scholar, Сyberleninka. Поиск проводился с использованием комбинации ключевых слов «хронический простатит», «доброкачественная гиперплазия предстательной железы» и «Аденопросин», а также «chronic prostatitis», «benign prostatic hyperplasia» и «Adenoprosin». Хронологические ограничения не применялись. В соответствии с мнемоническим правилом PICO область интереса исследования была следующей: Patients – мужчины, страдавшие хроническим простатитом и/или гиперплазией простаты; Intervention – терапия Аденопросином (монотерапия или сочетание со стандартным лечением); Comparison – стандартная терапия ХП и ДГПЖ или плацебо; Outcomes – симптомы ХП и ДГПЖ на основании валидированных опросников, а также инструментальные исследования – показатели урофлоуметрии, объем простаты и остаточной мочи, количество лейкоцитов в секрете простаты, IIEF-5, Study types – рандомизированные контролируемые клинические исследования.
Критерии включения статей в анализ: исследования на русском/английском языке, наличие данных о сравнении Аденопросина (в составе комплексной терапии или в качестве монотерапии) с группой контроля (стандартная терапия без Аденопросина или плацебо) у пациентов, страдавших ХП и/или ДГПЖ.
Критерии невключения: другие типы исследований (обзорные статьи, описание единичных клинических случаев, абстракты, книги, комментарии, рекомендации, тезисы, протоколы исследований, клинические исследования без группы сравнения или без рандомизации); статьи на языках, отличных от русского и английского; статьи о других заболеваниях мочеполовой системы, доклинические исследования.
На первом этапе систематического поиска оценивалось соответствие названия публикации с интересующей темой и анализировался абстракт. Были исключены явно несоответствующие критериям работы. На втором этапе были исключены дубликаты статей. На третьем этапе был проведен анализ полных текстов работ в соответствии с критериями включения и невключения.
Извлечение данных
Из статей были извлечены и внесены в таблицу следующие данные: количество пациентов, рандомизированных в группу комплексного лечения с Аденопросином и в группу стандартной терапии, и их возраст. Показатели: баллы по опросникам NIH-CPSI (домен «боль», сумма баллов, домен качества жизни), IPSS (сумма баллов), МИЭФ-5, объем предстательной железы и остаточной мочи, концентрация лейкоцитов в секрете простаты, Qmax. Показатели оценены до проведения лечения и спустя в среднем 4 нед.

Статистический анализ
Анализ данных и мета-анализ проводились с использованием программы R v. 4.2 с библиотеками meta, metafor, dmetar [16].
Для всех включенных исследований были доступны измерения в начале и в конце исследования. Из них были вычислены дельты изменения, как: μизменения=μконец-μначало
Стандартные отклонения изменений были рассчитаны на основании метода, предложенного в Руководстве кокрановского сотрудничества[17]: sdизменения=√(sd2конец+sd2начало-2×ρ×sdконец×sdначало),
где ρ – коэффициент корреляции между конечным и начальным измерениями. В связи с тем что данный коэффициент является неизвестным, было принято допущение о том, что эмпирический коэффициент ρ=0,5. После вычислений была оценена динамика изменений по каждой группе (экспериментальная и контрольная) в каждом исследовании.
В качестве размера эффекта в мета-анализе проводилось сравнение рассчитанной динамики между экспериментальной и контрольной группами в виде среднего значения.
Гетерогенность была оценена методом обратной дисперсии, и ограниченный оценщик максимального правдоподобия (REML) был использован для оценки разброса распределения эффектов в модели случайных эффектов (τ2). Оценка гетерогенности была проведена путем расчета-статистики и ее значимости, а также статистик I2 – Хиггинса и Томпсона.
Приведены результаты для моделей и с фиксированными, и случайными эффектами. При низкой (I2 менее 25%) и умеренной гетерогенности рекомендуется ориентироваться на результаты модели с фиксированными эффектами, при более высокой гетерогенности – на результаты модели со случайными эффектами [18]:
Анализ чувствительности был проведен на основе leave-one-out подхода, когда оценивается влияние исключения каждого отдельного исследования на взвешенный эффект и гетерогенность. Оценка потенциального публикационного смещения была проведена визуально с помощью воронковидных графиков (применяя метод trim-and-fill), тест Эггера не выполнялся в связи со сравнительно малым количеством исследований в мета-анализе [19].
Уровень статистической значимости различий между выборками был установлен на p< 0,05.
Поиск в базах данных на 19.06.2023 позволил идентифицировать в общей сложности 196 работ. После применения всех указанных критериев включения и невключения и удаления дубликатов в обзор вошли 12 исследований [14, 15, 20–23, 25–30], опубликованных в период с 2010 по 2022 г. (см. таблицу). В приведенных исследованиях показатели в группах до начала терапии не имели статистических различий, поэтому они не приведены в данной таблице. Данные до начала и по окончании терапии, использованные в статистических расчетах, доступны в дополнительных материалах к статье. В таблице во избежание дублирования данных не приведена статья А. В. Кузьменко и соавт. [15], посвященная отдаленным результатам лечения, так как она основывается на той же выборке, что и предыдущая статья авторов с меньшим сроком наблюдения [22]. В экспериментальной группе проводилась терапия Аденопросином в сочетании со стандартной терапией, в контрольной – аналогичная стандартная терапия без Аденопросина. Количество пациентов, получавших Аденопросин в каждом исследовании, варьировалось от 18 до 61, группы контроля были сопоставимыми по размеру с экспериментальной группой. Диапазон продолжительности исследования составлял от 3 до 12 нед.
NIH-CPSI, домен «боль»
Данные опросника NIH-CPSI, домен «боль» были представлены в пяти исследованиях [14, 25, 28–30], все они вошли в мета-анализ. Лесовидный график приведен на рис. 1. Несмотря на высокую статистическую гетерогенность исследований (I2=99%), обе модели (фиксированных и случайных эффектов) демонстрируют статистически значимое преимущество экспериментальной группы над стандартной терапией (более значительное снижение балла по опроснику): -2,06 (95% доверительный интервал [ДИ]: -3.32, -0.45); р<0,01. Поочередное исключение исследований (анализ чувствительности) не сказалось на результате: все они показывают положительный эффект от Аденопросина.

NIH-CPSI, общий балл
Данные о сумме баллов по шкале NIH-CPSI также представлены в семи исследованиях [14, 22, 23, 25, 27–29]. Лесовидный график (рис. 2) показывает более значимые изменения в экспериментальной группе, различия статистически достоверны, в модели случайных эффектов разница: -3.39 (95%ДИ: -5.66, -1.12); р=0,01.

Помимо этих работ, 2 исследования не были включены в мета-анализ: статья Медведева с соавт. [21] так как не указано среднеквадратичное отклонение, и статья Франка с соавт. [26], где результат приведён в виде медианы и межквартильного интервала. Оба эти автора сообщают о статистически значимом превосходстве экспериментальном группы (получавшей Аденопросин).
IPSS
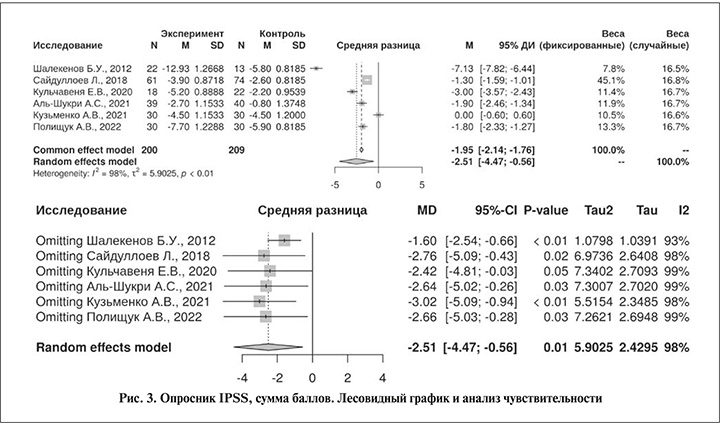
В мета-анализ вошли все шесть исследований [20, 22, 25, 27, 28, 30], содержавших результаты анкетирования по шкале IPSS. Наблюдается достоверное и существенное улучшение в каждой из моделей (рис. 3): -2,51 (95%ДИ: -4.47, -0.56); р=0.01. Гетерогенность была высокой (I2=98%). Несмотря на некоторое преобладание веса работы Сайдуллоева и соавт. [28], анализ чувствительности не выявил исследований, исключение которых могло бы сделать результат недостоверным. Также статистически достоверные различия в пользу Аденопросина получены в работе Медведева с соавт. [21], однако, они не включены в мета-анализ из-за отсутствия данных о среднеквадратичном отклонении исходной величины.
QoL, балл
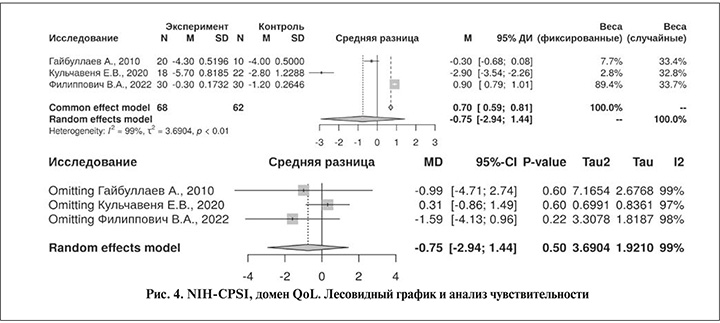
Оценка качества жизни проводилась по соответствующим доменам опросника NIH-CPSI (3 исследования [14, 25, 29]), результаты мета-анализа приведены на рис. 4. Статистически достоверных изменений не выявлено, разница в изменении показателя между группами составила -0.75 (95%ДИ: -2.94, 1.44); р=0. Интересно, что среди статей в мета-анализе наблюдали: в работе Е. В. Кульчавени и соавт. [25] в экспериментальной группе балл по домену QoL снизился достоверно больше, чем в группе контроля (то есть качество жизни улучшилось более значительно); в работе В. А. Филипповича и соавт. [29] – у пациентов основной группы показатели IPSS и качества жизни (QOL) выглядели предпочтительнее. Особенно обращает на себя внимание исследование А. В. Кузьменко с соавт. 2022 г. [15], в котором QоL значительно улучшились и по сравнению с группой контроля не ухудшалось в течение 12 мес. наблюдения.
МИЭФ-5
Результаты заполнения опросника МИЭФ-5 приведены лишь в двух работах [23, 27], рис. 5. Примечательна высокая статистическая однородность результатов, I2=0. Оба исследования показали увеличение этого показателя, 2,68 (95%ДИ: 2.08; 3.28), p<0,01.

Qmax, мл/с
Данные о Qmax были представлены в пяти исследованиях [20, 22, 25, 27, 30], лесовидный график представлен на рис. 6. Прирост скорости мочеиспускания оказался более значительным при добавлении Аденопросина, 2,34 (95%ДИ: 0.27, 4.41); р=0.04. Гетерогенность данных была высокой, I2=97%. Примечательны результаты исследования Е. В. Кульчавени и соавт. [25], где прирост максимальной объемной скорости потока мочи в экспериментальной группе был выше на 6,4 (95%ДИ: 5.56; 7.24) мл/с.

Концентрация лейкоцитов в секрете простаты
Данные о количестве лейкоцитов в секрете простаты были представлены в четырех исследованиях [14, 22, 25, 30]. И здесь рассматривать результаты нельзя в отрыве от исходных абсолютных значений. Так, в работе Б. У. Шалекенова и соавт. [30] исходная концентрация лейкоцитов была повышена незначительно. Авторы комментируют это включением пациентов с длительно- и вялотекущим абактериальным простатитом. Напротив, Е. В. Кульчавеня и соавт. [25] включили пациентов в существенным превышением концентрации лейкоцитов (в экспериментальной группе 32,3±5,7 в п./зр., в контрольной 28,6±6,9 в п./зр.) и получили более существенное снижение этого показателя по завершении лечения в группе Аденопросина, -7,2 (95%ДИ:-10.6; -3.8), по сравнению с контрольной группой.
Соответственно, данные в мета-анализе оказались гетерогенными, I2=85%, а средние изменения – незначимыми: -1,46 (95%ДИ: -4.63, 1.71); р=0,37 (рис. 7). Также данные о концентрации лейкоцитов приведена в работе Медведева с соавт. [21], однако, из-за отсутствия данных о среднеквадратичном отклонении исходного значения, они не были включены в мета-анализ. Автор сообщает о существенном снижении концентрации лейкоцитов в обеих группах, при этом в группе Аденопросина изменений были достоверно более значимыми.

Объем остаточной мочи
Данные о количестве остаточной мочи были представлены только в двух исследованиях [20, 22], рис. 8. Результаты отличались высокой статистической однородностью, I2=0. Оба исследования не обнаружили достоверных преимуществ той или иной группы по данному показателю (так как исходные объемы остаточной мочи были небольшими – до 100 мл), -1,3 (95%ДИ: -4.84, 2.24); р=0,47. В работе А. С., Аль-Шукри и соавт. [20] отмечено снижение объема остаточной мочи у пациентов 1-й и 2-й групп соответственно на 7,1 и 4,2 %. В исследовании А. В. Кузьменко и соавт. [22] объём остаточной мочи в обеих группах снизился примерно вдвое. Следует отметить, что в последнем случае терапия была более интенсивной (Тамсулозин+Левофлоксацин+Аденопросин).

V предстательной железы
Данные об объеме предстательной железы извлечены из трех исследований [20, 22, 30] рис. 9. Полученные данные о различиях гомогенны, I2=0%, и разницы в изменении между группами не отмечено, -0,11 (95%ДИ: -0.49, 0.27); р=0,56. Более того, в 2 из 3 этих работ не наблюдалось изменений в объеме простаты. Полученные результаты обусловлены тем, что в исследовании Б. У. Шалекенова с соавт. [30] объём простаты у пациентов до лечения в их выборке был близок к норме. А в работе А. В. Кузьменко с соавт. [22] при исходном среднем объёме простаты 60.7 см3 в группе Аденопросина объём уменьшился на 9 см3.

Также данные о динамике объема простаты приведены в исследовании А. В. Полищука и соавт. [27], однако оценка проведена спустя 90 дней от начала терапии, что не позволило включить работу в мета-анализ. Авторы сообщают о достоверном уменьшении объема простаты в экспериментальной группе (Аденопросин+ тамсулозин, исходный объем – 42,6±2,5 см3, по окончании терапии – 33,5±3,1 см3), в то время как в группе сравнения (только тамсулозин) существенных изменений не отмечено.
Воронковидные графики, отражающие публикационное смещение, для всех вышеперечисленных показателей приведены в дополнительных материалах к статье. Наличие публикационного смещения можно заметить для показателей качества жизни, однако с учетом небольшого количества статей с этим параметром говорить о значимости данной находки затруднительно. По остальным показателям графики в достаточной степени симметричны.
Обсуждение. В данном систематическом обзоре и мета-анализе мы оценили различные показатели у больных хроническим простатитом, в том числе в сочетании с ДГПЖ, на фоне терапии Аденопросином. Сравнение проводилось со стандартной терапией. Среди субъективных показателей наиболее существенное и единообразное преимущество экспериментальной группы отмечено в улучшении домена «боль», а также общего балла по опроснику NIH-CPSI. Клинически и статистически значимые положительные сдвиги от добавления Аденопросина видны и по опроснику IPSS. Следует отметить, что это не отразилось на опросниках качества жизни, возможно, вследствие их меньшей чувствительности. Качество жизни – более многофакторный показатель, чем опросники качества мочеиспускания, помимо СНМП на него влияют побочные эффекты проводимой терапии, а также психологические факторы [31]. Терапия Аденопросином также дала значимые улучшения по опроснику МИЭФ-5. Среди объективных показателей достоверные положительные изменения зарегистрированы относительно Qmax. Объем предстательной железы и остаточной мочи в обеих группах не изменился.
Говоря о возможных областях применения Аденопросин, хотелось бы также обратиться к ряду исследований, не вошедших в данный обзор. Х. С. Ибишев и соавт. выбрали особенно сложную категорию больных – с хроническим рецидивирующим бактериальным простатитом и множественной резистентностью микрофлоры к антибиотикам [32]. Исследование не было включено в наш анализ по причине отсутствия группы сравнения: все пациенты получали Аденопросин, проведен лишь анализ подгрупп в зависимости от длительности терапии. Важно, что Аденопросин был назначен в качестве монотерапии (в отличие от исследований в нашей выборке, где он добавлялся к стандартной терапии). Авторы отметили улучшение как субъективных (опросники NIH-CPSI и IPSS), так и объективных (показатели микроскопии секрета простаты и даже концентрация бактерий в нем) параметров, причем применение Аденопросина в течение 3 мес. позволяло достигать лучшего и более стойкого результата, чем в течение 1 мес. А. И. Неймарк и соавт. также назначали Аденопросин в качестве монотерапии, но больным хроническим абактериальным простатитом; в исследовании не было группы сравнения.
В дополнение к стандартным показателям они оценили качество эякулята. На выборке из 73 пациентов отмечено небольшое увеличение объема эякулята (+0,5 мл) и концентрации сперматозоидов (+8,1 млн/мл), а также увеличение доли активно-подвижных сперматозоидов и снижение доли патологических форм практически в 2 раза [33]. Ghicavii и соавт. кратко представили свои данные на ежегодном конгрессе SIU (Société Internationale d'Urologie) [34]. Интересно, что авторы проводили терапию Аденопросином пациентам с гиперплазией простаты, без указания на сопутствовавший хронический простатит. Они сообщили об улучшении со стороны СНМП, уменьшении объема остаточной мочи и увеличении скорости мочеиспускания. Таким образом, эти сведения приводят нас к заключению, что применение Аденопросина оправданно в отношении самых разных категорий пациентов, а его эффекты носят разносторонний и комплексный характер. На изучение подобных аспектов и стоит направлять будущие работы.
Большинство авторов сходятся во мнении, что в основе механизма действия препарата лежат два эффекта. Противовоспалительный реализуется посредством ингибирования цикла арахидоновой кислоты и подавления синтеза А2-фосфолипазы. Это уменьшает синтез простагландинов и лейкотриенов (ИЛ-6, ИЛ-8 и других). Антиоксидантный эффект обусловлен ингибированием пероксидации липидов [14, 26]. В свою очередь это несет вазопротективное и иммуномодулирующее действия, а на макроуровне проявляется уменьшением отека и тонуса ткани простаты. Данные патогенетические эффекты благотворно сказываются на течении заболевания. Особенность любых препаратов природного происхождения – это сложный состав и, соответственно, множественные механизмы действия и эффекты; некоторые из них еще предстоит проверить в будущих работах.
Ограничения. Наиболее достоверные данные могут быть получены из рандомизированных исследований с плацебо-контролем. К сожалению, мы не идентифицировали таких исследований для Аденопросина, поэтому в данный мета-анализ вошли работы по сравнению исследуемого препарата в комбинации со стандартной терапией против только стандартной терапии. Это может сказаться на точности полученных данных, так как принятые в разных учреждениях схемы терапии могут различаться, однако нужно понимать, что и плацебо-контроль не идеален [35]. Сравнительно большое количество пациентов в исследованиях и исследований в нашем обзоре позволяют рассчитывать, что данное влияние может быть нивелировано. Другое ограничение – разнородность представленных в статьях данных, что не позволило включить все их в мета-анализ. Во включенных статьях также присутствовала неоднородность отдельных показателей до начала лечения (например, концентрации лейкоцитов), тем не менее эти особенности позволяют нам оценивать эффекты от препарата у разно-образных категорий пациентов, что соответствует реальной клинической практике.
Заключение. Добавление Аденопросина к стандартной схеме терапии больных хроническим простатитом, в том числе в сочетании с ДГПЖ, достоверно улучшает симптомы нижних мочевыводящих путей и эректильную функцию (на основании опросников NIH-CPSI, IPSS, МИЭФ-5 и урофлоуметрии). Существенных различий с группой стандартной терапии по опросникам QoL, по объему предстательной железы и остаточной мочи, снижению количества лейкоцитов в секрете простаты не отмечено, однако данные по этим оценочным параметрам выглядели предпочтительнее в группе Аденопросина. Отдельные авторы сообщают об улучшении показателей эякулята на фоне приема Аденопросина, что требует дальнейшего изучения.



