Введение. Хронический простатит и синдром хронической тазовой боли (СХТБ) можно отнести к социально значимым заболеваниям ввиду широкой распространенности и существенного влияния на качество жизни пациентов. Они отличаются полиморфностью клинической картины: помимо боли могут приводить к возникновению симптомов нижних мочевыводящих путей (СНП) [1], ухудшению эректильной функции [2], а также провоцировать ряд симптомов, вообще не связанных с мочеполовой системой, – депрессию, беспокойство, бессонницу и утомляемость [3, 4]. Разнообразие путей патогенеза и гетерогенность клинических проявлений обусловливают подходы к лечению данных нозологий. Предложено множество вариантов терапии хронического простатита и СХТБ, тем не менее единый алгоритм лечения отсутствует [5]. Опциями лечения могут быть α1-адреноблокаторы, нестероидные противовоспалительные препараты, ингибиторы 5-α редуктазы, антибиотики, модуляторы невропатической боли (ингибиторы обратного захвата серотонина, противоэпилептические блокаторы кальциевых каналов) и другие препараты [6, 7]. Чаще всего применяется комбинация нескольких препаратов.
Важную роль в комплексной терапии простатита и СХТБ играют препараты природного происхождения. Так, существуют данные об успешном применении экстракта Serenoa repens, ранее используемого только при гиперплазии простаты [8], препарата на основе личинок насекомых Lymantria dispar [9] и ряда других препаратов. Достаточно большая доказательная база как доклинических [10], так и клинических исследований [11] говорит об эффективности применения биорегуляторных пептидов в лечении простатита и СХТБ. Сравнительно новым препаратом данной группы является Простатекс, действующее вещество которого – экстракт простаты крупного рогатого скота.
Цель данной работы: оценить в рамках постмаркетингового анализа (исследования 4-й фазы) влияние приема препарата Простатекс на показатели интенсивности синдрома хронической тазовой боли, копулятивную функцию пациентов и результаты микроскопии секрета предстательной железы и общего анализа мочи.
Материалы и методы. В данном проспективном мультицентровом обсервационном исследовании была сформирована когорта пациентов в возрасте 25–65 лет с диагностированным хроническим абактериальным простатитом, имеющих жалобы на наличие хронической тазовой боли.
В исследование включены 1700 пациентов в возрасте от 25 до 65 лет (средний возраст – 47,2 года).
Критерием невключения в исследование являлось наличие гиперплазии простаты с объемом железы >35 см3, рака предстательной железы, стриктуры уретры, склероза шейки мочевого пузыря с выраженными признаками инфравезикальной обструкции (объем остаточной мочи в мочевом пузыре >50 мл по данным УЗИ), острого или хронического уретрита, обострения сопутствующих заболеваний (сахарный диабет, системные заболевания), роста бактериальной флоры в секрете предстательной железы.
Критериями исключения являлись отказ пациента продолжать участие в исследовании, несоблюдение процедур протокола исследования, обострение сопутствующих заболеваний (сахарный диабет, системные заболевания).
Включенные в исследование пациенты на протяжении 30 дней получали Простатекс по схеме 1 суппозиторий ректально 1 раз в день. Наблюдение проводилось в течение 30 дней. Перед началом приема препарата и по окончании 30-дневного курса пациенты заполняли опросники «Индекс симптомов хронического простатита» (NIH-CPSI) и опросник исследования копулятивной функции, выполнялись объективный осмотр, общий анализ мочи, микроскопия секрета простаты.
Первичной конечной точкой оценки эффективности препарата являлась оценка болезненности предстательной железы при пальцевом ректальном исследовании, степени выраженности боли при СХТБ, мониторинга баллов опросника NIH-CPSI, количества лейкоцитов в исследовании секрета предстательной железы до и после проведенного курса лечения.
Вторичной конечной точкой оценки эффективности препарата являлись изменения баллов опросника мужской копулятивной функции (МКФ), прозрачности, количества белка, эритроцитов, лейкоцитов, кристаллов, эпителия, бактерий в моче, а также количества секрета простаты, цвета, pH, эритроцитов, эпителиальных клеток, амилоидных телец, лецитиновых зерен, макрофагов, кристаллов Беттхера, сперматозоидов. Регистрировались нежелательные явления, возникшие на фоне применения Простатекса.
Статистическая обработка выполнялась в программе IBM IPSS Statistics. Для каждого оцениваемого параметра произведен подсчет среднего арифметического, медианы, средних квадратических отклонений. При сравнении параметров показателей до и после лечения уровень значимости различий оценивался с использованием критерия хи-квадрат Пирсона, критерия Вилкоксона.
Результаты. Первичные конечные точки. Болезненность предстательной железы при пальпации статистически значимо снижалась или полностью исчезала у подавляющего большинства пациентов к концу курса приема препарата. Так, частота встречаемости выраженной болезненности снизилась до 0,1% (1 пациент) с 26,9% (457 пациентов), умеренной болезненности – с 43,1% (733 пациента) до 2,6% (44 пациента), а отсутствие боли стали отмечать 60,6% (1030 пациентов) против 1,9% (32 пациента) на начало исследования. Показатель встречаемости слабой болезненности вырос с 19,2% (327 пациентов) до 27,9% (474 пациента) за счет перехода больных из групп умеренной и выраженной болезненности. У 8,5% включенных в исследование пациентов показатель болезненности указан не был (рис. 1).
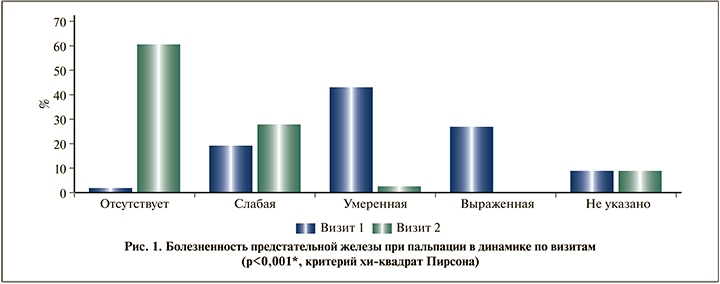
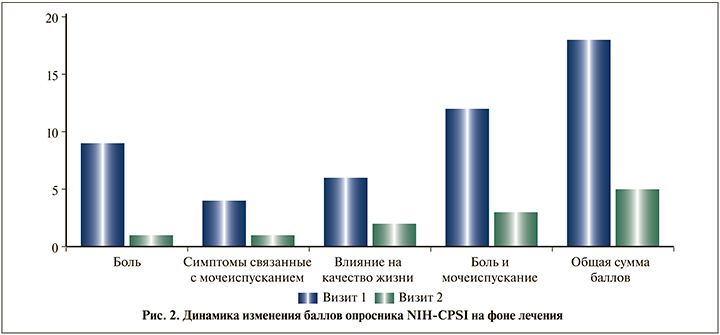
Степень выраженности симптомов хронического простатита после проведенного курса лечения была статистически значимо (p<0,001) ниже в каждой группе симптомов опросника NIH-CPSI. Отмечено снижение общей выраженности боли (2 балла против 9 до начала лечения), а также боли, связанной с мочеиспусканием (3 против 12), других симптомов, связанных с мочеиспусканием (1 балл против 4), влияния на качество жизни (2 балла против 6). Общая сумма баллов в среднем снижалась с 18 до 5 на фоне терапии Простатексом (рис. 2).
Выраженность боли на фоне лечения изменилась следующим образом: до 93,5% пациентов через 30 дней приема препарата охарактеризовали боль как незначительно выраженную, тогда как до начала лечения доля таких больных составляла лишь треть (37,5%). Боль средней степени выраженности отмечали 6,5% больных (50,8% – до начала лечения), сильно выраженную боль – 0,1% (11,7% – до лечения) (p<0,001).
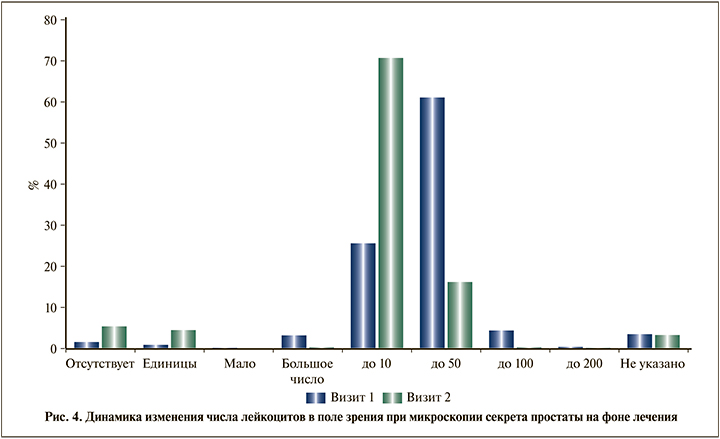
Касательно динамики изменения количества лейкоцитов при микроскопии секрета простаты на фоне лечения отмечалось снижение числа больных с показателями выше референсных значений. Так, число больных с показателем до 50 лейкоцитов в п/з изменилось с 1037 (61%) до 273 (16,1%), до 100 в п/з – с 73 (4,3%) до 4 (0,2%), до 200 в п/з – с 5 (0,3%) до 1 (0,1%), большое количество – с 52 (3,1%) до 4 (0,2%). При этом доля пациентов с нормальным количеством лейкоцитов в секрете простаты увеличилась: до 10 в п/з – с 434 (25,5%) до 1200 (70,6%), единичные – с 14 (0,8%) до 74 (4,4%), отсутствуют – с 25 (1,5%) до 90 (5,3%) (рис. 4).
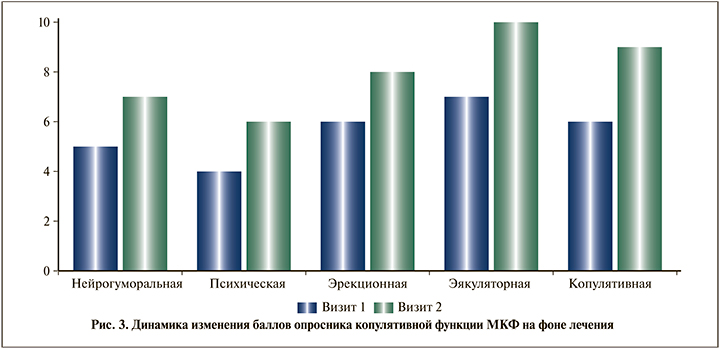
Вторичные конечные точки. Показатели опросника копулятивной функции МКФ выросли на фоне лечения во всех разделах: нейрогуморальном (7 против 5), психическом (4 против 6), эрекционном (6 против 8), эякуляторном (7 против 10), копулятивном (6 против 9) (p<0,001) (рис. 3).
Помимо изменения числа лейкоцитов при исследовании секрета простаты наблюдались повышение объема секрета за счет уменьшения числа пациентов со скудным количеством (с 3,6% (62) до 9 (0,5%) и ростом показателя 2–4 мл (с 3,6% [61] до 7,4% [125]), рост числа пациентов с белым цветом секрета простаты (с 26,9% [457] до 34,9% [593]), нормализация pH секрета за счет увеличения количества пациентов с pH 6,1–7,0 (c 16,5% [281] до 20,7% [352]), снижение количества эритроцитов (отсутствуют у 41,0% [697] до начала лечения, у 60,2% [1023] после курса лечения), снижение числа эпителиальных клеток (отсутствуют до лечения у 16,9% [288], после курса – у 25,9% [441]), амилоидных телец (отсутствуют до лечения у 49,3% [838], после – у 55,9 [950], небольшое количество до лечения – у 11,9% [203], 7,6% [51] – после), макрофагов (отсутствуют до лечения у 49,8% [846], после – у 59,8% [1017]), кристаллов Беттхера (до лечения отсутствуют у 57,2% [973], после – у 62,6% [1064]), сперматозоидов (до лечения отсутствуют у 59,1% [1005], после – у 66,2% [1125]), а также повышение количества лецитиновых зерен (большое количетво до лечения у 168 [9,9%[, поле – у 524 [30,8%[). В общем анализе мочи наблюдалось повышение прозрачности (увеличение числа пациентов с прозрачной мочой с 54,9% [934] до 61,4% [1043], снижение уровня белка (количество пациентов с отрицательным значением до лечения – 43,1% [733], после – 50,6% [861]), лейкоцитов (до лечения отсутствуют у 3,6% [62], после – 11,6% [197], до 3 в п/з – 25,8% [438] до лечения против 57,9% [985] после лечения), кристаллов (количество пациентов с отрицательным значением до лечения – 51,5% [875], после – 60,0% [1020]), эпителия (количество пациентов с отрицательным значением до лечения – 23,2%% [394], после – 30,2% [514]), бактерий (количество пациентов с отрицательным значением до лечения – 51,7% [879], после – 76,4% [1299], наибольшое количество до лечения – 17,6% [300], после – 3,2% [54]).
На фоне применения Простатекса не было зарегистрировано клинически значимых нежелательных явлений, потребовавших приостановки или отмены препарата, либо изменений проводимого лечения.
Обсуждение. Данное исследование, проведенное на большой и разнородной группе пациентов, указывает на положительные результаты применения препарата Простатекс как по субъективным показателям (уровень боли при пальпации предстательной железы, баллы по опросникам NIH-CPSI и МКФ), так и по объективным параметрам (показатели анализа секрета простаты и общего анализа мочи). Немаловажно, что при этом не было зарегистрировано значимых нежелательных явлений.
Полученные в ходе исследования результаты подтверждаются другими работами по изучению препаратов этой группы. А. В. Кузьменко и соавт. [11] показали, что добавление биорегуляторных пептидов к терапии α1-адреноблокаторами и фторхинолонами достоверно улучшает показатели опросников IPSS, QOL and NICH-CPSI и параметры секрета простаты. Дополнительно авторы выполняли урофлоуметрию и отметили, что в исследуемой группе максимальная скорость мочеиспускания оказалась на 1,4 мл/с выше, чем в контрольной. И. В. Кузьмин и соавт. приводят обзор литературы и 30-летний опыт применения данной группы препаратов, демонстрируя хорошие результаты как при гиперплазии простаты, так и при хроническом простатите [12]. Л. Е. Белый сообщает, что назначение данных препаратов оправданно также при патоспермии [13].
Детальный механизм действия биорегуляторных пептидов до сих пор не ясен. В обзоре на данную тему Ю. Л. Демидко и соавт. [14] описывают влияние препаратов на их основе на дифференцировку и пролиферацию клеток простаты, указывают на их противовоспалительные и иммуномодулирующие свойства. Т. Н. Саватеева-Любимова в экспериментальной работе на модели простатита у крыс [15] отметила не только органотропное действие регуляторных пептидов на простату, проявляющееся в уменьшении массы простаты, снижении уровня белка в моче, активности кислой фосфатазы, содержания церулоплазмина и С-реактивного белка, но и повышение уровня тестостерона в крови. Е. И. Карпов в дополнение к перечисленным эффектам указывает на повышение тонуса детрузора [16].
Дизайн проведенного исследования имеет ряд преимуществ и недостатков, на которых необходимо акцентировать внимание. Выборка отличается гетерогенностью по причине большой разницы в возрасте пациентов, различной предшествовавшей терапии и полиморфности клинической картины, присущей простатиту. Тем не менее по ключевым аспектам достигнуто единообразие: в исследование не включались пациенты с гиперплазией простаты, а также бактериальным простатитом (так как им может потребоваться дополнительная терапия антибиотиками). У всех пациентов в исследовании ранее имели место курсы терапии простатита или СХТБ, но их эффект не был достаточным, что и потребовало повторного обращения к врачу. В данном исследовании Простатекс применялся в качестве монотерапии, что позволяет изолированно оценить эффект Простатекса. Однако препараты, направленные на лечение простатита и СХТБ, часто обладают синергизмом, и именно применение комбинаций позволяет оценивать в полной мере их эффект. Таким образом, в дальнейшем при назначении Простатекса вместе со стандартной терапией следует ожидать еще и более существенных эффектов. В то время как предыдущие исследования были сосредоточены на оценке эффектов биорегуляторных пептидов у небольших групп пациентов по сравнению с группой контроля, то есть являлись клиническими исследованиями III фазы, задачей данной работы было оценить результат терапии Простатексом на большой и разнородной группе пациентов, представляющих реальную картину, с которой урологи сталкиваются в повседневной практике.
За неимением группы контроля и «ослепления» при интерпретации результатов необходимо учитывать плацебо-эффект. А. О. Морозов и соавт. в своем мета-анализе [17] количественно оценили его и показали, что эффект плацебо может оказывать существенное влияние на ряд субъективных показателей (в первую очередь балл по опроснику NIH-CPSI, а также по другим опросникам боли), но объективные показатели (урофлоуметрия, объем остаточной мочи) и даже балл по опроснику IPSS при СХТБ не были подвержены данному эффекту. К сожалению, в своей работе авторы не приводят сведений о влиянии эффекта плацебо на показатели секрета простаты, но трудно предположить физиологический механизм, по которому плацебо могло бы оказывать влияние на такие объективные параметры. Авторы сообщают, что среднее изменение общего балла по NIH-CPSI составило -4.2 (95% CI: -6.31, -2.09) из-за эффекта плацебо, в то время как в нашем исследовании среднее изменение общего балла составило 13, что не может быть объяснено одним лишь эффектом плацебо.
На фоне терапии Простатексом можно ожидать изменения других параметров, которые косвенно могут иметь отношение к хроническому простатиту и СХТБ, например показателей урофлоуметрии или ТРУЗИ. Однако это трудно осуществимо с учетом больших размеров выборки и не входило в задачи данного исследования, так как указанные исследования не являются первостепенными при этой нозологии.
Заключение. Использование препарата Простатекс в лечении пациентов с СХТБ снижает выраженность болевого синдрома и других симптомов хронического простатита, повышает копулятивную функцию и нормализует показатели микроскопии секрета предстательной железы и общего анализа мочи. С целью получения данных более высокого уровня доказательности необходимо проведение рандомизированных слепых плацебо-контролируемых исследований.



