Введение. Доброкачественная гиперплазия предстательной железы (ДГПЖ) является наиболее распространенным урологическим заболеванием среди мужчин пожилого и старческого возраста. На фоне повышения эффективности консервативного лечения симптомов нижних мочевыводящих путей при ДГПЖ сроки проведения оперативного лечения с момента начала заболевания существенно увеличились, что в сочетании с продолжающимся старением населения, накоплением интеркуррентных заболеваний привело к появлению массы пациентов старческого возраста с большими и огромными размерами предстательной железы [1–4]. При больших (80–100 см3), огромных (100–150 см3) и гигантских (свыше 150 см3) железах эффективность трансуретральной резекции (ТУР) простаты снижена в связи с большой продолжительностью операции, высоким риском развития осложнений (15–20%) и нерадикальностью вмешательства (50–70%), что требует выполнения повторных операций в течение 5–10 лет у 10–15% пациентов [5, 6]. Эндоскопическая энуклеация простаты, несмотря на рост популярности среди урологов, является технологичной операцией, требующей специального оборудования и характеризующейся сравнительно высокой частотой расстройств мочеиспускания в послеоперационном периоде [7, 8].
Целью исследования было проведение анализа предоперационных, интраоперационных, ближайших послеоперационных показателей и 12-месячных функциональных результатов эндоскопической энуклеации предстательной железы.
Материалы и методы. С января 2016 по май 2017 г. оперативное лечение по поводу ДГПЖ проведено 347 пациентам, у 179 из которых были выявлены большие, огромные и гигантские железы. Исследование было проспективным и одобрено локальным этическим комитетом. Из исследования были исключены 59 пациентов, которым были выполнены экстраперитонеоскопические аденомэктомии (22) и ТУРП (37).
Ста двадцати пациентам было проведено 63 биполярных электроэнуклеаций предстательной железы и 57 лазерных энуклеаций (28 гольмиевым лазером, 50 Вт, «AurigaXL», BostonScientific [США] и 29 тулиевым волоконным лазером, 60 Вт, «FiberlaseU1», ИРЭ-Полюс, Россия). Все операции выполнены в плановом порядке после стандартного комплексного предоперационного обследования (табл. 1, 2).

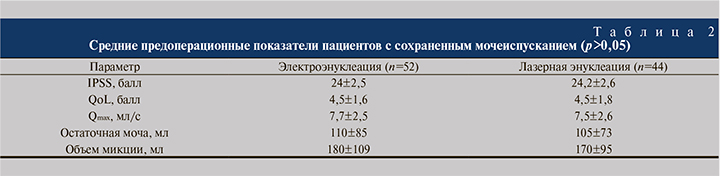
Для уточнения фенотипа ДГПЖ и длины апекса простаты помимо трансректального УЗИ использовали ретроцистоскопию, имея в виду, что расстояние выдвинутой петли резектоскопа до его кромки составляет 1,5 см.
Техника эндоскопической энуклеации предстательной железы. Все операции проводили в условиях специализированной эндоскопической операционной под спинальной анестезией. Для биполярной электроэнуклеации использовали резектоскопы фирм «Karl Storz» (n=32) и «Olympus» (n=31). Вмешательство начинали с создания дорсальной, по показаниям – вентральной) борозд и циркулярного рассечения слизистой в зоне апикальных тканей с помощью петли. Затем петлю меняли на специальный электрод-толкатель для энуклеации и выполняли отделение аденоматозных тканей от хирургической капсулы – в большей степени с помощью механической тракции. Двадцати трем больным операция выполнена с использованием трехдолевой методики, в 24 наблюдениях аденома удалена двумя долями, в 16 – единым блоком.
Лазерная энуклеация проведена 57 пациентам, из них 28 – с использованием 50 Вт гольмиевого лазера и 29 – 60 Вт тулиевого волоконного лазера FiberlaseU1. Для энуклеации применяли специализированные рабочие элементы компаний «Karl Storz» (48 операций) и«Richard Wolf» (19). Технические особенности лазерной энуклеации – раннее циркулярное рассечение слизистой в области апикальных тканей, преимущественное использование двухдолевой методики (33 операции), а также значительно меньшее использование механического отделения железы от простатической капсулы. Единым блоком аденома удалена 7 пациентам, трехдолевая методика использована в 17 наблюдениях. В 4 случаях морцелляцию тканей осуществляли вторым этапом спустя 2–3 дня после энуклеации из-за плохой эндоскопической видимости. Для удаления тканей из мочевого пузыря использовали морцелляторы Lumenis (48), Piranha (35) и Karl Storz (27). В одном случае из-за наличия крупных множественных камней мочевого пузыря энуклеированные ткани удалены при цистолитотомии.

Контрольные комплексные обследования проводили спустя 1, 3, 6 и 12 мес. после операции, во время каждого обследования проводилась оценка субъективных и объективных параметров (табл. 5–7). Статистическую обработку данных осуществляли с использованием программы Statistica 6,0. Достоверность межгрупповых различий определяли с помощью критерия Фишера, определялось отношение рисков. Статистически значимыми считали различия при p<0,05.
Результаты. Интраоперационные и ближайшие послеоперационные показатели, осложнения, результаты контрольных обследований приведены в табл. 3–7. Количество больных, прошедших контрольные обследования, указано в табл. 3–7, часть пациентов не смогли прибыть на контрольные обследования по различным немедицинским причинам, однако из исследования они не исключались, если смогли прийти на более поздние контрольные обследования.
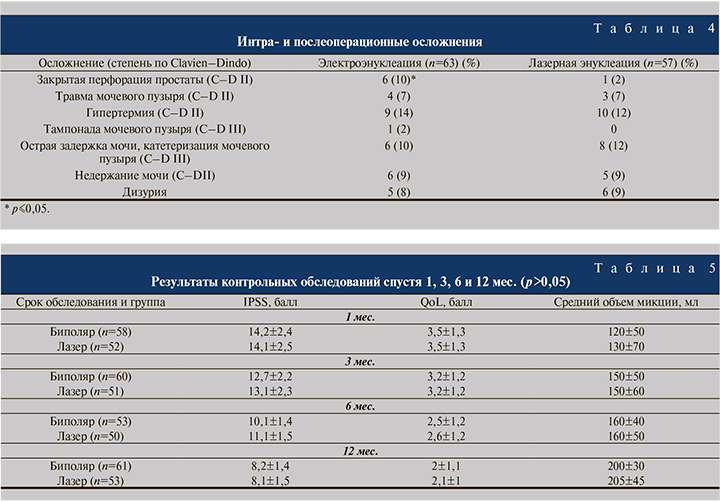
Наиболее серьезным осложнением после обоих видов вмешательств служит недержание мочи, которое в группах регистрировали с одинаковой частотой – 9% (см. табл. 4). Кроме того, еще примерно по 10% пациентов (5 и 6 в группе биполярной и лазерной энуклеации соответственно) испытывали послеоперационные симптомы нижних мочевыводящих путей – позывы на мочеиспускание, учащенное мочеиспускание малыми порциями и ночное мочеиспускание. В течение 1 мес. все пациенты (n=120) получали комбинированную терапию α-адреноблокаторами и м-холиноблокаторами. К концу 3-го месяца потребность в комбинированной терапии сохранялась у 82 (68%) прооперированных, спустя 6 мес. – у 32 (26%). По прошествии 6 мес. недержание мочи сохранялось только у 1 пациента. Спустя 11 мес. после операции ему была выполнена уретроцистоскопия, выявлен дефект смыкания наружного сфинктера с 10 до 2 ч условного циферблата, проведено подслизистое введение гиалуроновой кислоты с частично положительным эффектом в виде уменьшения количества прокладок с 3 до 1 в сутки. Важно отметить, что все 22 пациента с нарушением мочеиспускания, возникшим после энуклеации, имели короткое расстояние от верхушки семенного бугорка до наружного сфинктера (менее 1,5 см – расстояние выдвинутой петли резектоскопа: отношение рисков [ОР]=3,5) и внутрипузырную протрузию более 1 см (ОР=2,1).
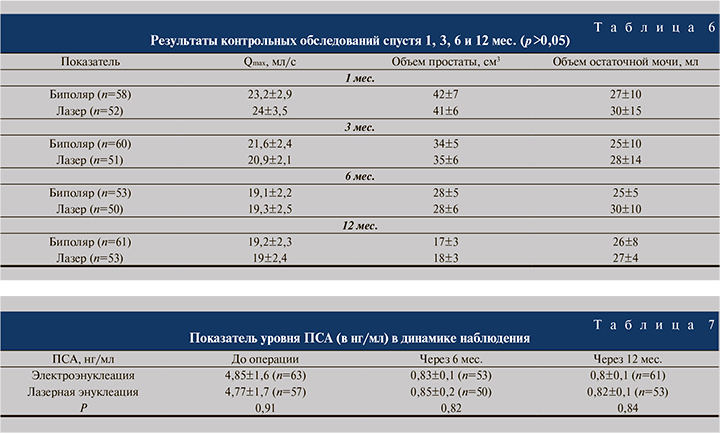
Обсуждение. Полученные в ходе настоящего исследования данные позволяют говорить о сопоставимой эффективности электроэнуклеации и лазерной энуклеации. По сравнению с предоперационными показателями статистически достоверно (р<0,05) доказана высокая эффективность обеих операций. С позиции частоты перфораций капсулы простаты использование лазерной энергии безопаснее, однако ни в одном случае использования биполярной энуклеации перфорация капсулы не влияла на ход операции – во всех наблюдениях отмечалась «закрытая» перфорация.
Особенностью данной работы является проведение фенотипирования роста предстательной железы, при больших и огромных размерах простаты оно отличается большим, чем у пациентов с малыми и средними размерами простаты, разнообразием. Выбор техники энуклеации, по нашему мнению, зависит от формы роста ДГПЖ. У пациентов с выраженной средней долей мы чаще использовали трехдолевую методику. Отдельные трудности представляет собой энуклеация при наличии развитой вентральной средней доли, что встречается реже, чем традиционная дорсальная форма роста. При использовании лазерной энергии, как правило, оперировали по двухдолевой методике. Единым блоком аденому удаляли чаще при использовании биполярной энергии.
На выполнение энуклеации в нашем исследовании требовалось больше времени, чем на биполярную трансуретральную резекцию при аналогичном объеме железы [2]. Сроки стояния уретрального катетера и продолжительность послеоперационного периода, наоборот, оказались короче, чем после ТУР предстательной железы большого объема, и соответствуют стандартным показателям послеоперационного периода после ТУР предстательной железы малого и средних объемов [1,2].
Полученная в настоящем исследовании частота геморрагических осложнений (см. табл. 4) свидетельствует об относительной безопасности операции по сравнению с ТУР предстательной железы [1, 2]. Ни одному пациенту не понадобилась гемотрансфузия. Лишь в одном случае после биполярной энуклеации на 1-е сутки после операции была выполнена цистоскопия и отмывание тампонады мочевого пузыря. После лазерной энуклеации подобных осложнений не было.
Закрытая перфорация капсулы предстательной железы после биполярной электроэнуклеации возникла у шести пациентов, после лазерной энуклеации – лишь у одного. Данное отличие, по нашему мнению, связано с невысокой проникающей способностью лазерной энергии и меньшей механической составляющей лазерной энуклеации. Недержание мочи и дизурия, требующие комбинированной медикаментозной терапии, регистрировали с частотой 18% в каждой из групп, что является относительным недостатком данного вида операций. Анализ данных показал, что вероятность развития данных симптомов повышена у пациентов с коротким, менее 1,5 см, апикально-сфинктерным расстоянием и внутрипузырной протрузией более 1 см. Применение комбинированной терапии α-адреноблоктаторами и м-холиноблокаторами после операции позволяет не только избавить пациента от ургентности, но и увеличить средний объем микции с 120 до 200 мл, т.е. на 66% от объема микции после операции.
К возможным недостаткам данного исследования можно отнести его моноцентровой характер и отсутствие ослепления исследователей, с другой стороны, сочетание межгруппового сравнения субъективных и объективных параметров не позволили данным недостаткам повлиять на его объективность.
Заключение. Биполярная и лазерная энуклеации ДГПЖ больших размеров остаются высокотехнологичными операциями, требующими более длительного нахождения в операционной, не сопровождаются геморрагическими осложнениями, отличаются сравнительно неосложненным послеоперационным периодом и характеризуются повышенной вероятностью развития ирритативных симптомов нижних мочевых путей. К факторам риска их возникновения являются короткое апикально-сфинктерное расстояние и внутрипузырная протрузия. Применение комбинированной терапии α-адреноблокаторами и м-холиноблокаторами позволяет улучшить качество жизни пациентов.



