Введение. Главный вектор в развитии всех направлений современной хирургии – замещение стандартных открытых операций малоинвазивными эндовидеохирургическими. Последние десятилетия в практику детского уролога наряду с лапароскопическим активно внедряется пневмовезикоскопический доступ [1–12]. Изначально пневмовезикоскопия применялась преимущественно для коррекции пузырно-мочеточникового рефлюкса (ПМР) [1–12]. Эффективность применяемого доступа в устранении ПМР составляет 94–98% [3–5, 7, 12, 13]. В дальнейшем метод расширил границы своего применения и стал активно использоваться при других заболеваниях: при обструктивном мегауретере для реимплантации мочеточника [10,12-16], иссечении уретероцеле [3, 13, 17], удалении дивертикула мочевого пузыря [18–20], разрушения камня мочевого пузыря [2], для проведения пластики шейки мочевого пузыря при недержании мочи [21, 22] и т.д. Однако внутрипузырный доступ довольно редко используют при обструктивном мегауретере, особенно при значительном расширении мочеточника. Малое внутреннее пространство детрузора затрудняет моделирование мочеточника, для этого его выводят наружу через отверстие в пузыре и открыто выполняют этап обуживания мегауретера [12–16, 18] либо дополнительно используют лапароскопический доступ [23–25].
Цель исследования: повысить эффективнось реимплантации мочеточника при ПМР, обструктивном мегауретере и патологии мочевого пузыря путем использования пневмовезикоскопического доступа.
Материалы и методы. За период с октября 2014 по март 2020 г. прооперированы 52 ребенка в возрасте от 10 мес. до 15 лет (средний возраст – 2,5 года) с использованием пневмовезикоскопического доступа. Большинство составили мальчики – 37 человек. Обследование пациентов включило лабораторные исследования, УЗИ органов мочевыделительной системы, микционную цистоуретрографию, динамическую или статическую нефросцинтиграфию, уродинамическое исследование. По результатам наблюдения и обследования были отобраны пациенты с рецидивирующей инфекцией мочевыводящих путей, высокой (3–5-й) степенью ПМР, прогрессированием уретерогидронефроза и снижением функции почек, что послужило показанием к хирургическому лечению.
Транстригональная реимплантация мочеточника с антирефлюксной защитой по методике Коэн выполнена на 58 мочеточниках (у 6 пациентов с двух сторон; см. таблицу).

Реимплантация вместе с иссечением дивертикула мочевого пузыря проведена 3 (5,7 %) пациентам. Объем дивертикула варьировался от 30 до 80 мл. Неоимплантация мочеточника в сочетании с иссечением ранее рассеченного уретероцеле выполнена 3 (5,7 %) детям.
Хирургическая техника. Оперативное вмешательство во всех случаях проводили под эндотрахеальным наркозом в положении ребенка на спине с валиком под ягодицами и разведенными нижними конечностями. Операцию начинали с тугого заполнения мочевого пузыря физиологическим раствором. В пузырь вводили цистоскоп с 30-градусной оптикой, под визуальным контролем длинной круглой иглой накладывали лигатуры (см. рис. 1 В,С,D), фиксировавшие мочевой пузырь к передней брюшной стенке (см. рис. 1 H), первые две – на середине расстояния между пупком и лонным сочленением (см. рис. 1 A, G ).
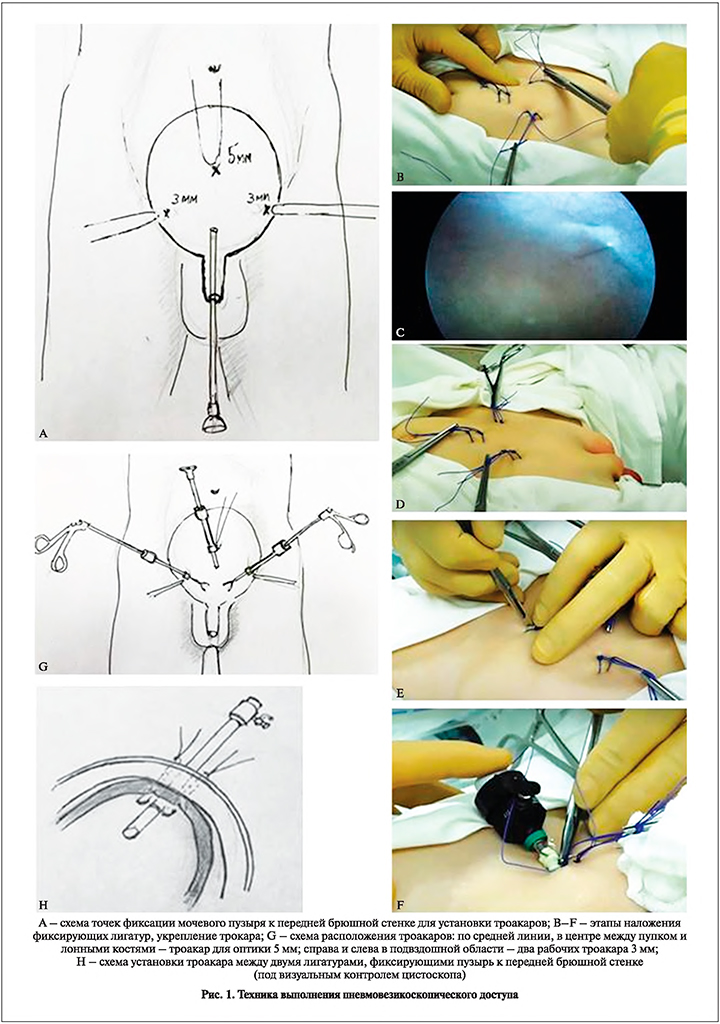
Использовали лигатуры 1 или 0 викрил на большой круглой игле. Троакар 5 мм (для оптики) вводили между двумя лигатурами и фиксировали к ним (см. рис. 1 E–H) для предотвращения смещения и выхода троакара из мочевого пузыря во время манипуляций, введения и извлечения оптики.
Другие лигатуры накладывали в подвздошных областях, где устанавливали 3-мм троакары для инструментов. Физиологический раствор удаляли из пузыря и вводили углекислый газ с максимальным давлением 10–12 мм рт.ст. Затем цистоскоп извлекали.
Пневмовезикоскопическая кросс-тригональная реимплантация по Коэну мочеточников выполнена у 52 детей, из них 6 билатерально, 37 (63,7 %) с левой стороны, 21 (36,2 %) с правой. В 9 случаях для внутрипузырного обуживания мочеточника была использована предложенная нами методика его фиксации к стенке мочевого пузыря (патент № 2724870 от 25.02.2020 «Способ эндовидеохирургического моделирования мочеточника при пневмовезикоскопической реимплантации у детей с мегауретером») [26].
Реимплантацию мочеточника детям с обструктивным мегауретером начинают с наложения фиксирующей лигатуры на область устья мочеточника без интубации устья катетером. Используют викрил 4/0. Лигатура помогает выделять мочеточник и служит ориентиром в случае ускользания мочеточника в паравезикальное пространство (при повторных операциях и коротком мочеточнике). Подтягивают лигатуру зажимом. и коагуляционным крючком выделяют устье окаймляющим разрезом. Мочеточник постепенно мобилизуют с последовательной коагуляцией сосудов на протяжении 6–7 см. Далее начинают моделирование (обуживание, плицирование мочеточника) в случае его значительного (более 25 мм) расширения. Для стабилизации (фиксации) мочеточника снаружи в область шейки мочевого пузыря вводят иглу с изгибом на конце (например, Тахуоки) (см. рис. 2 А, В, С), в просвете иглы и снаружи от нее оставляют лигатуру из монофиламентного материала (например, Prolene 3/0), в созданную петлю из лигатуры укладывают конец выделенного мочеточника (см. рис. 2 D, E, F). Лигатуру подтягивают и фиксируют мочеточник в максимально вытянутом из запузырного пространства положении (см. рис. 3 А, В).
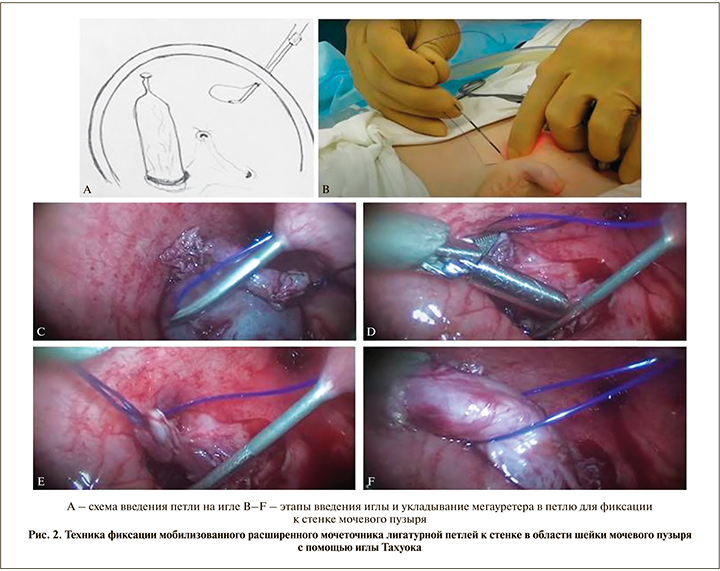
Далее непрерывным плицирующим (обуживающим) швом викрилом 4/0 выполняют моделирование мочеточника, уменьшая его диаметр в 2 раза на протяжении 5 см (см. рис. 3 С, D, E).
Затем на мочеточник, максимально выведенный из паравезикального пространства в мочевой пузырь, накладывают фиксирующий шов со стенкой мочевого пузыря, чтобы предотвратить возвращение мочеточника в запузырное пространство. Далее формируют подслизистый тоннель длиной 4–5 см в горизонтальном направлении над контралатеральным устьем (см. рис. 4 А). Выделенный мочеточник проводят в подслизистом тоннеле (см. рис. 4 В). Следующим этапом выполняют резекцию устья мочеточника, удаляя диспластичные ткани суженного сегмента. Мочеточник дополнительно фиксируют узловым швом (викрил 4/0) к стенке мочевого пузыря в области формирования нового устья. Слизистую мочеточника и мочевого пузыря соединяют непрерывным швом (викрил 5/0) (см. рис. 4 С).
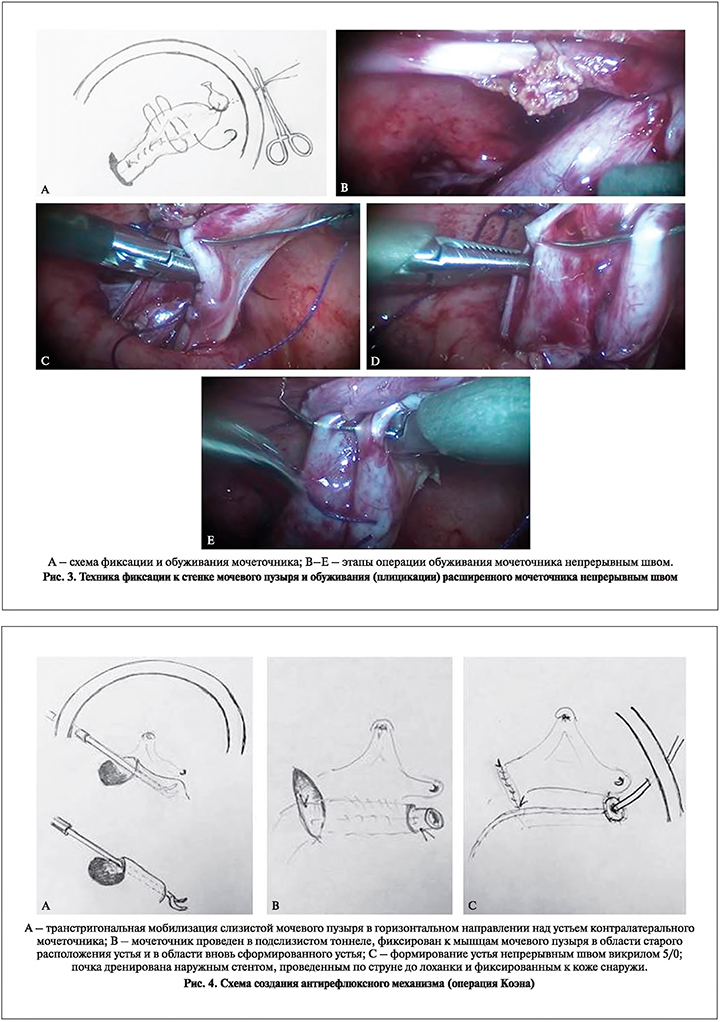
Мочеточник и почку дренируют наружным J-стентом, который устанавливают по струне, используя пункционную иглу, подведенную к устью, введенную в мочевой пузырь через дополнительный прокол. Рану мочевого пузыря в области выделения устья ушивают узловым швом 4/0 викрил. Слизистую мочевого пузыря соединяют непрерывным швом викрил 5/0. Операцию заканчивают установкой уретрального катетера и извлечением троакаров. Накладывают давящую повязку на мочевой пузырь и стягивающие пластырные повязки на область разрезов. В связи с необходимостью разгрузки мочевого пузыря уретральный катетер удаляют на 3–4-й день. Детей выписывают на 5-е сутки.
В случае удаления дивертикула мочевого пузыря выполняли поиск устья мочеточника в дивертикуле, выделяли мочеточник окаймляющим разрезом на протяжении 5–6 см. Рассекали слизистую мочевого пузыря по краю отверстия дивертикула, затем ткань дивертикула выводили в просвет пузыря, брали верхушку выпячивания на держалку (викрил 3/0), введенную в мочевой пузырь снаружи через прокол стенки. Далее иссекали стенки дивертикула, сохраняя целостность мочеточника. Реимплантацию выполняли с созданием подслизистого туннеля. Отверстие дивертикула ушивали двумя рядами узловых рассасывающихся швов на мышцы мочевого пузыря. Дивертикул из пузыря удаляли частями, чтобы не травмировать уретру и не расширять отверстия троакаров в мочевом пузыре. Больные дивертикулом требовали длительного медикаментозного лечения нейрогенных дисфункций мочевого пузыря и нарушений опорожнения детрузора, чаще связанных со спазмом наружного сфинктера.
Контрольное обследование (анализ мочи, УЗИ) проводили через 1, 3, 6, мес. после операции. Микционную цистоуретрографию выполняли через 6 мес.
Результаты. Среднее время операции составило 142 (83–235) мин. Причины увеличения продолжительности операции: двустороннее вмешательство на мочеточниках; потребность в обуживании мегауретера; трудности выделения мочеточника из-за наличия объемообразующего вещества (после 2–3 инъекций) для коррекции ПМР; сочетание реимплантации с иссечением дивертикула мочевого пузыря или уретероцеле.
Конверсия потребовалась одному ребенку из-за потери визуализирующего троакара в первый год внедрения пневмовезикоскопического доступа, вмешательство было завершено открытой реимплантацией мочеточника.
Осложнений, связанных с повторной обструкцией уретеровезикального сегмента или с инфекцией мочевыводящих путей в послеоперационным периоде, мы не наблюдали, поскольку все больные выписывались с наружным мочеточниковым катетером, который удалили через 1 мес. после вмешательства. Эпизодов длительной гематурии, которая часто сопровождает открытые реимплантации мочеточника, не было. Уретральный кататер извлекали на 3–4-е сутки. Число эпизодов послеоперационного обезболивания больных с 9–12 раз (за весь послеоперационный период) при открытых операциях сократилость до 4–6 раз при использовании пневмовезикоскопического доступа. Продолжительность пребывания в клинике составила 5–7 дней, в среднем 5,41 дня, вместо 7–9 дней (в среднем 7,8 дня) при открытых вмешательствах.
Отдаленные результаты пневмовезикоскопической реимплантации мочеточников с внутрипузырным обуживанием (плицированием) или без такового оценивали по результатам УЗИ, которое проводилось через 1, 3, 6 и 12 мес. после операции. У всех больных отмечено уменьшение размеров чашечно-лоханочной системы и мочеточника. По данным микционной цистографии, рефлюкс был обнаружен у 3 (5,7%) из 52 пациентов (5,1% из 58 оперированных мочеточников): двух детей с ПМР, одного из них с ПМР после открытой реимплантации мочеточника по Политано–Леадбеттеру и коротким мочеточником, одного пациента с обструктивным мегауретером и обуживанием мочеточника. Во всех трех случаях была выполнена успешная эндоскопическая коррекция ПМР с введением объемообразующего вещества. В целом эффективность реиплантации мочеточника при лечении ПМР 3–5-й степеней составила 91%, эффективность лечения обструктивного мегауретера – 96%.
Обсуждение. В отличие от лапароскопической пиелопластики, реимплантация мочеточника лапароскопическим или пневмовезикоскопическим доступом не стала единодушно признанным стандартом лечения для большинства детских урологов. Пневмовезикоскопический доступ, несмотря на свои очевидные преимущества, остается высокотехнологичным, трудоемким и непростым в освоении, сложным по технике выполнеия из-за особенностей установки и фиксации троакаров. Метод имеет возрастные органичения из-за объема мочевого пузыря.
Везикоскопический доступ можно считать оптимальным при выполнении простых процедур: иссечении дивертикулов [18–20] и полипов мочевого пузыря [27], удалении конкрементов [2, 5]. Реимплантация мочеточника внутрипузырным доступом требует достаточного опыта лапароскопических операций и навыков работы в ограниченном пространстве мочевого пузыря [3, 5, 7, 13]. Доступ широко используют при реимплантации мочеточника в случае ПМР [1–13], реже – при рефлюксирующем мегауретере [3, 5] и еще реже при обструктивном мегауретере с значительной дилатацией мочеточника [5, 13, 18]. Причиной тому, вероятно, трудности выполнения везикоскопического обуживания мочеточника для достижения качественного антирефлюксного механизма. В соответствии с концепцией A.J. Paquin [27] для предупреждения возникновения ПМР соотношение длины подслизистого туннеля к диаметру реимплантированного мочеточника должно составлять 5:1. Традиционно диаметр мочеточника уменьшают пликацией: дорсальным (методика Starr) [28], боковым (Kalicinski) [29, 30] или продольным «ломпасным» иссечением части мочеточника (пластика по Hendren) [31, 32]. Известно, что продольная резекция расширенного мочеточника может нарушать его кровоснабжение и стать причиной обструкции [30, 32, 33]. Пликация мочеточника редко сопровождается рубцеванием устья, но характеризуется длительным периодом нарушения уродинамики и перистальтики в обуженном отделе мочеточника [33]. Однако ряд авторов ставят под сомнение необходимость обуживания мочеточника при мегауретере [33, 34], аргументируя быстром исчезновением признаков гидронефроза у пациентов без пликации, в то же время указывая, что число случаев ПМР у таких больных было выше.
Считаем обуживание мочеточника при обструктивном мегауретере более 25–30 мм целесообразным. В своей работе мы отдавали предпочтение методике Starr как наиболее щадящей, сопровождающейся меньшим число осложнений.
Заключение. Проведенное исследование подтвердило высокую эффективность пневмовезикоскопического доступа при лечении ПМР, обструктивного мегауретера, дивертикула моевого пузыря и уретероцеле. Несмотря на трудоемкость и определенную техническую сложность, пневмовезикоскопическая кросс-тригональная реимплантация мочеточников с внутрипузырным обуживанием мочеточника – эффективный и безопасный метод хирургического лечения. Послеоперационный период характеризуется малым числом осложнений, коротким сроком пребывания в клинике и отличным косметическим эффектом. Предложенный нами метод внутрипузырной фиксации мочеточника к стенке мочевого пузыря в области шейки для упрощения этапа обуживания позволяет сокращать время хирургического вмешательства.



