Введение. Доброкачественная гиперплазия предстательной железы (ДГПЖ) — одно из наиболее распространенных заболеваний мужской половины человечества старше 40 лет, пропорционально увеличивающееся с возрастом [1]. В Российской Федерации с 2000 г. заболеваемость ДГПЖ увеличилась в 1,5 раза, достигнув 12 млн мужчин [2]. В повседневной работе врача-уролога данная патология занимает второе место по распространенности (23%), уступая только инфекционным заболеваниям мочевыводящих путей (32%) [3, 4]. В течение последних 5 лет прирост заболеваний органов мочеполовой системы в России превысил таковую при патологии кровообращения, а ДГПЖ стала самым распространенным урологическим заболеванием мужчин пожилого и старческого возраста [5]. Около трети мужчин старше 50 лет с симптомами нижних мочевыводящих путей (СНМП) при ДГПЖ имеют выраженное ограничение социальной активности, тревожность, бессонницу и депрессию [6, 7]. Таким образом, это сочетание выходит в ряд первоочередных медико-социальных проблем мужчин данной возрастной категории.
Реальные результаты консервативной терапии СНМП/ ДГПЖ связаны с доказательством влияния альфа-блокаторов на нижние мочевыводящие пути. В 1976 г. М. Caine et al. первыми показали эффективность феноксибензамина в отношении лечения СНМП при ДГПЖ [8]. В 1984 г. удалось идентифицировать альфа1- и 2-адренорецепторы в предстательной железе человека и обосновать их участие в сокращении ее гладкой мускулатуры [9].
Согласно научным данным, все а1-адреноблокаторы независимо от степени селективности имеют сходную клиническую эффективность при использовании в адекватных дозах [10, 11]. Предпочтение в выборе того или иного а1-адреноблокатора сегодня определяется его безопасностью, которая в свою очередь, по устоявшемуся убеждению, зависит от аффинности к а1А-рецепторам [12, 13]. Наибольшую тревогу вызывают нежелательные явления, связанные с эффектом вазодилатации. В то же время обширный мета-анализ продемонстрировал сопоставимые шансы по развитию побочных эффектов со стороны сердечно-сосудистой системы для тамсулозина (1,42) и менее селективного алфузозина (1,66) [14]. По всей видимости, рецепторная уроселективность не является абсолютным предиктором эффективности и безопасности препарата. Тем более что степень рецепторного взаимодействия изучается in vitro на химерных клетках без учета функциональной уроселективности. В то время как по ключевому фармакологическому показателю «объем распределения» для алфузозина характерна аккумуляция в тканях и наибольшая тропность к ткани простаты. Индекс простатотропности алфузозина в 6 раз превышает таковой у тамсулозина: 543,6 против 89,8 соответственно [15]. Оценка простатотропности а1-блокаторов в серии работ продемонстрировала наиболее высокую диффузию алфузозина в ткань простаты [16, 17].
Не случайно в Руководстве Европейской ассоциации урологов в 2021 г. отмечено, что вазодилатирующие эффекты наиболее выражены с доксазозином и теразозином и реже с альфузозином и тамсулозином [18], поскольку систематический обзор последних 10 лет с использованием библиотек MEDLINE, EMBASE и Cochrane 2020 г. показал, что алфузозин проявляет селективную концентрацию в простате по сравнению с плазмой у пациентов с ДГПЖ [19].
Необходимость продолжительной, порой пожизненной, терапии больных гиперплазией предстательной железы делает актуальным изучение эффективных при длительном применении лекарственных форм и препаратов. Неопределенность, связанная с интеркуррентными заболеваниями, полифармацией, побочными эффектами лекарственных препаратов и низкой приверженностью пациентов к терапии, определяет необходимость дальнейшего поиска алгоритма по ведению коморбидных пациентов с гиперплазией предстательной железы.
Все вышесказанное стало основанием для изучения эффективности и профиля безопасности применения таблеток с пролонгированным высвобождением алфузозина (Алфупрост® МР) для пациентов с ДГПЖ в реальной клинической практике.
Материалы и методы. Целью нашего исследования было оценить эффективность и безопасность применения Алфупрост® МР 10 мг/сут. длительностью 12 мес. в реальной клинической практике. В исследование были включены 55 мужчин с ДГПЖ/СНМП в возрасте 55-80 лет с IPSS >8 и QоL >3 баллов, с уровнем общего простатического специфического антигена (ПСА) <4 нг/мл. Лечение и наблюдение за пациентами проводились на базе шести амбулаторных клиник Санкт-Петербурга с июня 2020 по сентябрь 2021 г.
Критерии невключения: прием каких-либо а1-адреноблокаторов менее чем за 1 мес. до включения в программу; любое состояние, препятствующее применению препарата в соответствии с противопоказаниями, мерами предосторожности и специальными предупреждениями, указанными в инструкции по медицинскому применению препарата Алфупрост® МР; психические заболевания или другие коморбидные состояния, которые могли бы помешать пациенту участвовать в программе; предшествовавшие операции на простате; острая задержка мочи в анамнезе; стриктура уретры; объем остаточной мочи более 150 мл; подозрение или установленные онкологические заболевания органов мочеполовой системы; почечная или печеночная недостаточность; камни мочевого пузыря, дивертикулы мочевого пузыря больших размеров, обусловленные инфравезикальной обструкцией гиперплазией простаты.
Обследование и назначения включенным в программу пациентам соответствовали реальной клинической практике и включали сбор анамнеза, анализы крови и мочи, пальцевое ректальное исследование, общий ПСА, трансректальное ультразвуковое исследование (ТРУЗИ) простаты (объем), ультразвуковое исследование (УЗИ) мочевого пузыря (объем остаточной мочи), урофлоуметрию (Q max), международные опросники суммарной оценки симптомов болезней предстательной железы, качества жизни пациентов с СНМП (IPSS-QоL) и мужской копулятивной функции (МКФ), регистрацию частоты сердечных сокращений (ЧСС) и систалического артериального (САД) и диастолического артериального давления (ДАД). Для оценки удовлетворенности лечением у пациентов и врачей была использована шкала Лайкерта. Наблюдательная часть программы включила 7 визитов (каждые 60±5 дней) и длилась 12 мес.
Статистическая обработка полученных данных проводилась с использованием стандартных пакетов программ Statistica (V7.0) и SPSS Statistics (V17.0). Для обработки данных были использованы методы описательной статистики. Проверка выборок на нормальность осуществлялась при помощи теста Колмогорова-Смирнова. При сравнении выборок применялись t-критерий Стьюдента, U-критерий Манна—Уитни и t-критерий Уилкоксона. Взаимосвязь параметров выявляли с помощью методов корреляционного анализа Пирсона и Спирмена. Анализ различия частот признаков в независимых группах производилась с использованием критерия Хи-квадрат с поправкой Йейтса. Также применялся расчет показателей относительного риска по Mantel-Haensel (ОР или RR). Отношение шансов (OR) и доверительного интервала (CI) производилось путем сопоставления частоты бинарного признака в группах с помощью четырехпольных таблиц.
Результаты. В возрастной популяции преобладали мужчины старше 60 лет (76,4%) и их средний возраст составлял 62,8±8,7 года. Средний показатель индекса массы тела (ИМТ) составлял 27,48 (±3.31) кг/м2, что характерно для избыточной массы тела. В структуре сопутствовавших заболеваний и вредных привычек, выявленных из анамнеза и протекающих в настоящее время, наиболее часто выявлялась длительно существующая ДГПЖ на фоне хронического простатита и артериальной гипертензии, сопровождавшаяся сниженной физической активностью и употреблением алкоголя (p<0,05) (рис. 1).
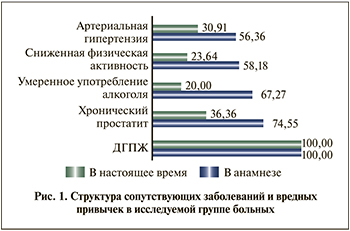
Уже после 2 мес. терапии Алфупрост® МР наблюдалось статистически достоверное (p<0,05) уменьшение числа пациентов, жалующихся на локальную боль до 11% и боль при мочеиспускании 16,7%, а также императивные позывы на 50% и затрудненное мочеиспускание на 30%. Последующее уменьшение симптоматики также достоверно (p<0,05) постепенно отмечалось от визита к визиту (рис. 2).
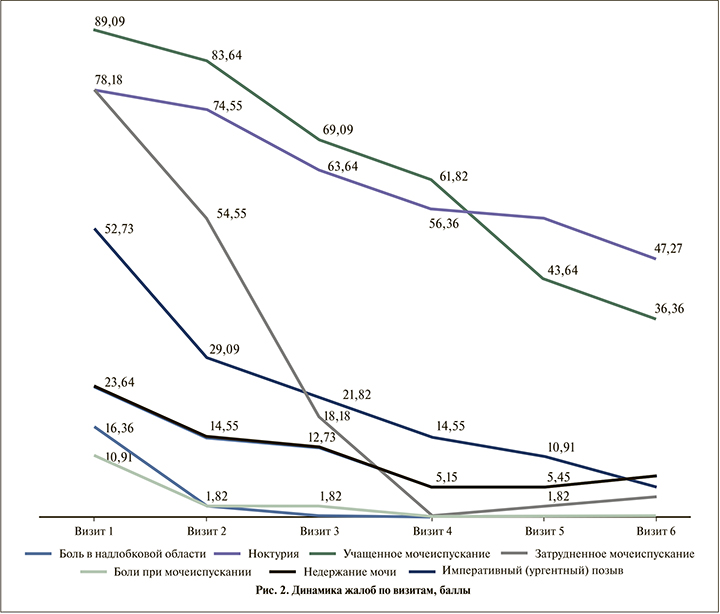
В результате к концу исследования суммарный балл IPSS достоверно (p<0,05) уменьшился (в 1,9 раза) и составил в среднем 9,98 балла после 12 мес. терапии препаратом Алфупрост® МР, а качество жизни QoL пациентов улучшилось на 2,5 балла (рис. 3, 4).
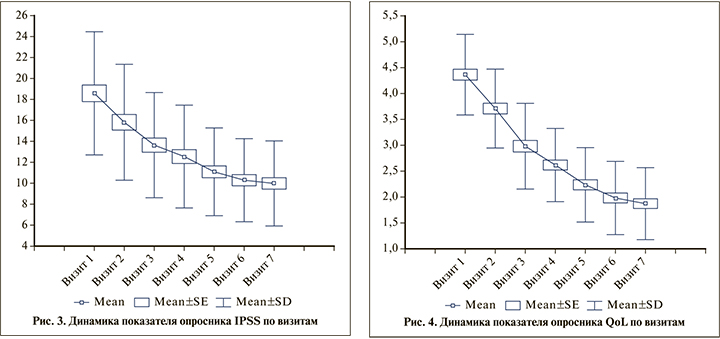
Через 12 мес. терапии средний показатель максимальной скорости потока мочи (Qmax, мл/с) достоверно (p<0,05) увеличился в 1,4 раза, достигнув 17,4 мл/с (рис. 5), а объем остаточной мочи достоверно (p<0,05) уменьшился до 12,5 мл (в 3,8 раза).
Интересные данные получены в отношении объема предстательной железы, который стал достоверно (p<0,05) уменьшаться уже через 2 мес. терапии, а через 12 мес. терапии снизился на 4,3% (рис. 6). К последнему визиту также наблюдалось уменьшение на 25,4% доли пациентов с изначальным уровнем общ. ПСА 2,5—4,0 нг/мл до значений менее 2,5 нг/мл, количество которых составило 70,9% через 12 мес. терапии (рис. 7).
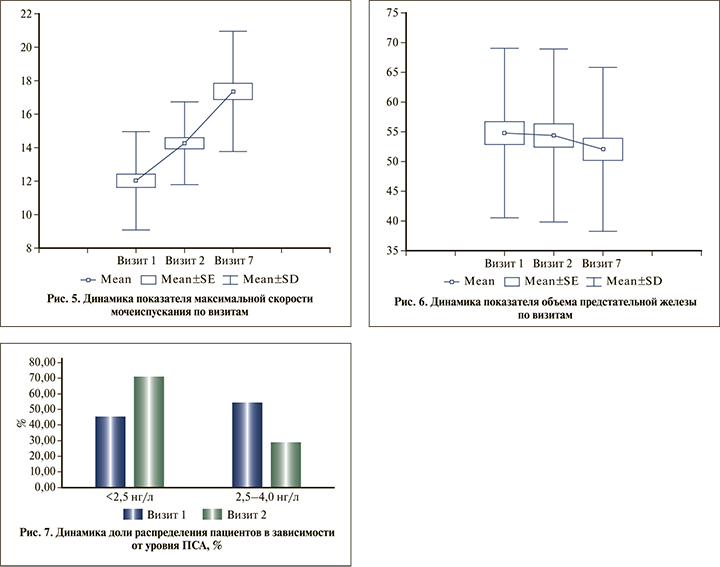
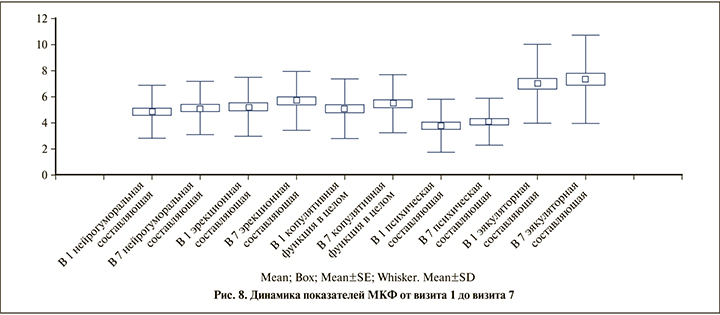
Изучение влияния проводимой терапии на мужскую копулятивную функцию продемонстрировало достоверное (p<0,05) улучшение всех ее составляющих (рис. 8): нейрогуморальной — ко 2-му визиту без дальнейших изменений до 7-го визита, психической — с 5-го визита по 7-й, и эректильной — с 4-го визита по 7-й. В течение 10 мес. не было существенных изменений эякуляторной составляющей. Незначительное, но достоверное улучшение на последнем, 7-м, визите по сравнению 6-м (p<0,05). По сравнению с 1-м визитом достоверное улучшение копулятивной функции на 2-м и медленное улучшение к 7-му визиту (p<0,05). В целом достоверное улучшение показателя копулятивной функции наступило на 2-м визите (через 2 мес.). С 2-го по 5-й визит в течение 3 мес. наблюдалось плато и с 5-го (через 10 мес.) по 7-й визит снова достоверное улучшение (p<0,05). По сравнению с первым визитом эректильная функция достоверно (p<0,05) улучшилась сразу (уже на 2-м визите) и продолжала постепенно усиливаться (p<0,05) к 12-му месяцу терапии препаратом Алфупрост® МР.
Нами также было изучено влияние терапии препаратом Алфупрост® МР на гемодинамические показатели пациентов в течение всего периода наблюдения. Гемодинамические показатели на протяжении 12 мес. наблюдения оставались стабильными. Хотя на 4-м и 6-м визитах по сравнению с визитом 1 отмечалось урежение ЧСС на 1,5 удара в минуту, а также снижение в течение 12 мес. систолического и диастолического артериального давления: менее чем на 2 мм рт.ст. — эти колебания были клинически незначимыми.
При исследовании приверженности к лечению с использованием шкалы Лайкерта пациенты уже через 2 мес. терапии отметили удовлетворенность проводимым лечением, а исследователи отметили удовлетворенность от результатов назначенной ими терапии к 5-му визиту. Ни один пациент не выбыл из исследования.
Обсуждение. Альфа1-блокаторы остаются наиболее популярным препаратом для лечения СНМП/ДГПЖ: 48-62% врачей во всем мире предпочитают назначать монотерапию альфа-блокаторами в начале лечения пациентов с СНМП при ДГПЖ, среди урологов России они также остаются на лидирующем месте (63%) [20]. Популярности альфа-блокаторов способствует быстрое улучшение (на 35-55%) субъективных и объективных показателей мочеиспускания. Уродинамические исследования, проведенные на пациентах, принимавших альфа-блокаторы, показывают снижение уретрального сопротивления и увеличение максимальной скорости потока мочи в пределах 1-3,5 мл/с, уменьшение количества остаточной мочи на 50%, снижение микционного давления на 1/3 [21].
Полученные нами данные соответствуют представленным в литературе. Суммарный балл IPSS через 12 мес. терапии улучшился на 8,6 балла (в 1,9 раза), средний показатель максимальной скорости мочеиспускания увеличился на 5,3 мл/с (в 1,4 раза), объем остаточной мочи уменьшился на 25,7 мл (в 3,8 раза), что, согласно результатам заполнения опросника QoL, позволило улучшить качество жизни пациентов в среднем на 2,49 балла (в 2,3 раза).
Довольно быстро, уже со 2-го визита, отмечена тенденция к постепенному незначительному уменьшению размеров простаты и увеличению доли пациентов со значением общ. ПСА менее 2,5 нг/мл. Согласно литературным данным, полученные результаты в краткосрочном периоде можно объяснить снижением уретрального сопротивления и исчезновением интрапростатического рефлюкса, уменьшением отека простаты и явлений простатита [22, 23], который практически всегда сопутствует ДГПЖ. Кроме того, в исследованиях зарубежных коллег установлено, что альфа-адренобокаторы способны индуцировать апоптоз гладкомышечных клеток предстательной железы и улучшать СНМП при ДГПЖ в долгосрочном периоде [24, 25].
Наличие побочных эффектов, связанных с адренорецепторной вазодилатацией (возможная тошнота, гипотензия, усталость, ретроградная эякуляция, заложенность носа), может ограничивать применение альфа-адреноблокаторов в клинической практике [26]. Системный сосудистый эффект альфа-блокаторов подтвержден в крупном исследовании ALLHAT, которое подтолкнуло к дальнейшему поиску альфа-адреноблокаторов для лечения СНМП при ДГПЖ с минимальным воздействием на сердечно-сосудистую систему, особенно у пожилых пациентов [27].
На протяжении всего периода наблюдения за пациентами, включенными в наше исследование, не было зарегистрировано каких-либо нежелательных реакций в отношении показателей гемодинамики, что подтверждает высокий профиль безопасности применения препарата в клинической практике. Данные проведенного нами наблюдения продемонстрировали, что на протяжении 12 мес. терапии у пациентов были зафиксированы клинически незначимые колебания САД и ДАД (на 1-2 мм рт.ст.); изменения ЧСС на протяжении 12 мес. терапии Алфупрост® МР были также клинически незначимыми и в среднем составили не более 1,5 ударов в минуту.
Подобные результаты могут быть связаны с особенностями фармакокинетического профиля препарата Алфупрост® МР, лекарственная форма которого производится по запатентованной технологии модифицированного высвобождения. Таблетка матричного типа препарата Алфупрост® МР состоит из гидрофильного матрикса, куда погружено действующее вещество алфузозин. Гипромеллоза, входящая в состав таблетки, используется как гидрофильный матричный агент, благодаря которому обеспечивается пролонгированное высвобождение действующего вещества. При попадании таблетки в жидкую среду гидрофильный матрикс способен впитывать массу воды без растворения с образованием гидрогеля. Модифицированное высвобождение алфузозина находит отражение и в фармакокинетическом профиле препарата: отсутствие пиков концентрации препарата в сыворотке обеспечивает равномерное поступление алфузозина в сыворотку на протяжении 24 ч, тем самым оказывая минимальное и клинически незначимое воздействие на колебания как САД, так и ДАД.
Выводы. Алфупрост® МР (10 мг 1 раз/сут.) подтвердил свою эффективность в отношении уменьшения СНМП и улучшения качества жизни мужчин с ДГПЖ. Суммарный балл IPSS через 12 мес. терапии улучшился на 8,6 балла (в 1,9 раза), средний показатель максимальной скорости мочеиспускания увеличился на 5,3 мл/с (в 1,4 раза), объем остаточной мочи уменьшился на 25,7 мл (в 3,8 раза), что позволило улучшить качество жизни пациентов, согласно результатам заполнения опросника QoL, в среднем на 2,49 балла (в 2,3 раза). К концу исследования наблюдалось улучшение копулятивной функции главным образом за счет эректильной составляющей, при этом эякуляторная функция не ухудшалась. На протяжении 12 мес. терапии Алфупрост® МР не оказывал клинически значимого влияния на показатели САД, ДАД и ЧСС. Все пациенты закончили исследование и, как и врачи, были удовлетворены результатами проведенной терапии.
Результаты нашего наблюдения позволяют рекомендовать Алфупрост® МР как эффективное средство лечения СНМП при ДГПЖ, обладающее минимальными вазодилатирующими эффектами. Это позволяет применять его длительно, в том числе и коморбидным пациентам.



