Введение. Мочекаменная болезнь (МКБ) представляет собой одну из актуальных проблем современной урологии в связи с высокой распространенностью и склонностью к рецидивированию [1, 2]. Уролитиаз – это одна из форм заболеваний обмена веществ, которая имеет тенденцию к неуклонному росту в связи с особенностями характера питания людей, увеличением числа неблагоприятных экологических и социальных факторов, оказывающих как прямое, так и опосредованное действие на организм человека. С учетом постоянного роста заболеваемости клинические аспекты диагностики, лечения и метафилактики МКБ сохраняют значимость. Актуальность проблемы МКБ обусловлена тем, что в 65–70% случаев болезнь диагностируют у лиц в возрасте 20–55 лет, т.е. в наиболее трудоспособном периоде жизни [3, 4]. Ежегодно регистрируют не менее 85 тыс. больных МКБ, при этом 62 тыс. из них – с рецидивным камнеобразованием. В настоящее время в развитых странах мира из 10 млн человек примерно 400 тыс. страдают МКБ. Больные МКБ составляют 30–40% всего контингента урологических стационаров.
Совершенствование диагностики МКБ и появление современных методов лечения изменили структуру форм заболевания [5]. Однако известно, что как бы эффективно ни была проведена хирургическая операция по удалению конкремента, без последующей комплексной и индивидуальной метафилактики отдаленный и конечный результаты лечения будут неудовлетворительными [6]. Многочисленные метаболические нарушения при МКБ требуют применения различных лекарственных препаратов. В то же время, несмотря на постоянное расширение ассортимента синтетических лекарственных средств, значительное место в лечении и профилактике МКБ занимают препараты растительного происхождения [1–6].
Использование фитопрепаратов (роватинекс, канефрон и др.) связано со следующими клинико-фармакологическими аспектами лечебного действия:
- физиологически активные вещества препаратов на растительной основе проявляют разностороннюю фармакологическую активность, способствуя эффективному лечению многих заболеваний, и не оказывают побочного действия на организм [7];
- совокупность диуретического, противовоспалительного и спазмолитического эффектов обеспечивает высокий литокинетический эффект [8];
- препараты на растительной основе реже вызывают осложнения в отличие от синтетических препаратов, поэтому их можно использовать в течение длительного промежутка времени;
- потенцируют действие антибактериальных препаратов [9];
- если препарат на растительной основе имеет антибактериальный эффект, он не вызывает дисбактериоза и никогда не провоцирует суперинфекцию [10].
Кроме того, одним из важных преимуществ препаратов на растительной основе является минимальное количество побочных реакций и нежелательных лекарственных взаимодействий, а также возможность длительного приема, что очень важно в метафилактике рецидива МКБ [7–10].
Таким образом, в лечении больных МКБ растительные препараты используют для:
- профилактики рецидивов камнеобразования;
- улучшения самостоятельного отхождения конкрементов, в том числе и их фрагментов после дистанционной литотрипсии (ДЛТ);
- профилактики обострений хронических воспалительных заболеваний органов мочеполовой системы, главным образом хронического калькулезного пиелонефрита [7–10].
В лечении больных МКБ давно и эффективно применяется фитотерапия эфирными маслами или терпенами. Терпены (лат. Oleum Terebinthinae) – класс углеводородов, продуктов биосинтеза с общей формулой (C5H8)n, с углеродным скелетом, формально являющимся производным изопрена СН2=С(СН3) – СН=СН2. В больших количествах терпены содержатся в растениях семейства хвойных. Основной фармакологический эффект этих веществ заключается в снятии спазма гладкой мускулатуры чашечно-лоханочной системы и мочеточника. Эфирные масла и терпены усиливают почечный кровоток, что приводит к увеличению диуреза. Кроме того, терпены в высоких концентрациях демонстрируют бактериостатический эффект [11]. Одним из препаратов, основу которого составляет особая комбинация растительных терпенов, является Роватинекс, имеющий 60-летнюю историю применения более чем в 60 странах мира.
В России Роватинекс зарегистрирован (рег. № ЛСР-006862/08) в 2008 г. в виде кишечно-растворимых желатиновых капсул. В состав препарата входят анетол 4 мг; борнеол 10 мг; камфен 15 мг; пинен{α+β} 31 мг; фенхон 4 мг; цинеол 3 мг. Анетол, борнеол и камфен оказывают диуретический, противовоспалительный (антибактериальный) эффекты, а также усиливают почечный кровоток; пинен{α+β} и фенхон ответственны за спазмолитический и противовоспалительный (антибактериальный) эффекты, цинеол – за противовоспалительный (антибактериальный) эффект. Не исключено и собственное экспульсивное действие Роватинекса, обусловленное тропностью терпеновых соединений, входящих в его состав, к гладкой мускулатуре мочеточников. Именно данный состав делает препарат уникальным в качестве вспомогательного средства в терапии больных МКБ [12, 13].
Установлено, что Роватинекс:
- оказывает спазмолитическое действие; способствует отхождению камней и их фрагментов; уменьшает выраженность боли; усиливает почечный кровоток, улучшая функцию почек и повышая диурез [14–16];
- обладает противовоспалительным и противомикробным действиями по отношению к грамположительным и грамотрицательным микроорганизмам [14–16];
- усиливает фармакологический эффект антимикробных препаратов [17];
- повышает содержание защитных коллоидов и глюкуроновой кислоты в моче [17];
- содержит легкоусвояемые жирорастворимые терпены природного происхождения, которые выводятся с мочой;
- можно назначать детям с 6 лет [18, 19].
Показания к применению:
- общая профилактика МКБ;
- комплексная метафилактика рецидивов камнеобразования после ДЛТ, чрескожной нефролитотрипсии (ЧНЛТ) и контактной уретеролитотрипсии (КУЛТ);
- литокинетическая терапия при камнях почки и мочеточника;
- купирование почечной колики;
- комплексная терапия острого и хронического калькулезного пиелонефрита.
Во время лечения необходимо увеличить прием жидкости для усиления суточного диуреза. Препарат с осторожностью следует назначать пациентам, принимающим противосвертывающие препараты. Роватинекс не рекомендован к применению в I триместре беременности и во время лактации. Обычно взрослым и детям старше 14 лет назначают по 1–2 капсулы 3 раза в сутки, детям после 6 лет – по 1 капсуле 2 раза в сутки. При почечной колике возможно увеличение дозы до 2–3 капсул 4–5 раз в сутки.
Представляет интерес применение этих свойств препарата для пациентов после ДУВЛ с целью улучшения отхождения осколков конкремента.
Цель работы: оценить клиническую эффективность препарата Роватинекс в качестве литокинетического средства после дистанционной литотрипсии (ДЛТ).
Материалы и методы. В исследование были включены 220 пациентов с МКБ, которым выполнили ДЛТ.
В зависимости от проводимого после ДЛТ лечения пациенты были разделены на две группы. В основную группу вошли 150 больных (86 мужчин и 64 женщины). У 70 (46,7%) человек камень локализовался в почке, при этом у 31 (20,7%) – в верхней трети, у 15 (10,0%) – в средней и у 34 (22,7%) – в нижней трети мочеточника. У 61 (40,7%) пациента размер камней составил 1–1,9 см. Всем пациентам данной группы после ДЛТ был назначен Роватинекс 1–2 капсулы в день до еды 3 раза в день в течение месяца.
Контрольную группу составили 70 больных (39 мужчин и 31 женщина). В 61 (87,1%) наблюдении камни локализовались в почке, в 5 (7,1%) – в верхней трети, в 1 (1,4%) – в средней и в 3 (4,3%) – в нижней трети мочеточника. У 43 (61,4%) пациентов размер камней составил 0,5–0,9 см.
В послеоперационном периоде после дистанционной литотрипсии назначались спазмолитические препараты (баралгин и т.д.).
Дистанционную литотрипсию выполняли с использованием литотриптеров Siemens «Modularis» и Dornier «Gemini».
Программа клинического обследования включила стандартные лабораторные и лучевые методы исследования. Обязательными стали оценка боли по визуальной аналоговой шкале и исследование физико-химической структуры мочевых камней для определения типа камнеобразования и детализации последующей метафилактики. Контрольное обследование (общий анализ крови и мочи, биохимический анализ крови, суточная экскреция, лучевые методы исследования и т.д.) пациентов в обеих группах проводили через 30 дней после сеанса ДЛТ, так как длительность приема Роватинекса в основной группе составила 30 дней.
Критерии клинической эффективности Роватинекса:
- частота возникновения почечной колики после ДЛТ;
- сроки и процент отхождения фрагментов камня после ДЛТ;
- индивидуальная переносимость препарата.
Результаты обработаны с применением статистической программы MedCalc (MedCalc Statistical Software version 17.0.,2017). Данные представлены в виде среднего и стандартного отклонений. Сравнение данных выполняли с применением критерия лог-рангового критерия, критерия Краскелла–Уоллиса, критерия χ². Уровень значимости Р принят равным 0,05.
Результаты и обсуждение. В основной группе почечная колика через 30 дней поле ДЛТ отмечена у 19 (12,7%) пациентов, при этом выраженность боли по ВАШ соответствовала 5 баллам. Среди пациентов контрольной группы почечная колика отмечена у 32 (45,7%) пациентов, уровень боли по ВАШ соответствовал 7 баллам. Таким образом, на фоне приема Роватинекса почечную колику после ДЛТ наблюдали реже, чем при приеме спазмолитиков (р<0,0001).
Отхождение фрагментов после ДЛТ в течение 1–5 сут. в основной группе отмечено у 104 (69,3%) больных, в контрольной – у 30 (42,9%; рис. 1).
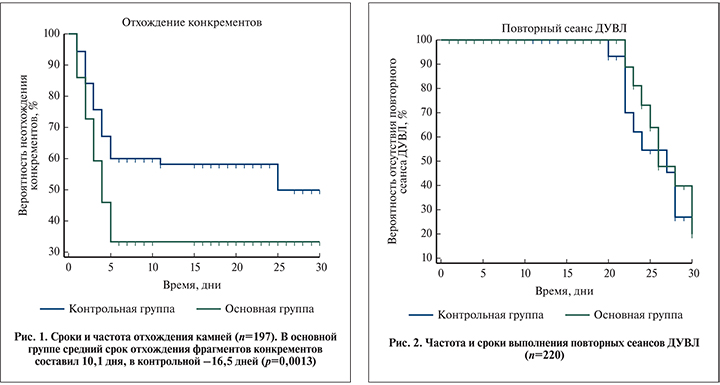
Частота выполнения повторного сеанса ДЛТ в основной группе составила 9,3%, в контрольной – 12,9% (рис. 2).
Средний срок выполнения повторного сеанса ДУВЛ в основной группе составил 26 дней, в контрольной – 25 дней. Статистически значимых различий сроков выполнения повторных сеансов ДЛТ в группах не выявлено (р=0,5102).
При изучении влияния проводимой терапии на динамику показателей общего анализа крови, биохимического анализа крови и суточной экскреции (магния, мочевой кислоты, кальций и т.д.) в основной группе не было установлено существенных отличий от соответствующих значений пациентов контрольной группы и нормативных показателей. Анализ параметров функционального состояния почек, а также основных показателей обмена камнеобразующих веществ не выявил изменений в обеих группах, следовательно, Роватинекс не влияет на динамику лабораторных показателей.
Критерием результативности литокинетического эффекта служит увеличение суточного диуреза. На фоне приема Роватинекса пациентами основной группы отмечено увеличение диуреза с 1600 (810–2200) до 1750 (1400–2650) мл/сут (р=0,011), в контрольной группе – с 1300 (910–1900) до 1525 (1250–1800) мл/сут (р=0,0317). Исходно у пациентов основной группы суточный диурез был выше (р=0,0011).
Динамика диуреза на фоне анальгетического и спазмолитического эффекта Роватинекса способствует эффективному и быстрому отхождению фрагментов камней после ДЛТ.
По данным клинического анализа мочи отмечено снижение лейкоцитурии в обеих группах: в основной – с 25±5 до 5±3 в поле зрения, в контрольной – с 20±4 до 6±2 в поле зрения. Кроме того, в основной группе отмечена стабилизация рН-мочи в пределах 6,2–6,8, что важно и необходимо в метафилактике рецидивного камнеобра-зования.
Всем пациентам был выполнен бактериологический посев мочи с определением вида и титра возбудителя.
В основной группе до лечения бактериурия (103–104–105) выявлена у 31 (20,7%) пациента, в контрольной – у 15 (21,4%; р=0,8972). При этом в основной группе у 18 (12%) пациентов до лечения выявлена E. coli, в то время как в контрольной группе таких пациентов было 7 (10%). У остальных пациентов обеих групп микрофлора была представлена следующими возбудителями: Staphylococcus aureus, Streptococcus faecalis, Pseudomonas aeruginosa, Klebsiella pneumoniae, Proteus mirabilis. При анализе динамики после лечения бактериурия в основной группе выявлена у 6 (4,6%) человек, в контрольной – у 4 (5,8%; р=0,7081).
Как известно, изучение состава мочевого камня обязательно в обследовании больного МКБ, так как позволяет определить тип камнеобразования и индивидуально подойти к метафилактике. В настоящее время с этой целью мы используем различные методы исследования (рентгенофазовый, спектральный, химический и т.д.) физико-химической структуры мочевых камней [15, 16].
В таблице приведен результат физико-химического анализа конкременов и их фрагментов, которые удалось получить.
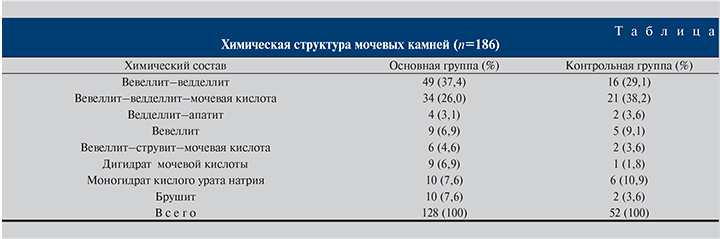
Таким образом, в основной группе у 58 (44,3%) пациентов выявлены оксалаты, у 44 (33,6%) – камни смешанного состава, у 19 (14,5%) – ураты, у 10 (7,6%) – фосфаты.
В контрольной группе в 21 (38,2%) случае выявлены оксалаты, в 25 (45,5%) – конкременты смешанной структуры, в 7 (12,7%) – ураты, в 2 (3,6%) – фосфаты. Значимых различий распределения пациентов по составу камней не выявлено (р=0,4144).
Средний срок отхождения камня в основной группе после ДУВЛ у пациентов с оксалатным камнем составил 9,9 дня, при смешанном – 10,2, при уратном – 5,9, а при фосфатном – 3,3 дня (рис. 3). Значимых различий в сроках отхождения фрагментов конкрементов после ДУВЛ в зависимости от состава камня не выявлено (р=0,197).
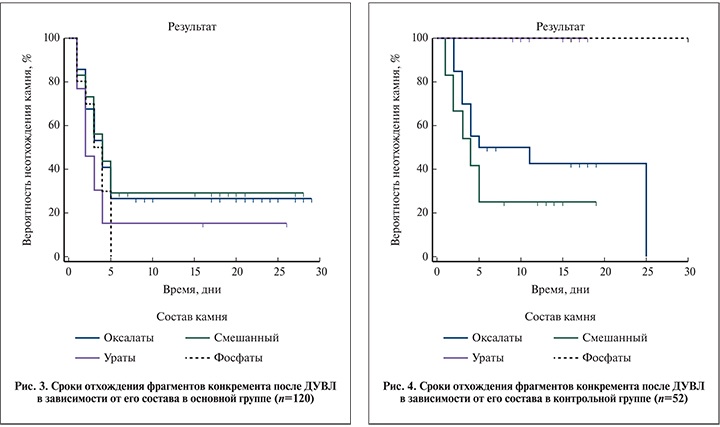
Средний срок отхождения фрагментов конкремента, состоящего из оксалатов, после ДУВЛ составил 13 дней, смешанного состава – 6,9, уратов – 18 дней, фосфатов – 30 дней (рис. 4). На диаграммах представлено, что наименьший срок отхождения фрагментов конкремента после ДУВЛ в контрольной группе отмечен у пациентов с оксалатами и конкрементами смешанного состава (р=0,006).
Побочных эффектов на фоне приема Роватинекса нами не отмечено.
Выводы
- Назначение препарата Роватинекс сокращает срок отхождения фрагментов камней после ДЛТ.
- Прием препарата Роватинекс приводит к снижению лейкоцитурии и увеличению суточного диуреза.
- Эффект препарата Роватинекс не зависит от состава конкремента.
- Прием Роватинекса не сопровождается развитием осложнений, побочных эффектов, что позволяет принимать его в течение длительного времени в составе комплексной литокинетической терапии и для метафилактики рецидивного камнеобразования.



