Введение. Хронический рецидивирующий бактериальный простатит (ХРБП) представляет собой актуальную проблему современной урологии и служит ведущей нозологией в структуре заболеваний мужской репродуктивной системы, существенно ухудшающей качество жизни, отрицательно влияющей на семейные взаимоотношения, работоспособность и т.д. [1–4].
Патофизиология ХРБП признана многогранной, хотя в большинстве случаев удается выделить один из доминирующих механизмов развития – инфекционный, иммунологический, неврологический, эндокринный и психологический [5, 6].
Дисфункция иммунологических звеньев у пациентов с ХРБП – одна из важных причин рецидива заболевания и отсутствия эффекта антибактериальной терапии [7, 8]. Иммунологические нарушения в простате иногда играют ключевую роль в персистенции микроорганизмов в предстательной железе (ПЖ) [9–11]. Кроме того, постоянное воздействие факторов патогенности микроорганизмов приводит к полному срыву процессов иммунологической защиты простаты на фоне дисфункции иммунной системы, что способствует нарушению функций предстательной железы [12–14].
Данные обстоятельства стали причиной поиска альтернативных методов лечения, которые бы дополнили существующие стандарты лечения, рекомендованные РОУ и EAU [8, 15].
Цель исследования: изучение эффективности иммуноактивной терапии (препаратом рекомбинантного интерферона альфа-2b c антиоксидантным комплексом) в сочетании с антибактериальной терапией при ХРБП.
Материалы и методы. Проведено проспективное обследование и лечение 62 пациентов с ранее установленным диагнозом ХРБП.
План обследования включил опросники (NIH – CPSI, IPSS, Гамильтона), общие анализы крови и мочи, биохимический анализ крови, соскоб уретры на ЗППП (ПЦР-диагностика), тестостерон в сыворотке крови, световую микроскопию, бактериологическое исследование и ИФА секрета предстательной железы (СПЖ), урофлоуметрию, трансректальное сонографическое исследование (ТРУЗИ).
Дизайн исследования: проспективное рандомизированное простое сравниваемое исследование эффективности комбинированной терапии интерферонами и антибактериальными препаратами.
В зависимости от выбора терапии обследуемые пациенты были разделены на две группы. Пациентам I группы (n=31) проводили комбинированную терапию: АБТ, согласно индивидуальной антибиотикограмме, дополненную интерферонотерапией препаратом ВИФЕРОН®, суппозитории ректальные 3 млн МЕ 2 раза в день через каждые 12 ч в течение 4 нед.; пациентам II (контрольной) группы (n=31) проводили только АБТ, согласно индивидуальной антибиотикограмме, в течение 4 нед.
Критерии включения пациентов в исследование: возраст старше 18 лет; наличие симптомов ХБП; лабораторно подтвержденный диагноз ХРБП, согласно стандартам РОУ и EAU; согласие пациента участвовать в исследовании.
Критерии невключения пациентов в исследование: наличие ЗППП и других заболеваний простаты (гиперплазия, рак, склероз); инфекционно-воспалительных заболеваний мочевых путей и репродуктивных органов (везикулит, уретрит, пиелонефрит); инфравезикальной обструкции (стриктура уретры, склероз шейки мочевого пузыря, а также МКБ и др.); сопутствующей ССС, неврологической, эндокринной, системной и др. патологий, которые могли бы повлиять на результаты исследования; аномалий со стороны мочевых путей и репродуктивных органов; дефицита тестостерона; любого иммунодефицитного состояния; приема антибактериальных или других средств с антибактериальным, простатопротективным, противовоспалительным, иммуностимулирующим действиями в течение 30 дней до включения в исследование.
Статистическая обработка данных проведена с использованием электронных таблиц Microsoft Excel из пакета программ Microsoft Office 2007 и статистического пакета STATISTICA 6.1 (StatSoft Inc., США). Соответствие распределения признаков закону нормального распределения осуществлено с применением критерия Шапиро–Уилка.
Анализ жалоб, анамнестических данных, лабораторных показателей и данных инсрументальных исследований подтвердил равноценность групп до лечения.
Клиническую и лабораторную эффективность проведенного лечения пациентов с ХРБП оценивали сразу после лечения (1 мес. от начало терапии), а также через 3, 6, 12 мес. после завершения запланированной терапии.
 Статья выполнена в рамках диссертационной работы, одобренной Локальным независимым этическим комитетом ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России.
Статья выполнена в рамках диссертационной работы, одобренной Локальным независимым этическим комитетом ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России.
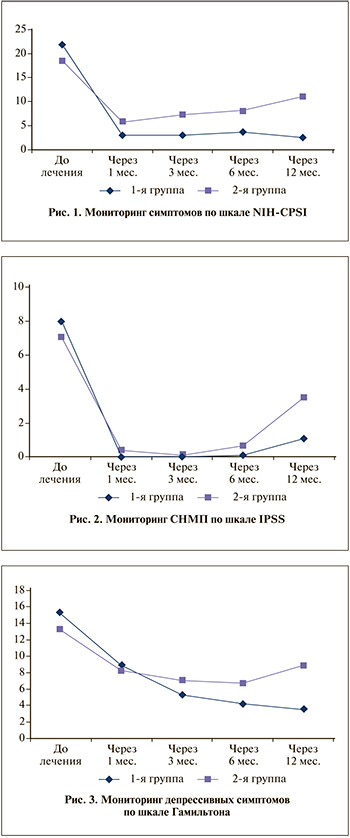
Результаты. По данным анкеты NIH-CPSI, после завершения лечения (к концу 4-й недели) среднее значение суммы баллов у пациентов I группы снизилось с 18,6±2,8 до 3,1±0,5. Через 3, 6, 12 мес. данный показатель существенно не изменился.
У пациентов II группы среднее значение данного показателя до лечения составляло 21,8±0,7 балла, к концу лечения – 5,8±0,5, через 3 мес. – 7,3±0,9, к 6-му месяцу увеличилось до 8,1±0,4 балла, а к 12-му достигло 11±0,5 балла (р<0,05) (рис. 1).
Согласно оценке СНМП по шкале IPSS, через 1 мес. после проведенной терапии достоверное снижение симптомов отмечено в обеих исследуемых группах (p<0,05) (рис. 2).
Однако к 12-му месяцу после завершения лечения среднее значение суммы балов по шкале IPSS у пациентов I группы составляло 1,1±0,1 балла, у пациентов II группы, получавших только АБТ, – 3,5±0,4 балла.
Анализ депрессивных симптомов после завершения лечения по шкале Гамильтона выявил, что среднее значение суммы баллов у пациентов I группы снизилось с 15,3±0,5 до 9,9±0,2 балла, а к 3-му месяцу лечения составило 5,3±0,3 балла. Через 6 мес. данный показатель значительно не изменился – 4,2±0,3 балла, а к 12-му месяцу имелась тенденция снижения среднего значения до 3,5±0,5 балла.
У пациентов II группы средний показатель суммы шкалы Гамильтона снизился с 13,3±0,5 до 8,3±0,5 балла. Через 3 и 6 мес. значение составляло 7,0±0,2 и 6,7±0,3 балла соответственно, к 12-му месяцу повысилось до 8,9±0,3 балла (рис. 3).
Таким образом, согласно оценке клинических проявлений, сразу же после завершения терапии и через 1, 3, 6, и 12 мес. достоверное снижение клинических проявлений было отмечено у пациентов I группы, которым проводилась комбинированная терапия.
Согласно интерпретации данных микроскопического исследования СПЖ, после проведенного лечения во все периоды наблюдения имело место снижение степени выраженности инфекционно-воспалительного процесса в СПЖ, оцениваемое главным образом по числу лейкоцитов. По завершении терапии среднее количество лейкоцитов в СПЖ у пациентов I группы снизилось с 145±5,0 в поле зрения до 50±5,0, к 12-му месяцу данный показатель приблизился к нормативному значению (16±5,0 лейкоцитов в поле зрения). У пациентов II группы количество лейкоцитов в СПЖ после завершения терапии также снизилось с 138±5,0 в поле зрения до 69±5,0 и в 12 мес. составляло 40±5,0 лейкоцитов в поле зрения (рис. 4).
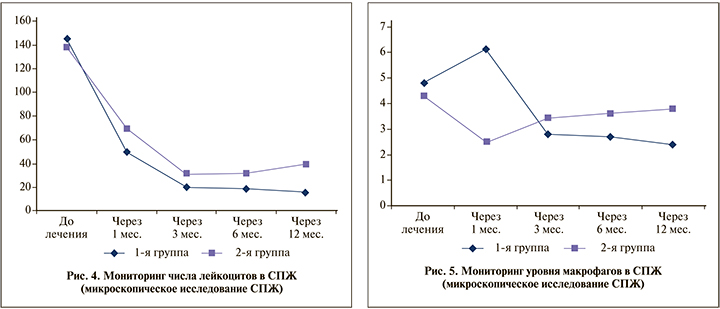
Касательно количества макрофагов в СПЖ после завершения терапии пациентов I группы, среднее количество макрофагов повысилось с 4,8±0,2 до 6,1±0,2 в поле зрения, что было обусловлено действием интерферонотерапии и повышением фагоцитарной активности макрофагов. Согласно оценке числа макрофагов через 3, 6 и 12 мес. по мере снижения признаков инфекционно-воспалительного процесса в ПЖ имело место снижение числа макрофагов в СПЖ.
У пациентов II группы цитологическая картина была прямо пропорциональна таковой цитологического исследования СПЖ у пациентов I группы. По окончании лечения среднее значение количества макрофагов снизилось с 4,3±0,2 до 2,5±0,2, что свидетельствовало об угнетении местного иммунитета, а через 3, 6 и 12 мес. после лечения отмечено повышение среднего числа макрофагов в СПЖ, обусловленное повторной активацией инфекционно-воспалительного процесса в простате (рис. 5).
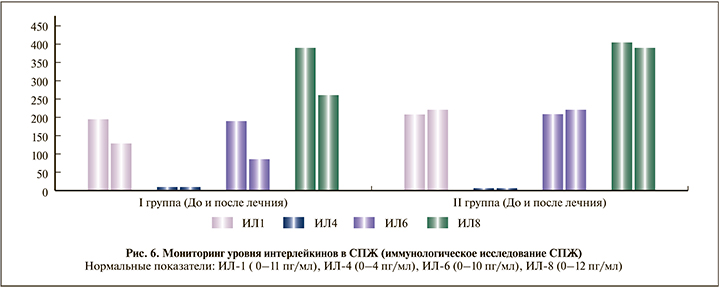
Кроме того, согласно оценке иммунологических параметров СПЖ, у больных ХРБП отмечено повышение уровня ИЛ-1, -6 и -8 в обеих группах. На фоне проводимой терапии отмечено достоверное снижение уровня провоспалительных цитокинов у пациентов I группы, получавших комбинированную терапию (рис. 6).
При определении максимальной скорости мочеиспускания (МСМ), по данным урофлоуметрии отмечено, что до лечения группы были сопоставимыми, среднее значение в обеих группах соответствовало нормативным значениям: в первой группе – 18,7, во второй – 18,9 мл/с. Согласно контрольной оценке вышеуказанного исследования, выполненного через 1, 3, 6, 12 мес., наблюдалось улучшение максимальной скорости потока мочи в обеих группах: в I – 24,8 мл/с, во II группе – 21,0 (р<0,05).
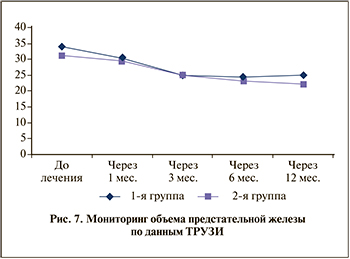 Контрольное ТРУЗИ ПЖ (1, 6, 12 мес. после лечения) показало: у пациентов обеих групп отмечено улучшение данных ультразвуковой картины ПЖ. Согласно мониторингу результатов, достоверных различий между группами по объему ПЖ отмечено не было (рис. 7).
Контрольное ТРУЗИ ПЖ (1, 6, 12 мес. после лечения) показало: у пациентов обеих групп отмечено улучшение данных ультразвуковой картины ПЖ. Согласно мониторингу результатов, достоверных различий между группами по объему ПЖ отмечено не было (рис. 7).
При оценке клинической эффективности терапии больных I группы через 12 мес. после завершения лечения положительный эффект выявлен у 22 (70,9%) мужчин, при этом выздоровление отмечено у 15 (48,4%) пациентов, улучшение – у 7 (22,5); у 9 (29,1%) пациентов данной группы клиническая эффективность отсутствовала. Во II группе положительный эффект имели 12 (38,7%) больных, из них выздоровление отмечено у 7 (22,5%) пациентов, улучшение – у 5 (16,2%), у 19 (61,3%) пациентов клиническая эффективность отсутствовала.
Обсуждение. ХРБП – это патологическое состояние, существенно ухудшающее качество жизни пациентов. Согласно литературным данным, рекомендуемое РОУ и EAU антибактериальное лечение в качестве терапии 1-й линии эффективно далеко не для всех пациентов [5].
Полученные нами данные свидетельствуют о том, что у пациентов с ХРБП в ПЖ на фоне инфекционно-воспалительного процесса происходят выраженные аутоиммунные нарушения, которые можно идентифицировать только специфическими исследованиями СПЖ (световая микроскопия и ИФА СПЖ). У всех обследованных пациентов, по данным микроскопического и иммунологического исследований СПЖ, были выявлены нарушения местного иммунитета, способные поддерживать хроническое воспаление в ПЖ. По данным световой микроскопии, СПЖ характеризуется в 100% случаев дефектом фагоцитоза. Нарушения иммунологических параметров СПЖ у пациентов с ХРБП обусловливают включение в план лечения иммуноактивных препаратов, направленных на активацию факторов местного иммунитета. Одним из альтернативных методов лечения инфекций мочевых путей и репродуктивных органов с высокой доказательной базой является интерферонотерапия [16, 17].
Согласно нашим результатам, на фоне проведенной комбинированной терапии отмечена нормализация не только клинических показателей у пациентов с ХРБП, но и данных лабораторных исследований.
Так, по данным световой микроскопии, нормализация лабораторных показателей СПЖ имела место у пациентов I группы, которым в сочетании с антибактериальной терапией проводили интерферонотерапию, а у пациентов II группы, получавших монотерапию АБП, среднее значение числа лейкоцитов в СПЖ было выше нормативных показателей и после терапии так и не снизилось. Также у пациентов II группы по окончании терапии среднее число макрофагов имело тенденцию к повышению по сравнению с таковым у пациентов I группы, что свидетельствует о сохранении активного инфекционно-воспалительного процесса в ткани ПЖ.
Кроме того, на фоне интерферонотерапии, по данным ИФА СПЖ, отмечено снижение уровня ИЛ-1, -6 и -8 у пациентов I группы относительно II, получавшей только АБТ.
Включение рекомбинантного интерферона альфа-2b c антиоксидантным комплексом (витаминами Е и С) в состав стандартной терапии ХРБП позволяет нормализовывать у превалирующего большинства пациентов как клинические, так и лабораторные показатели ХРБП, а также способствует купированию воспалительного процесса, снижая клинические проявления хронического простатита и восстанавливая вторичный иммунодефицит.
Предложенный нами способ лечения (Патент РФ № 2723997) ХРБП с использованием интерферонотерапии в 70,9% случаев приводит к клинической эффективности проводимого лечения.
Выводы. Поскольку при хронических инфекциях с большой частотой отмечаются нарушения в иммунной реактивности организма, стандартную терапию антибиотиками целесообразно дополнять препаратом рекомбинантного интерферона альфа-2b ВИФЕРОН® (суппозитории ректальные), который помимо интерферона альфа-2b содержит антиоксиданты токоферола ацетат и аскорбиновую кислоту.
Стандартная антибактериальная терапия хронического рецидивирующего бактериального простатита приводит к ремиссии простатита в течение 12 мес. в 38,7% случаев. Тогда как антибактериальная терапия хронического рецидивирующего бактериального простатита в сочетании с иммуноактивной терапией повышает клиническую эффективность до 70,9%.



