Злокачественные новообразования яичек у детей встречаются крайне редко. В детском возрасте они составляют 1–2% от всех солидных опухолей [1, 2]. Наиболее часто в данной группе диагностируются герминогенные опухоли яичка: на их долю приходится от 60 до 75% всех злокачественных опухолей яичка у детей [2]. Менее распространенными злокачественными новообразованиями являются стромальные опухоли гонад (25–28%), паратестикулярная рабдомиосаркома (5–8%), поражение тестикул при лейкозах (5%) и лимфомах (~3%) [1, 2].
Первичные лимфомы яичка
Первичные лимфомы яичка (Primary testicular lymphoma) (ПТЛ) являются редким заболеванием и составляют, по разным данным, 2–9% от всех новообразований данной локализации [3]. Согласно популяционным исследованиям, ежегодная заболеваемость варьируется от 0,09 до 0,26 на 100 тыс. населения [4]. В группе неходжкинских лимфом (НХЛ) они составляют всего 1–2% случаев. Однако, несмотря на низкую общую заболеваемость, это наиболее распространенное злокачественное новообразование яичек у мужчин старше 50 лет с преобладанием одностороннего поражения [3]. Двустороннее поражение встречается в 6–10% случаев [4]. Подавляющее большинство ПТЛ у взрослых (от 80 до 98%) представлено диффузной В-крупноклеточной лимфомой (ДВККЛ) [5]. К редко встречающимся ПТЛ относятся лимфома из клеток зоны мантии [6–8], NK/T-клеточная лимфома [9]. В детском возраста в литературе описаны случаи фолликулярной лимфомы (ФЛ) [10], лимфомы Беркитта (ЛБ) [11], Т-лимфобластной лимфомы (Т-ЛБЛ) [12] с изолированной локализацией в яичке.
Клинически поражение яичек при ПТЛ чаще всего диагностируется на основании данных объективного осмотра: увеличенного размера, одностороннего безболезненного отека, у некоторых пациентов может присутствовать болезненность в области мошонки [13]. Методы визуализации, которые могут помочь в диагностике ПТЛ, включают ультразвуковое исследование (УЗИ) с допплерографией, которое позволяет визуализировать фокальные или диффузные гипоэхогенные области с гиперваскуляризацией в увеличенном яичке [14], и магнитно-резонансную томографию (МРТ), которая дает возможность одновременно оценить оба яичка, паратестикулярные области и семенной канатик. При ПТЛ на МРТ в Т2-режиме обычно выявляется гипоинтенсивное образование, с целью оценки внутренней структуры и границ которого используют контрастное усиление [15]. При подозрении на ПТЛ на первом этапе показана паховая орхиэктомия с последующим проведением гистологического и иммуногистохимического (ИГХ) исследований [16].
Отсутствие стандартизированного подхода к лечению ПТЛ объясняется редкостью данного заболевания [17]. Большинству взрослых пациентов с ПТЛ тактика терапии предполагает проведение оперативного вмешательства в объеме орхиэктомии с дальнейшей химиотерапией по схеме R-CHOР (ритуксимаб, циклофосфамид, доксорубицин, винкристин и преднизолон, профилактика поражения центральной нервной системы в виде интратекального введения цитостатиков) и лучевой терапии на область контрлатерального яичка (суммарная очаговая доза – 25–45 Гр в зависимости от стадии и морфоиммуногистохимического варианта заболевания), а также поражения регионарных лимфоузлов [18]. В детском возрасте ПТЛ встречается гораздо реже, чем у взрослых, что объясняет отсутствие клинических рекомендаций по лечению данного заболевания и исследований, направленных на изучение преимуществ одного метода лечения перед другим.
Современные представления о клинических, иммуноморфологических, лабораторных характеристиках ПТЛ у детей складываются из описания единичных клинических наблюдений. Так, в одной из работ описано три клинических наблюдения ФЛ у детей в возрасте от 4 до 11 лет с первичным поражением яичка, каждому из пациентов после орхиэктомии была проведена химиотерапия в объеме двух курсов CHOР (циклофосфамид, винкристин, преднизолон и доксорубицин). После проведенного лечения все пациенты достигли полной ремиссии. Средняя длительность наблюдения после завершения ПХТ составила от 7 до 59 мес., рецидивов зарегистрировано не было [19]. Также описано единичное наблюдение ФЛ с изолированным поражением яичка у 3-летнего мальчика, которому была выполнена левосторонняя орхиэктомия без последующей системной химиотерапии, период наблюдения после оперативного вмешательства составил 30 мес., в течение которых ребенок находился в полной ремиссии [1].
В 2005 г. группой исследователей во главе с Yavuz Köksal было опубликовано клиническое наблюдение ЛБ у 13-летнего ребенка с изолированным тестикулярным поражением, которому после оперативного вмешательства в объеме орхиэктомии было проведено два курса полихимиотерапии. Первый курс включал препараты циклофосфамид, винкристин, преднизолон, адриамицин; 2-й курс: циклофосфамид, винкристин, преднизолон, адриамицин, метотрексат. Период наблюдения за пациентом составил 19 мес., данных за рецидив или прогрессирование не получено [11].
Впервые в 2020 г. Yongren Wang, Jian Li, Yongjun Fang описали клиническое наблюдение первичной Т-ЛБЛ яичка у 3-летнего ребенка. Пациенту была проведена правосторонняя паховая орхиэктомия с последующей химиотерапией (протокол SMCC-2011, модифицированный на основе режима NHL-BFM-90/95) без лучевой терапии контрлатерального яичка. У ребенка была достигнута полная ремиссия, которая сохранялась на протяжении 36-месячного периода наблюдения [12].
Тестикулярное поражение при остром лимфобластном лейкозе
Анатомически гемато-тестикулярный барьер (ГТБ) – это физиологический гистогематический барьер между кровеносными сосудами и извитыми семенными канальцами, который состоит из плотных соединений между клетками Сертоли и миоидными клетками, выстилающими семенные канальцы. Главная функция ГТБ – защитная. ГТБ не позволяет иммунным клеткам попасть в семенные канальцы, таким образом предотвращая развитие аутоиммунных заболеваний и выработку антиспермальных антител, ведущих к мужскому бесплодию [20]. Доказано, что при использовании химиотерапевтических агентов ГТБ снижает их способность проникать в ткани, уменьшает терапевтический эффект проводимого лечения [13].
При остром лимфобластном лейкозе (ОЛЛ) у детей на момент диагностики поражение яичек обнаруживается у 1,1–2,4% мальчиков. У мужчин инициально поражение яичек встречается еще реже [21–22]. Усовершенствование протоколов терапии, используемых в лечении детей с первично диагностированным ОЛЛ, позволило добиться результатов 5-летней общей выживаемости (ОВ), превысившей 90% [23]. Тем не менее изолированный тестикулярный рецидив встречается с частотой 0,5–2% среди мальчиков, по данным исследований ALL Children’s Cancer Group (CCG), как в стандартной группе риска, так и в группе высокого риска [24–26]. Пятилетняя ОВ у пациентов с ранним тестикулярным рецидивом (развившимся <18 мес. после постановки диагноза) составляет 13,6%, что значительно хуже, чем у пациентов в промежуточной группе (18–36 мес. после постановки диагноза), – 52,2%, или поздним рецидивом (≥36 мес. после постановки диагноза) – 60,0% [27].
Поражение яичек при ОЛЛ инициально или на момент возникновения рецидива при физикальном обследовании диагностируется на основании увеличения размера, одностороннего отека и/или плотной консистенции яичек. Для подтверждения поражения яичек используется ультразвуковое исследование органов мошонки. УЗИ в режиме «серой шкалы» обычно показывает увеличение одного или обоих яичек с диффузными или фокальными областями сниженной эхогенности, при этом допплерография позволяет выявлять усиление кровотока внутри очага поражения [13]. С целью верификации диагноза проводится пункционная биопсия с дальнейшим цитологическим исследованием полученного материала, по показаниям – биопсия яичка с последующим морфоиммуногистохимическим исследованием [28].
Пациентам с диагнозом «ранний тестикулярный рецидив В-линейного ОЛЛ» (В-ОЛЛ), а также пациентам с диагнозом «Т-линейный ОЛЛ» (Т-ОЛЛ) вне зависимости от времени возникновения тестикулярного рецидива рекомендуется агрессивное противоопухолевое лечение, включающее трансплантацию гемопоэтических стволовых клеток (ТГСК). Если в схему предтрансплантационного кондиционирования включено тотальное облучение тела (ТОТ), дополнительно облучаются и тестикулы в дозе 12 Гр [29–31]. У пациентов с диагнозом «поздний изолированный тестикулярный рецидив В-ОЛЛ» в качестве лечения используется системная химиотерапия. Кроме этого применяется облучение яичек или орхиэктомия пораженного яичка [30, 32]. До сих пор не существует достаточных доказательств в пользу одного метода лечения перед другим. Исследовательская группа AIEOP-BFM пациентам с односторонним тестикулярным рецидивом в качестве метода лечения предлагает одностороннюю орхиэктомию с биопсией контрлатерального яичка, а также проведение лучевой терапии на область тестикул в дозе 15 Гр [30]. Пациентам с двусторонним поражением яичек рекомендуется лучевая терапия в дозе 24 Гр или двусторонняя орхиэктомия [33].
С целью сохранения фертильности у пациентов, достигших пубертатного возраста, показана криоконсервация спермы перед проведением химиолучевого лечения [34].
Далеко не каждый врач сталкивается с подобными заболеваниями в клинической практике из-за их редкости, в связи с чем описание опыта диагностики и лечения поражения яичек при лимфоидных опухолях является важным с научно-практических позиций.
Клиническое наблюдение № 1
Пациент Л. 3 лет заболел в ноябре 2022 г., когда при плановом осмотре у педиатра было выявлено увеличение размеров правого яичка. По месту жительства 23.11.2022 выполнена пункционная биопсия правого яичка. Цитологический состав соответствовал лимфоидной опухоли.
Пациенту выполнена орхофуникулэктомия справа, по данным морфо-иммунологического исследования, проведенного в НИИ детской онкологии и гематологии, операционный материал был представлен фрагментированной тканью яичка, структура субтотально стерта вследствие распространения мономорфного клеточного инфильтрата с диффузным характером роста. Клеточный инфильтрат представлен клетками среднего размера с высоким ядерно-цитоплазматическим соотношением, округлыми ядрами с мелкодисперсным хроматином, среди которого определялись мелкие эозинофильные ядрышки, отмечена высокая митотическая и апоптотическая активность. При иммуногистохимическом исследовании клеточный инфильтрат представлен CD3/TdT/CD44-позитивными Т-лимфоцитами с коэкспрессией CD4, CD8, CD1a, CD5, со слабой коэкспрессией CD45, CD10; реактивный инфильтрат представлен единичными мелкими CD20/PAX-5-позитивными В-лимфоцитами. Уровень экспрессии Ki-67 высокий – до 90–100%. Отсутствовала экспрессия PCK, Vimentin, c-Myc.
По данным УЗИ органов брюшной полости, забрюшинного пространства, малого таза, периферических лимфатических узлов, патологических изменений не выявлено. При УЗИ в правой половине мошонки дополнительные образования не выявлены. В области наружного пахового кольца справа определялось округлое неоднородное гипоэхогенное образование с зонами повышенной эхогенности размером 10х9х10 мм. Образование было расценено как остаточная опухолевая ткань правого семенного канатика. При цветовом допплеровском картировании (ЦДК) по периферии его визуализировались сосуды. Левое яичко определялось в мошонке обычной структуры и нормального размера (13х8х10 мм), головка придатка – 6х5 мм, не изменена.
По результатам позитронно-эмиссионной томографии, совмещенной с компьютерной томографией (ПЭТ/КТ), получены данные о наличии патологической ткани с гиперметаболической активностью 18F-фтордезоксиглюкозы (ФДГ) в области проксимальных отделов семенного канатика справа в узловом образовании в области правой пахово-бедренной области с высокой активностью 18F-ФДГ.
Показатели общего и биохимического анализов крови оставались в пределах референсных значений. Уровень биологической активности опухоли, анализируемый по лактатдегидрогеназе (ЛДГ), был низким (ЛДГ – 350 ЕД/л). В соответствии с протоколом обследования больных с подозрением на лимфоидные опухоли выполнено цитологическое исследование костного мозга (признаков его поражения не было) и ликвора (опухолевые клетки в спинномозговой жидкости не обнаружены).
После проведенного дообследования пациенту установлен клинический диагноз: Т-лимфобластная лимфома с поражением правого яичка. I стадия. Стандартная группа риска. Орхофуникулэктомия справа (ноябрь 2022 г.).
С 26.12.2022 начата программная полихимиотерапия по протоколу ALL-IC BFM 2009 препаратами преднизолон, винкристин, даунорубицин, ПЕГ-аспарагиназа, метотрексат, 6-меркаптопурин, цитарабин, циклофосфамид. На 33-й день терапии, по данным УЗИ, опухолевое образование в области пахового канала справа не определялось. В соответствии с протоколом общая продолжительность лечения составляет 104 нед. Пациент лечение переносит хорошо, признаков раннего рецидива нет.
Клиническое наблюдение № 2
Больной Ш. 5 лет. В начале сентября 2022 г. родители заметили увеличение левой половины мошонки, болезненность при пальпации левого яичка. В анамнезе с рождения гидроцеле слева.
После обращения за медицинской помощью было выполнено оперативное вмешательство в следующем объеме: иссечение гидроцеле слева, ревизия левого яичка, биопсия яичка и придатка левого яичка. По данным цитологического исследования биопсийного материала заподозрено лимфопролиферативное заболевание.
Для дообследования и проведения специального лечения ребенок был направлен в НИИ детской онкологии и гематологии.
По данным УЗИ яички в мошонке. Левое яичко увеличено, 34х20х27 мм (средняя норма – 15х7х9 мм), контуры четкие, паренхима неоднородной эхогенности за счет неправильной формы гипоэхогенных участков и центральной зоны сниженной эхогенности размером 18х21 мм. В нижнем полюсе –
гипоэхогенная округлая зона 7х8 мм. При ЦДК отмечена повышенная васкуляризация гипоэхогенных зон. Головка придатка яичка увеличена, 9х5 мм, однородной средней эхогенности. Семенной канатик несколько утолщен – до 6 мм. Вены гроз-девидного сплетения расширены. Правое яичко в мошонке, размеры нормальные – 16х7х13 мм, паренхима однородная, структура не нарушена. Головка придатка – 6х6 мм, не изменена. В оболочках обоих яичек небольшое количество жидкости, слой до 7 мм.
При проведении ПЭТ/КТ всего тела с 18F-ФДГ получены данные о наличии патологической ткани с гиперметаболической активностью в левом яичке, в мезентериальных лимфоузлах.
По результатам миелограммы, костный мозг в опухолевый процесс не вовлечен, признаков поражения ЦНС не было.
23.11.2022 ребенку выполнено оперативное вмешательство в объеме орхофуникулэктомии слева. При гистологическом исследовании материал представлен фрагментами ткани яичка, структура субтотально стерта вследствие распространения клеточного инфильтрата, который имел нодулярное строение, нодули располагались среди извитых семенных канальцев и были представлены преимущественно крупными клетками с морфологией центробластов, клетки имели скудную амфифильную цитоплазму с нечеткими границами, везикулярные ядра со светлым хроматином и мелкими эозинофильными ядрышками, среди крупных клеток видны немногочисленные мелкие клетки с морфологией центроцитов, в части ядер просматривались мелкие эозинофильные ядрышки. При иммуногистохимическом исследовании клеточный инфильтрат представлен CD20-позитивными В-лимфоцитами с коэкспрессией BCL6, CD10, HGAL, реактивный инфильтрат представлен мелкими CD3/BCL2-позитивными Т-лимфоцитами. Уровень экспрессии Ki-67 высокий – в нодулярных структурах около 80%. Заключение: фолликулярная лимфома, тестикулярный тип.
Таким образом, пациенту был установлен диагноз «фолликулярная лимфома с поражением левого яичка, мезентериальных лимфатических узлов. II стадия. Орхофуникулэктомия слева от 23.11.2022» .
С ноября 2022 по декабрь 2022 г. было проведено 2 курса лечения по программе R-CHOP (ритуксимаб, циклофосфамид, доксорубицин, винкристин, преднизолон; эндолюмбально: метотрексат, цитарабин, преднизолон). С целью оценки эффекта после проведенной терапии выполнена компьютерная томография органов брюшной полости с внутривенным контрастным усилением, по результатам которой признаки прогрессирования основного заболевания в зоне исследования не выявлены. Таким образом, получен полный ответ на противоопухолевое лечение.
С января 2023 по апрель 2023 г. с целью консолидации результата проведено еще 4 курса по программе R-CHOP. По результатам ПЭТ/КТ, данных о наличии опухолевой ткани с гиперметаболической активностью 18F-ФДГ не получены.
В данном наблюдении программное лечение R-CHOP (6 курсов) привело к ранней полной ремиссии фолликулярной лимфомы тестикулярного типа.
Клиническое наблюдение № 3
Больной А. 8 лет. В 2020 г. на основании клинико-лабораторных данных (субфебрилитет, общая слабость, периферическая лимфаденопатия, гепатоспленомегалия, появление бластных клеток в периферической крови, тотального бластоза в миелограмме и иммунофенотипирования бластных клеток) установлен диагноз В-ОЛЛ. Инициально яички поражены не были. Проведенная противоопухолевая лекарственная терапия привела к полной ремиссии, но 08.06.2023 был констатирован комбинированный (костномозговой и тестикулярный) рецидив. При осмотре обращало внимание увеличение мошонки (рис. 1).
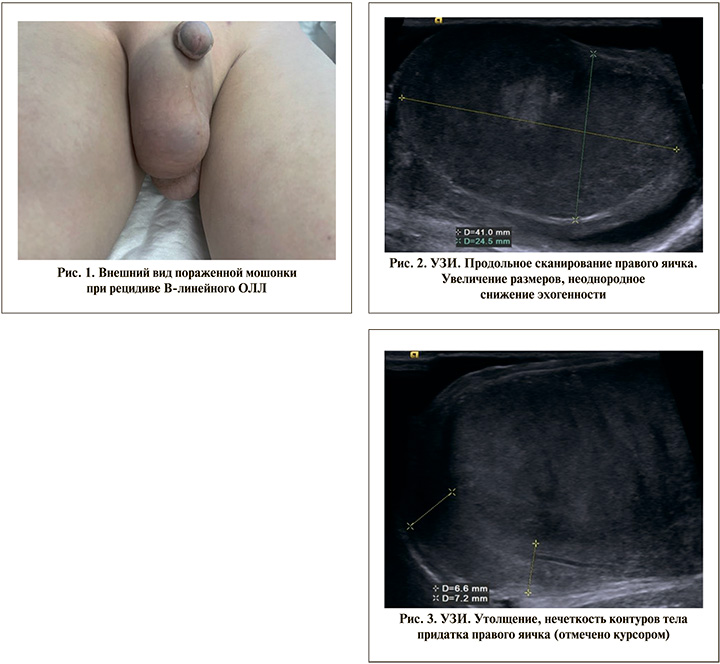
При абдоминальном УЗИ были выявлены выраженная гепатоспленомегалия (КВР правой доли – 216 мм, размер селезенки – 202х60 мм), увеличение количества и размеров (до 27х14 мм) лимфоузлов ворот печени и селезенки, изменение их структуры.
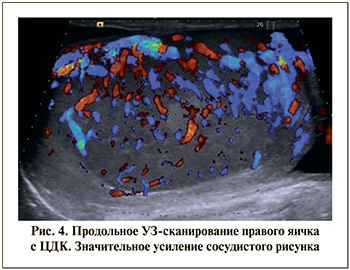
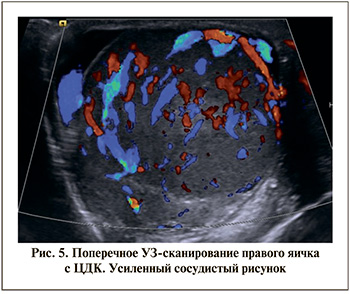
При УЗИ мошонки определялось значительное увеличение обоих яичек: правое – 41х25х30 мм, левое – 44х23х30 мм (средние возрастные размеры – 20х8х15 мм). Эхогенность обоих яичек была диффузно неоднородно снижена (рис. 2). Головка придатка правого яичка четко не дифференцировалась. Тело и хвост придатка были утолщены (рис. 3). В оболочках правого яичка определялось 12 мл жидкости. Головка придатка левого яичка дифференцировалась, была увеличена до 10х7 мм, имела среднюю эхогенность. В оболочках левого яичка определялся незначительный слой жидкости. Васкуляризация обоих яичек была значительно усилена (рис. 4, 5). Поражение обоих яичек подтверждено цитологически.
В общем анализе крови обращало внимание снижение гемоглобина до 78 г/л, эритроцитов до 2,72х1012/л, лейкоцитов до 3,37х109/л, тромбоцитов до 8х109/л. В лейкоцитарной формуле бластные клетки составляли 21%, миелоциты – 4%, сегментоядерные нейтрофилы – 4%, лимфоциты – 71%.
По данным миелограммы от 13.06.2023, тотальная бластная метаплазия костного мозга. Иммунофенотипически бластные клетки были отнесены к В-линейным предшественникам.
Осложнения В-ОЛЛ: гипокоагуляционный синдром, тромбоцитопения, рефрактерная к заместительной терапии тромбоконцентратом, субдуральная гематома, двусторонняя полисегментарная пневмония.
16.06.2023 была начата терапия по противорецидивному протоколу ALL REZ-BFM 2002 препаратами дексаметазон, винкристин, метотрексат. Противоопухолевого эффекта не было, а крайне тяжелое соматическое состояние пациента не позволило применить другие терапевтические опции. Констатировано рефрактерное течение В-ОЛЛ, по решению консилиума врачей 03.07.2023 пациенту присвоен паллиативный статус.
Злокачественные лимфопролиферативные заболевания (лейкозы и неходжкинские лимфомы) очень редко локализуются в яичке. Тестикулярное поражение может быть первым (или единственным) проявлением заболевания, в связи с чем пациенты могут быть направлены к врачу-урологу. Диагностика должна включать комплексное обследование для оценки распространенности опухолевого процесса и определения морфо-иммуногистохимической природы опухоли. Лечебная тактика зависит от варианта злокачественного лимфопролиферативного заболевания и его стадии. Если при I стадии ФЛ проведение орхиэктомии является адекватной и единственной опцией для выздоровления больного, то лимфомы из клеток-предшественников и распространенные стадии В-клеточных лимфом требуют проведения после орхиэктомии системной ПХТ. В случаях поражения яичек при впервые диагностированном ОЛЛ показано проведение системной ПХТ без орхиэктомии, тогда как тестикулярный рецидив ОЛЛ требует проведения орхиэктомии или лучевой терапии на область мошонки с обязательной системной ПХТ и в ряде случаев – трансплантации гемопоэтических стволовых клеток.
С учетом клинического и морфоиммуногистохимического разнообразия злокачественных лимфопролиферативных заболеваний яичка необходима мультидисциплинарная работа врачей-урологов и детских онкологов-гематологов для своевременной диагностики злокачественного процесса на ранних стадиях и назначения современной дифференцированной программной терапии.



