Введение. Рак почки в настоящее время занимает 9-е место по частоте развития среди всех злокачественных новообразований у мужчин и 14-е – у женщин во всем мире [1, 2]. Среди новообразований почки на почечно-клеточный рак (ПКР) приходится 90% всех видов опухолей почки в мире [3]. По данным ракового регистра, в США за последнее десятилетие тенденции роста выявления ПКР стабилизировались с середины 2000 г. по сравнению с ежегодным приростом с уровня 1995 г. на протяжении 10 лет за счет улучшения визуализации и более частого выявления образований почки. Уровень смертности от рака почки с 1995 по 2005 г. с каждым годом имеет тенденцию к падению на 1% в год. Две трети образований почки диагностируются на ранней стадии, для данной категории пациентов 5-летняя относительная выживаемость составляет 93%[4].
 В настоящее время основным радикальным методом лечения рака паренхимы почки считается хирургический. По данным рекомендаций РОУ (Российское общество урологов), EAU (European Association of Urology) и АUА (American urological Association), «золотым» стандартом в лечении ПКР стадии Т1а являются органосохраняющие операции (ОСО), при стадии Т1b и Т2 ОСО выполняются при наличии технической возможности проведения оперативного пособия [5–7]. В текущем десятилетии предпочтение в хирургическом лечении ПКР отдают ОСО [8, 9]. Основанием послужили результаты ряда мировых исследований, где было установлено, что пациенты, подвергшиеся ОСО, имеют лучшие функциональные и онкологические результаты лечения [10]. Успех ОСО напрямую зависит от знания и понимания хирургом топографо-анатомических и патологоанатомических характеристик образований почки на этапе предоперационного планирования и в ходе оперативного вмешательства. В настоящее время выполняемые в предоперационном периоде обследования с помощью визуализирующих методов диагностики: мультиспиральная компьютерная (МСКТ), магнитно-резонансная томографии (МРТ) в режиме 2D, не всегда обеспечивают хирурга полной информацией об области оперативного вмешательства. Для решения данной проблемы в большинстве ведущих урологических клиник мира используется 3D-моделирование и планирование оперативного вмешательства [11–14]. В клинике урологии Первого МГМУ им. И. М. Сеченова метод предоперационного виртуального планирования на основании 3D-моделирования патологического процесса используется с 2009 г. Ранее в клинике проводились исследования по определению эффективности 3D-моделирования при выполнении оперативных вмешательств в отношении пациентов с ПКР из открытого доступа [15]. В настоящее время при выборе операционного доступа предпочтение отдается высокотехнологичным видам оперативных пособий-лапароскопическому и робот-ассистированному [16, 17].
В настоящее время основным радикальным методом лечения рака паренхимы почки считается хирургический. По данным рекомендаций РОУ (Российское общество урологов), EAU (European Association of Urology) и АUА (American urological Association), «золотым» стандартом в лечении ПКР стадии Т1а являются органосохраняющие операции (ОСО), при стадии Т1b и Т2 ОСО выполняются при наличии технической возможности проведения оперативного пособия [5–7]. В текущем десятилетии предпочтение в хирургическом лечении ПКР отдают ОСО [8, 9]. Основанием послужили результаты ряда мировых исследований, где было установлено, что пациенты, подвергшиеся ОСО, имеют лучшие функциональные и онкологические результаты лечения [10]. Успех ОСО напрямую зависит от знания и понимания хирургом топографо-анатомических и патологоанатомических характеристик образований почки на этапе предоперационного планирования и в ходе оперативного вмешательства. В настоящее время выполняемые в предоперационном периоде обследования с помощью визуализирующих методов диагностики: мультиспиральная компьютерная (МСКТ), магнитно-резонансная томографии (МРТ) в режиме 2D, не всегда обеспечивают хирурга полной информацией об области оперативного вмешательства. Для решения данной проблемы в большинстве ведущих урологических клиник мира используется 3D-моделирование и планирование оперативного вмешательства [11–14]. В клинике урологии Первого МГМУ им. И. М. Сеченова метод предоперационного виртуального планирования на основании 3D-моделирования патологического процесса используется с 2009 г. Ранее в клинике проводились исследования по определению эффективности 3D-моделирования при выполнении оперативных вмешательств в отношении пациентов с ПКР из открытого доступа [15]. В настоящее время при выборе операционного доступа предпочтение отдается высокотехнологичным видам оперативных пособий-лапароскопическому и робот-ассистированному [16, 17].
Цель исследования: оценить эффективность и преимущества использования 3D-планирования и виртуального осуществления операций при хирургическом лечении пациентов с локализованным раком паренхимы почки из лапароскопического доступа.

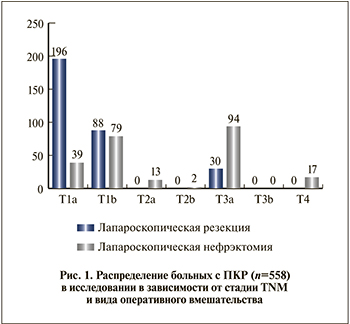
Материалы и методы. В ретроспективный анализ включены данные 558 пациентов с ПКР, подвергнутых хирургическому лечению в клинике урологии Первого МГМУ им. И. М. Сеченова с января 2012 по май 2017 г. В 244 (43,7%) наблюдениях выполнялась лапароскопическая радикальная нефрэктомия (ЛРН), в 314 (56,3%) – лапароскопическая резекция почки (ЛРП) (рис. 1).
Средний возраст больных составил 55,85±10,5 (25–78) лет. Мужчин было 307 (55%), женщин – 251(45%). Всем пациентам в предоперационном периоде проведены стандартные физикальное и инструментальное обследования. Из дополнительных методов обследования 248 (44,4%) больным на основании данных МСКТ проведено 3D-моделирование и виртуальное осуществление операций при помощи программы 3D-моделирования «Amira». Распределение больных в зависимости от стадии TNM и вида оперативного вмешательства представлено в табл. 1.
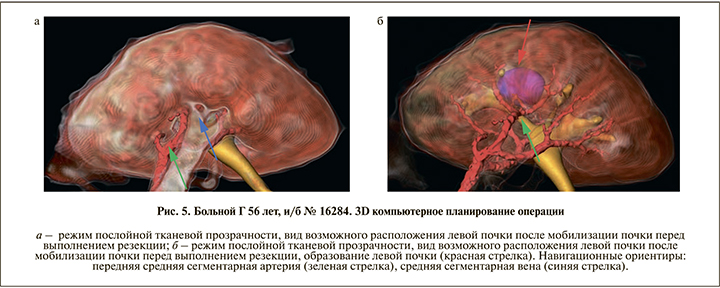
Виртуальное планирование и осуществление операций выполнялись на основании алгоритма, разработанного в нашей клинике (рис. 2).

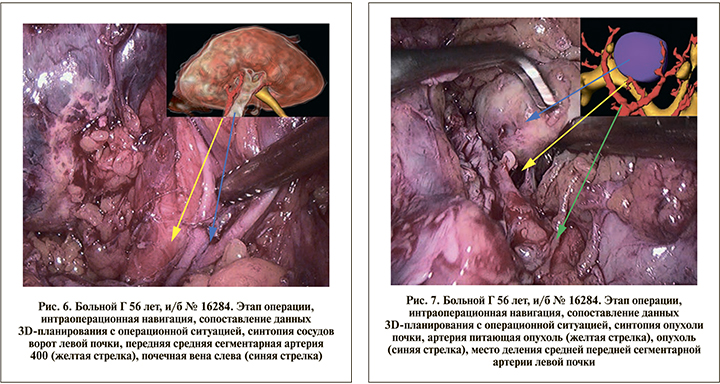
Виртуальное осуществление оперативных вмешательств по алгоритму выполнялось хирургом накануне оперативного вмешательства, а также с целью навигации на этапе проведения операции в самой операционной с использованием ноутбука, на котором хирурги имели возможность сопоставлять данные предоперационного виртуального планирования и реальной операционной картины (рис. 3–7).
В связи с тем что на результаты операций влияют много разных факторов, статистический анализ проводили, используя парный метод сравнения. Из каждой группы больных с выполненным 3D-планированием и без него были подобраны сопоставимые пары по основным признакам: однородность операторов и их опыт при выполнении операции, размер и локализация опухоли (отношение к сегменту, передней и задней поверхности), вариант хирургического доступа. По итогам было сформировано по две однородные подгруппы больных: группы с ЛРН (по 22 человека) и ЛРП (по 53 человека), которым 3D-планирование проводилось и нет (табл. 2, 3).
Операции были выполнены 7 урологами клиники с большим опытом проведения лапароскопических пособий. Этапы всех операций были стандартными для ЛРН и ЛРП.
Статистическая обработка полученных данных выполнялась при помощи компьютерной программы IBM SPSS, версии 22.0.
Проверка распределения значений переменных в группах наблюдения проводилась с использованием критериев Шапиро–Уилкса и Колмогорова–Смирнова.
При подтверждении нормального распределения количественных переменных в исследуемых группах проверку статистической значимости различий проводили при помощи t-критерия Стьюдента для независимых выборок. Для оценки различий, полученных при изучении динамики нормально распределенных переменных, использовался t-критерий для связанных выборок.
Для парных межгрупповых сравнений количественных переменных в отсутствие нормального распределения использовали непараметрический ранговый критерий Манна–Уитни. Для оценки различий в динамике переменных в отсутствие нормального распределения применялся непараметрический критерий Вилкоксона.

Статистическую значимость различий категориальных и порядковых признаков при парных сравнениях оценивали при помощи критерия χ2 Пирсона с поправкой на непрерывность. При ожидаемой частоте встречаемости признака 5 и менее в четырехпольных таблицах использовался точный критерий Фишера.
Различия между группами наблюдения считали статистически значимыми при р<0,05.
Построение логистической регрессионной модели осуществлено в одно- и многофакторном форматах методами принудительного и пошагового включения прогностических факторов с определением минимального набора предикторов с оценкой значения коэффициента детерминации (R2 Нэйджелкерка), показывающего долю влияния всех предикторов модели на дисперсию зависимой переменной.

Проверка статистической значимости модели осуществлена при помощи критерия χ2. При значении р<0,05 нулевая гипотеза о незначимости модели отвергалась. Соответствие модели использованным данным характеризовали с помощью критерия согласия Хосмера–Лемешева. При р>0,05 принималась гипотеза о согласованности модели.
Интерпретация параметров логистического регресса произведена на основе величины exp(b). Положительный коэффициент b и значение exp(b) больше 1 указывают, что шансы наступления прогнозируемого события возрастают. Отрицательный коэффициент b и величина exp(b)<1 свидетельствуют о снижении шансов. Для отношений шансов рассчитаны 95% доверительных интервалов. Показатель оценивали как статистически значимый, если в доверительный интервал не входила единица.
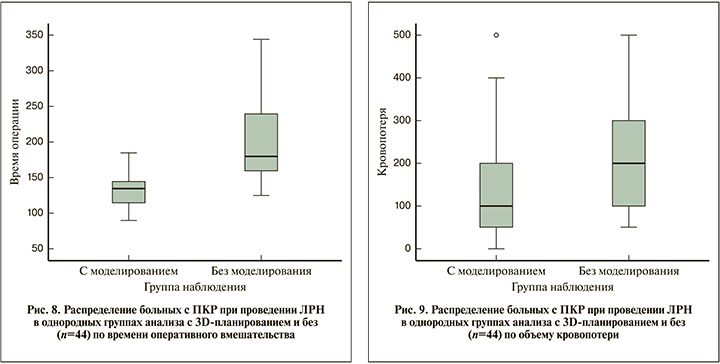
Результаты. Все пациенты в однородных группах сравнения с ЛРН (n=44) были прооперированы из трансперитонеального доступа. При сравнении однородных подгрупп пациентов, перенесших ЛРН, по медиане времени выполнения в подгруппе с 3D-планированием операций среднее время операци составило 135,2±27,2 мин, что было меньше, чем в подгруппе без 3D-планирования, где средняя продолжительность вмешательства равнялась 202,9±55,5 мин (р=0,0001) (рис. 8).
Также было получено статистически значимое различие по медиане кровопотери, которая в подгруппе пациентов с 3D-планированием составила 143,2±137,4 мл, что значительно меньше, чем в группе больных без 3D-планирования 472,0±395,4 мл (р=0,001) (рис. 9).
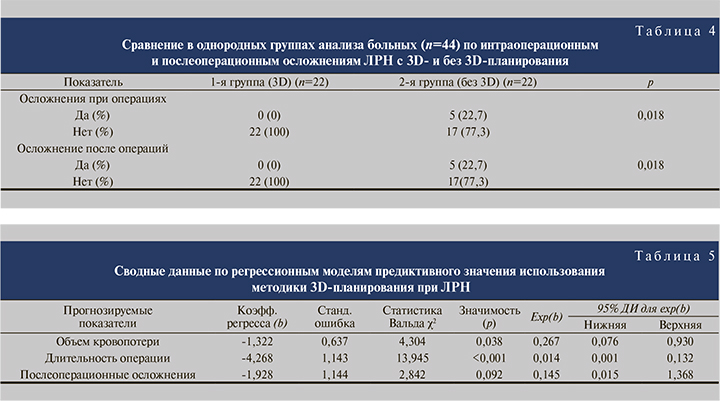
Гемотрансфузии из 44 больных подгрупп сравнения потребовались 4 (9,1%) больным, причем все они были из подгруппы больных без 3D-планирования (р=0,042). Конверсия потребовалась 3 (13,6%) пациентам подгруппы без 3D-планирования (р=0,11). Ручное асисстирование выполнено в 1 (4,5%) случае также пациентам подгруппы без 3D-планирования (р=0,62) Интраоперационные осложнения при проведении ЛРН в однородных подгруппах были зафиксированы у 5 (11,4%) больных, причем все из подгруппы больных без 3D-планирования (р=0,018). Послеоперационные осложнения также имели место только в подгруппе без 3D-планирования – 5 (11,4%) пациентов (р=0,018). Осложнения соответствовали III и IV степеням по классификации осложнений «Clavien–Dindo» (табл. 4).
При построении однофакторных регрессионных моделей, отражающих прогностическое значение использования методики 3D-планирования при выполнении ЛРН (n=44), в качестве прогнозируемых показателей рассматривались объем кровопотери во время операции более 100 мл, общая длительность оперативного вмешательства более 150 мин, наличие послеоперационных осложнений (табл. 5).
Отмечается статистическая значимость использования 3D-планирования как прогностического фактора снижения кровопотери менее 100 мл (65,9% корректных предсказаний), сокращения объема операции до 2,5 ч и менее (86,6% корректных предсказаний). В отношении послеоперационных осложнений статистически значимая прогностическая регрессионная модель не была получена в связи с их малым количеством.
Среди больных, которым была проведена операция в объеме ЛРП (n=106), ретроперитонеоскопический доступ использован в 8 (7,5%) случаях, трансперитонеальный – в 98 (92,5%). Данные основных результатов операций при статистическом анализе приведены в табл. 6.

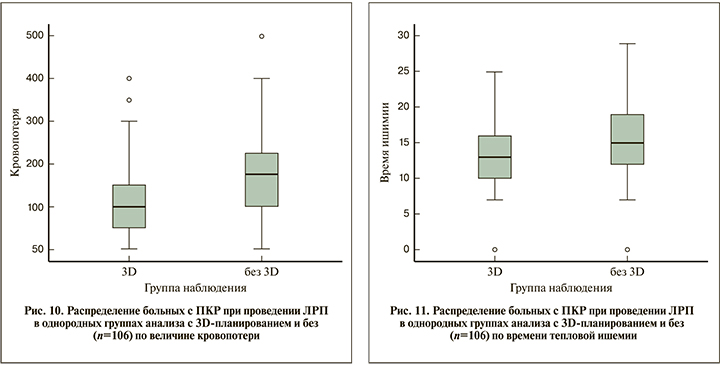
Как видно из табл. 6, в подгруппах парного анализа выявлено статистически значимое различие по средней продолжительности операции (р=0,0001) Кроме того, пациентов, на операцию которых было затрачено ≤120 мин, в подгруппе с 3D-планированием было больше, чем в подгруппе без, а в группе без 3D-планирования – 28 (42,8%) и 17 (32,1%) человек соответственно (р=0,031). По результатам интраоперационной кровопотери различие между группами больных было статистически значимым и наглядно продемонстрировано на рис. 10.
При сравнении по времени тепловой ишемии также выявлено статистически значимое различие: для больных группы с 3D-планированием 12,0±6,4 и 15,6±5,7 мин в группе больных парного анализа без 3D-планирования (рис. 11).

Интраоперационные осложнения при проведении ЛРП отмечены у 4 (7,6%) пациентов подгруппы без 3D-планирования (p=0,039). Послеоперационные осложнения возникли у 1 (1,9%) и 3 (5,7%) пациентов подгруппы с и без 3D-планирования соответственно (табл. 7).
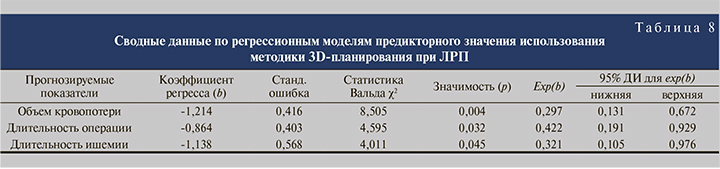
При построении однофакторных регрессионных моделей с целью определения предикторного значения использования методики 3D-моделирования при выполнении ЛРП в качестве прогнозируемых показателей рассматривались объем кровопотери во время операции более 100 мл, общая длительность оперативного вмешательства более 120 мин, длительность ишемии почки более 20 мин (табл. 8).
Отмечается статистическая значимость использования 3D-планирования как прогностического фактора снижения кровопотери менее 100 мл (64,2% корректных предсказаний), сокращения объема операции менее 2 ч (60,4% корректных предсказаний) и уменьшения длительности ишемии менее 20 мин (83% корректных предсказаний).
Обсуждение. Хирургическое лечение пациентов ПКР с использованием лапароскопических доступов при выполнении ЛРН и ЛРП относится к категории сложных оперативных вмешательств. Освоение хирургической техники данного вида оперативных доступов характеризуется высокой кривой обучения [18]. На этапе освоения, согласно мировым данным, уровень конверсий операций в открытый доступ достигает 13,6% [19]. Точное знание и понимание нормальной и патологической топографической анатомии области планируемого оперативного вмешательства служат значимым фактором достижения положительного результата выполняемого хирургического пособия. Использование в повседневной практике стандартных 2D-данных предоперационного обследования, полученных на основании выполняемой МСКТ с контрастированием, не всегда в полной мере позволяет хирургу иметь полное представление об области хирургических интересов. В урологии использование 3D-планирования и виртуального осуществления операций пациентам с ПКР, по данным мировых исследователей, представлено несколькими работами [12–14, 20–26]. В заключении данных работ авторы отмечают положительный эффект от использования компьютер-асисстированных технологий при выполнении оперативных вмешательств в отношении пациентов с ПКР. Одним из недостатков большинства данных работ, по мнению авторов, служит малое число наблюдений и отсутствие сравнения с разделением на группы больных с использованием виртуального планирования и без него. Результаты небольшого числа работ, в которых анализ проведен на выборках с большим числом пациентов и разделением их в зависимости от использования 3D-планирования, неоднозначны. В нашей клинике ранее была проведена работа Д. Н. Фиева, в которой было доказано статистически значимое преимущество при использовании 3D-технологий при анализе разделенных на равные группы 105 пациентов ПКР с выполненными органосохраняющими операциями из открытого доступа. По величине интраоперационной кровопотери, по показателям времени тепловой ишемии и времени операции различия были статистически незначимыми, хотя авторы отмечают, что у больных с уровнем нефрометрического индекса «RENAL» более 8 баллов данные различия были статистически значимыми [26]. Схожие результаты были получены Wang et al. (2017), проанализировавших результаты оперативного лечения 94 пациентов с ПКР в объеме ЛРП. В первой группе (n=49) проведено 3D-моделирование и виртуальное планирование, во второй (n=45) планирование и выполнение операций осуществляли только на основании данных МСКТ с контрастированием. При сравнении результатов оперативного лечения по времени операции, времени тепловой ишемии и величины интраоперационной кровопотери авторы не отметили статистически значимых различий. При последующем разделении пациентов в зависимости от величины индекса RENAL (меньше и больше 8 баллов) выявлено статистически значимое преимущество пациентов с 3D-планированием и показателем RENAL более 8 баллов только по продолжительности оперативного вмешательства. Авторы связывают уменьшение времени операции с лучшим знанием анатомии области оперативного вмешательства [25]. В нашей работе для более корректного статистического сравнения был использован парный анализ, для которого были сформированы одинаковые пары пациентов как по морфометрическим показателям опухолевого процесса, так и по хирургам, выполняющим пособия с учетом их хирургического опыта в разные годы. В результате по всем основным показателям операций было получено статистически значимое преимущество для пациентов, которым было проведено 3D-планирование и виртуальное осуществление операций в предоперационном периоде, прооперированных в объеме ЛРН и ЛРП. Наши результаты показывают, что влияние использования 3D-планирования и виртуального осуществления операций невозможно установить при простом сравнении групп больных без учета множества факторов, которые при анализе могут сильно влиять на конечный результат статистического анализа.
Несмотря на положительные результаты, наша работа также имела ряд ограничений. Наше исследование выполнено ретроспективно в рамках одной клиники с общим количеством 150 пациентов. Для выявления всех преимуществ и недостатков использования 3D-технологий требуется проведение рандомизированного многоцентрового исследования с большим числом наблюдений.
Заключение. Применение компьютер-асисстированных технологий в объеме 3D-планирования и виртуального осуществления операций позволяет улучшать непосредственные результаты оперативных пособий у пациентов с ПКР при выполнении органосохраняющих и органоуносящих операций из лапароскопического доступа.



