Киста предстательной железы (КПЖ) – это полое инкапсулированное, в подавляющем большинстве случаев доброкачественное образование в ткани железы или простатвезикулярного комплекса, заполненное жидкостным компонентом и способное вызывать нарушения мочеиспускания. Лечение КПЖ остается актуальной проблемой современной урологии. Кисты ПЖ являются редким заболеванием, составляя в структуре всех доброкачественных новообразований урогенитального тракта от 7,0 до 8,6% [1]. Поскольку наиболее часто КПЖ диагностируют у людей трудоспособного возраста, разработка и совершенствование имеющихся высокотехнологичных методов лечения КПЖ остаются первостепенной задачей ведущих урологических клиник.
Симптомы КПЖ включают гематоспермию, боль при эякуляции, обструктивные симптомы мочеиспускания, инфекцию мочевыводящих путей. Кисты ПЖ могут быть причиной рецидивирующего эпидидимита и недержания мочи, а также мужского бесплодия. Нередко они ассоциированы с различными аномалиями мочеполовой системы, включая гипоспадию, крипторхизм и ипсилатеральную агенезию почек [2]. На выраженность симптомов влияют такие факторы, как локализация кист, их размеры и наличие перстистенции инфекционного агента. Однако следует отметить, что в большинстве случаев КПЖ не имеют ярковыраженной клинической картины и чаще всего являются случайной находкой при инструментальном обследовании.
Классификация. Клиническая картина
Существует несколько вариантов классификаций КПЖ, которые отражают анатомо-топографические особенности, позволяя подобрать оптимальный вид оперативного лечения. В 2008 г. R Nayyar et al. была предложена классификация, согласно которой все кисты были разделены на три группы [3]: 1 – срединная киста, не сообщающаяся с уретрой (традиционная киста простатической маточки); 2а – срединная киста, имеющая сообщение с мочеиспускательным каналом (кистозное расширение простатической маточки); 2b – кистозное расширение простатической маточки, сообщающееся с семявыносящими путями; 3 – кистозное расширение семявыбрасывающего протока.
В 2009 г. A. Galosi и R. Montironi опубликовали работу, в которой представили новую расширенную классификацию КПЖ [4]:
1. Срединные кисты: a – киста простатической маточки (ранее именовавшаяся кистой Мюллерова протока), расположена по средней линии выше уровня семенного бугорка; b – кистозная дилатация простатической маточки, имеет гистологически подтвержденное сообщение с уретрой, но не определяется при трансректальном УЗИ (ТРУЗИ); с – увеличенная простатическая маточка (остаток Мюллерова протока, или мужское влагалище [vagina masculinus]), является врожденной патологией, при которой может отсутствовать семенной бугорок, но из-за широкого входного отверстия в просвет мочеиспускательного канала его нельзя отнести к КПЖ. Данное заболевание нередко ассоциировано с другими пороками развития, например с гипоспадией.
2. Кисты семявыбрасывающего (эякуляторного) протока.
3. Паренхиматозные кисты, которые в свою очередь разделяют на: а –простые кисты и b – множественные кисты: I – протоковая эктазия (микрокисты), II – небольшой кистозный узелок, III – большой кистозный узелок.
4. Осложненные кисты: а – инфекционные, b – геморрагические.
5. Кистозная опухоль: а – кистозная карцинома, b – цистаденома, c – цисткарцинома, d – дермоидная киста.
6. Вторичные кисты по отношению к другим заболеваниям: бильгарциоз и эхинококкоз.
R. Furuya et al. в 2017 г. представили свою классификацию КПЖ [5]:
1. Паренхиматозные кисты: a – срединные, b – парамедианные, c – латеральные.
2. Внепростатические кисты: a – киста семенных пузырьков, b – киста семявыносящего протока, c – киста Куперового протока.
Все КПЖ в зависимости от их топографического расположения делятся на внутрипростатические и внепростатические. По происхождению кисты разделяют на врожденные и приобретенные. Срединные, или медианные, КПЖ расположены по средней линии, позади верхней половины простатического отдела уретры. Они включают кисты простатической маточки и кисты Мюллерова протока (рис. 1).

Кисты простатической маточки возникают вследствие внутриутробной дилатации простатической маточки и сообщаются с задней уретрой. Обычно они обнаруживаются на 1–2-м десятилетии жизни. Размеры их невелики и обычно составляют 8–10 мм (рис. 2). Содержимое этих кист имеет белый или коричневый цвет, в его состав входят сперматозоиды (цитологический маркер кист простатической маточки). Сообщается, что они встречаются примерно у 1–5 % населения [6, 7]. Кисты простатической маточки ассоциированы с различными врожденными аномалиями мочеполовой системы, включая гипоспадию, крипторхизм и ипсилатеральную агенезию почек [7, 8]. Данные кисты имеют вариабельную клиническую картину, включая инфекцию мочевыводящих путей, боль, постмикционное недержание мочи, рецидивирующий эпидидимит и гематоспермию [6]. Поскольку кисты простатической маточки сообщаются с уретрой, они могут обусловливать подтекание мочи после микции. Кисты ПЖ могут инфицироваться и содержать гной или кровь, что вызывает сложности при визуализации, поскольку внешне они похожи на абсцесс и кистозные опухоли простаты [9].
Кисты Мюллерова протока развиваются из остатков парамезонефрального (Мюллерова) протока при неполной его редукции на 3-м месяце внутриутробной жизни. Кисты Мюллерова протока связаны с семенным бугорком с помощью стебелька, однако с уретрой сообщения не имеют (рис. 3). Эти кисты чаще проявляются на 2–4-м десятилетиях жизни, однако имеются данные о нескольких случаях заболевания в младенчестве [10]. По результатам проведенных аутопсий, распространенность заболевания среди мужчин составляет около 1%, однако данные могут быть занижены. Так, некоторые авторы сообщают, что распространенность кист Мюллерова протока может достигать 5% [9]. Кисты Мюллерова протока обычно протекают бессимптомно, но могут проявляться в зрелом возрасте задержкой мочеиспускания и инфекцией мочевыводящих путей [11]. Они также могут вызывать нарушение эякуляции из-за обструкции семявыбрасывающего протока по средней линии. Как и кисты простатической маточки, кисты Мюллерова протока могут инфицироваться; при визуализации они напоминают абсцессы или кистозные опухоли ПЖ [12]. Описаны случаи наличия в кистах простатической маточки и кистах Мюллерова протока карциномы ПЖ [12]. Содержимое их имеет коричневый или зеленый цвет, серозную или мукозную консистенцию, обычно неоднородное за счет мелких конкрементов, примеси крови или гноя и лишено сперматозоидов. В таблице представлена сравнительная характеристика кист простатической маточки и кист Мюллерова протока [7].


Кисты семявыбрасывающего протока расположены латерально (парамедианно), близко к срединной линии и кзади от простатического отдела уретры (рис. 4). Кисты семявыбрасывающего протока встречаются редко и формируются вследствие врожденной или приобретенной обструкции семявыбрасывающего протока [13]. Обструкция семявыбрасывающего протока – одна из основных причин мужского фактора бесплодия. В анализе эякулята у этих пациентов отмечается преимущественно олигос- или азооспермия, а также гематоспермия. Однако, несмотря на патоспермию, у данной группы пациентов обычно нормальные результаты физикального обследования, уровень гонадотропинов в сыворотке крови в референтных пределах. При аспирации кисты семявыбрасывающего протока могут содержать фруктозу или сперматозоиды, нередко камни, а иногда гной или кровь. Описаны случаи возникновения кистозной дилатации ипсилатерального семенного пузырька [14].
Латеральные КПЖ расположены на некотором расстоянии от средней линии и могут поражать любую зону простаты. Они включают ретенционные, дегенеративные кисты и кисты, связанные с опухолями.
Патогенез ретенционных КПЖ неясен, однако известно, что они ассоциированы с возрастом и наблюдаются у пациентов с доброкачественной гиперплазией предстательной железы (ДГПЖ). Установлено, что у пациентов с бесплодием они встречаются чаще, чем у фертильных пациентов [8]. Ретенционные КПЖ возникают в результате расширения ацинусов желез из-за приобретенной обструкции протоков, в результате чего образуются кисты диаметром 1–2 см, содержащие прозрачную жидкость. Эти кисты встречаются часто, возникают на 5–6-м десятилетии жизни и редко бывают симптоматическими [9]. Ретенционные КПЖ представляют собой однокамерные кисты с гладкими стенками обычно круглой формы, которые могут возникать в любой зоне ПЖ. По внешнему виду они идентичны кистам, связанным с ДГПЖ. Диагноз основывается на расположении кист в периферической зоне или в отсутствие других доказательств ДГПЖ [9].
Дегенеративные КПЖ составляет большинство кистозных поражений ПЖ. Они располагаются в переходной зоне простаты вместе с узелками ДГПЖ. Данные кисты имеют неправильную форму и вариабельные размеры, также могут содержать кровь или конкременты. Пациенты с этими кистами обычно имеют симптомы обструкции мочевыводящих путей из-за гиперплазии ПЖ (рис. 5) [5].
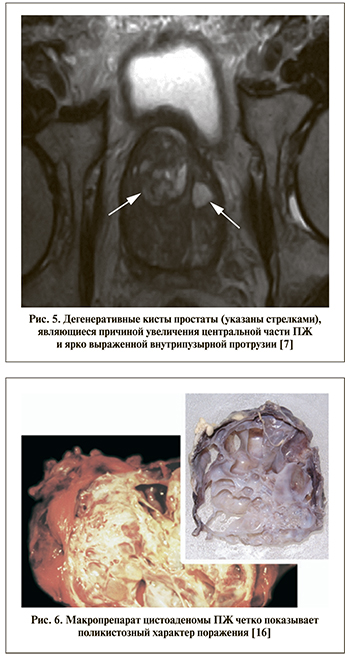
Кисты, связанные с опухолями, – это доброкачественные или злокачественные новообразования ПЖ, которые содержат кистозные компоненты. Цистаденома – редкая доброкачественная опухоль, состоящая из кист, выстланных простым столбчатым эпителием с хронически воспаленной рыхлой фиброзной или фиброзно-мышечной стромой, нередко может достигать больших размеров (рис. 6) [16]. Кистозная карцинома ПЖ представляет собой преимущественно кистозную массу с узловатыми стенками, при этом твердые компоненты стенки являются новообразованием [17, 18]. Магнитно-резонансная томография (МРТ) в режиме Т2-взвешенного изображения позволяет отображать кистозное содержимое и оценивать степень поражения. Патогенез кистозной карциномы ПЖ может быть связан либо с псевдокистой из-за центрального некроза или кровоизлияния в злокачественном очаге, либо со злокачественным перерождением ретенционной кисты. Большинство зарегистрированных кистозных карцином представляют собой псевдокисты с кровоизлиянием в полость; только 17% из них возникли из-за перерождения ретенционных кист [18]. При кистозных поражениях ПЖ наличие крови должно вызывать подозрение на злокачественное новообразование. Другие опухоли ПЖ, которые могут проявляться кистозным поражением, включают аденокарциному папиллярной кисты и комбинированную аденокарциному переходных клеток. В редких случаях кистозные элементы имеют лейомиома и липосаркома простаты. На МР-томограмме неоднородная интенсивность сигнала кистозных компонентов и наличие мягких тканей указывают на неопластическую причину.
Внепростатические кисты возникают вне ПЖ из близлежащих структур – семенных пузырьков, семявыносящих протоков и протоков Купера.
Кисты семенных пузырьков могут быть врожденными и приобретенными. Обычно они обнаруживаются у пациентов в возрасте от 10 до 40 лет [19, 20]. Врожденные кисты семенных пузырьков можно подразделить на изолированные кисты, кисты, связанные с аномалиями верхних мочевыводящих путей, и кисты, связанные с аутосомно-доминантной поликистозной болезнью почек [20]. Зарегистрировано несколько случаев кист семенных пузырьков, большинство из которых ассоциировано с ипсилатеральной агенезией почек и входят в триаду симптомов Циннера [1, 21].
Кисты семенных пузырьков, как правило, имеют небольшие размеры (<5 см) и либо бессимптомны, либо проявляются ирритативными симптомами и инфекционной персистенцией. Большие кисты (>8–10 см) встречаются реже и могут проявляться симптоматической обструкцией мочевого пузыря или кишечника [1, 20]. Пациенты с кистами семенных пузырьков также могут иметь симптомы хронического рецидивирующего простатита и рецидивирующего эпидидимита, болезненную эякуляцию, выделения из уретры, ургентность, гематурию, острую задержку мочеиспускания, боль при дефекации, тенезмы, запоры, дискомфорт в области таза, боль в промежности или яичках, образование в брюшной полости или малом тазу, бесплодие или гематоспермию [22].
Кисты семявыносящего протока расположены по ходу семявыносящего протока и выше ПЖ. Врожденные аномалии семявыносящего протока – наиболее частая находка у мужчин с азооспермией и малым объемом эякулята [14]. Инфекция, непроходимость и неоплазия – возможные причины приобретенных кист семявыносящего протока.
Протоки железы Купера впадают в бульбозные отделы уретры. Обструкция этих протоков может вызывать образование ретенционных кист. Кисты протока Купера могут быть врожденными и приобретенными. Большинство из этих кист протекает бессимптомно, однако кисты большего размера могут стать причиной гематурии или непроходимости мочевыводящих путей и, возможно, мужского бесплодия [12]. Сообщалось о нескольких случаях внутриутробной и ранней послеродовой смерти в результате непроходимости мочевыводящих путей из-за больших кист протока Купера. У взрослых приобретенные кисты протока Купера возникают в результате инфекции или травмы [8].
Лечение
В настоящее время в мировой литературе программных исследований, посвященных сравнению методов лечения КПЖ, практически нет. Имеющиеся работы по данной теме носят характер клинических наблюдений, в которых описаны различные методики выполнения разных по объему оперативных вмешательств. В отечественной литературе по данной теме имеется ограниченное число публикаций, особенно касающихся эндохирургии КПЖ.
Одно из первых упоминаний трансуретрального эндоскопического вмешательства по поводу КПЖ в мировой литературе датируется 1987 г. Японские врачи H. Takatera, H. Sugao и T. Sakurai описали клиническое наблюдение КПЖ у мужчины 51 года, обратившегося в больницу с жалобами на дискомфорт в промежности, периодические эпизоды макрогематурии и уменьшение объема эякулята [23]. При УЗИ была выявлена интрапростатическая киста, в связи с чем выполнена ее трансуретральная инцизия. По данным УЗИ, проведенного через 4 мес. после операции, остаточная КПЖ не определялась, симптомы разрешились в течение 3 мес. A. Six et al. в 1989 г. описали три случая КПЖ у мужчин, имевших обструктивные симптомы мочеиспускания, которым была выполнена трансуретральная эндоскопическая резекция передней стенки кисты, обеспечившая адекватное дренирование полости последней [24]. В 1990 г. J. V. Rodriguez и E. Ruiz-Castane провели исследование, в которое были включены 12 пациентов с кистой простатической маточки, 6 из которых обратились за консультацией по поводу бесплодия [25]. Трансуретральная резекция капсулы простатической маточки во всех случаях устранила дистальную непроходимость семенного протока, в половине случаев увеличилась подвижность и концентрация сперматозоидов в эякуляте. Успешное эндоскопическое лечение ретенционной КПЖ также описано в работе M. Tamaki et al. в 1994 г. [26].
Преимущество интраоперационного использования сонографии и рентгеноскопии при трансуретральной инцизии КПЖ было продемонстрированно в работе T. Manohar в 2008 г. [27]. C 1997 по 2005 г. 25 пациентам, имевшим расстройства эякуляции, включая гематоспермию, выполнена трансуретральная инцизия эякуляторных протоков под трансректальным УЗ-наведением и рентгеновским контролем. Улучшение симптоматики отмечено у 96% пациентов с нарушением эякуляции. Все пациенты с болезненной эякуляцией и гематоспермией отметили полное исчезновение симптомов в течение 3 мес. после операции; у 3 пациентов развился транзиторный орхоэпидидимит, купированный консервативно. Ни у одного из пациентов не было отмечено ретроградной эякуляции или недержания мочи. Развитие у 51-летнего мужчины гематоспермии, вызванной КПЖ и обструкцией семявыбрасывающих протоков, описали японские ученые H. Fuse и R. Nishio в 2003 г. [28]. Стенку кисты рассекли уретротомом, полость кисты была заполнена кровянистым содержимым, внутри кисты определились два отверстия эякуляторных протоков. Интра- и послеоперационных осложнений отмечено не было. Через 1 мес. после выполнения оперативного вмешательства гематоспермия полностью купировалась, в течение 7 мес. наблюдения рецидивов выявлено не было.
Одной из первых работ, сравнивавших эффективность эндоскопических методов лечения КПЖ, было исследование Xiong-Bing Zu et al., опубликованное в 2009 г. [29]. Авторы ретроспективно проанализировали клинические данные девяти пациентов с КПЖ, пять из которых проявлялись частым и ургентным мочеиспусканием, трое – затрудненным мочеиспусканием вялой струей мочи и один – гематоспермией. Трансуретральная инцизия стенки была выполнена трем пациентам с небольшим объемом кист, расположенных рядом с простатическим отделом уретры, а шести, имевшим кисты большего объема с локализацией позади от простатического отдела уретры, выполнено лапароскопическое иссечение последних. Длительность трансуретрального удаления КПЖ составила от 30 до 50 мин, кровопотеря во время операции – 20–70 мл. При лапароскопическом доступе показатели составили 100–150 мин и 30–50 мл соответственно. Все пациенты находились под наблюдением на протяжении 3–12 мес., в течение которых не было отмечено проблем с эректильной функцией и эякуляцией, отсутствовала обструктивная и ирритативная симптоматика. Авторы пришли к выводу, согласно которому для КПЖ небольшого размера, расположенных близко к простатической части уретры, предпочтительным оперативным методом является трансуретральная инцизия. Лапароскопическая эксцизия КПЖ благодаря своей безо-пасности, эффективности, минимальной инвазивности, небольшому количеству осложнений и быстрому восстановлению может быть использована в качестве метода первой линии лечения больших КПЖ. Похожий сравнительный анализ провели Xiang-zhou Sun et al., ими была проанализированы истории болезни 48 пациентов с кистой Мюллерова протока и сопоставлены методы диагностики (ТРУЗИ и МРТ) и лечения [30]. Семерым пациентам была выполнена трансперинеальная пункция кисты под УЗ-наведением с последующей аспирацией содержимого полости кисты. Одному пациенту с большой кистой Мюллерова протока выполнено открытое оперативное вмешательство и еще одному – лапароскопическое удаление кисты. В 39 наблюдениях при кистах небольших размеров выполнена трансуретральная инцизия. Всем пациентам проведено ТРУЗИ предстательной железы через 3 мес. после операции, рецидива кист выявлено не было. В течение 6 мес. после оперативного вмешательства 10 из 39 пациентов с обструктивной азооспермией зачали детей. У 9 из 29 пациентов в анализе эякулята были обнаружены сперматозоиды, у одного 19-летнего пациента были купированы симптомы хронической тазовой боли. По результатам данного исследования, показано, что больные с кистой Мюллерова протока чаще всего предъявляли жалобы на бесплодие, вызванное обструктивной азооспермией, а также на хроническую тазовую боль. Трансректальное УЗИ предстательной железы является предпочтительным методом обследования при кистах Мюллерова протока, а МРТ малого таза может дать более точную информацию о локализации и размерах кист. Авторы отметили, что трансуретральный доступ является наиболее эффективным методом лечения кист Мюллерова протока, лапароскопическая резекция кисты может являться методом выбора при кистах больших размеров.
Несмотря на внедрение эндоскопических методов лечения КПЖ, все еще остается место для открытой хирургии. В 2009 г. группа индийских урологов описала успешное открытое оперативное вмешательство, выполненное 13-летнему пациенту с большой КПЖ (11,5×4,4 см), которая вызывала жжение при мочеиспускании и подкапывание мочи после микции [31]. Полное иссечение кисты проведено через задний сагиттальный доступ с боковой мобилизацией прямой кишки. Осложнений во время операции, а также в послеоперационном периоде выявлено не было. Полное разрешение предоперационных симптомов отмечено через 3 мес. после вмешательства.
Роль везикулоскопии в диагностике и лечении КПЖ изучали корейские ученые во главе с Pil Moon Kang [32].
В исследование был включен 61 пациент с симптоматической срединной КПЖ и жалобами на гематоспермию, симптомы хронической тазовой боли (боль в промежности, дискомфорт в мошонке и боль в яичках) и нарушенную эякуляцию, не получавший медикаментозной терапии на протяжении 4 нед. Всем пациентам выполнена трансуретральная везикулоскопия с использованием ригидного уретероскопа 9,0 Fr и электрода Bugbee. По результатам эндоскопического исследования, кровоизлияние в расширенную простатическую маточку и семенной пузырек наблюдалось у 11 (18,0%) и 21 (34,4%) больного соответственно. Камни в полости расширенной простатической маточки наблюдались у 12 (19,7%) пациентов, в то время как камни в семенном пузырьке обнаружены у 6 (9,8%) пациентов. Гематоспермия разрешилась у 29 (90,6%) из 32 пациентов после оперативного лечения, а у 29 пациентов с синдромом хронической тазовой боли и нарушениями эякуляции показатели шкалы симптомов хронического простатита (NIH-CPSI) после лечения улучшились с 19,0±3,8 до 11,8±3,6 (p<0,001). Острый эпидидимит как послеоперационное осложнение наблюдался у 2 (3,3%) пациентов. Данное исследование показало, что роль везикулоскопии в уменьшении симптомов может быть опосредованна эффектами эндоскопической фенестрации, удалением сгустков крови, конкрементов, гнойного содержимого, при необходимости – электрокоагуляцией внутрикистозного кровоизлияния. Данный эндоскопический метод позволил совместить диагностический и терапевтический подходы к лечению симптоматических срединных КПЖ.
Первую лазерную литотрипсию камней семенных пузырьков пациенту 25 лет с жалобами на болезненную эякуляцию описал S. P. Cuda et al. в ноябре 2006 г. [33]. Ригидным уретероскопом 7 Fr выполнена трансуретральная везикулоскопия, при которой обнаружена группа рыхлых конкрементов диаметром 1–3 мм, заполнявших семенные пузырьки и семявыбрасывающие протоки. Камни были фрагментированы гольмиевым лазером (Ho:YAG) и удалены орошением ирригационной жидкости и корзинкой для литоэкстракции. Пациент был выписан на следующий день после операции, симптомы окончательно купированы в течение 3 мес. Лазерная инцизия кисты простаты у мужчины 35 лет с жалобой на первичное бесплодие описана J. Ethan et al. еще раньше – в 2000 г. [34]. При проведении ТРУЗИ предстательной железы выявлена срединная киста размером 14×9×10 мм, лоцированная выше семенного бугорка и имевшая сообщение с расширенными протоками семенных пузырьков. Больному проведены уретроцистоскопия, лазерная неодимовая (Nd:YAG) инцизия передней стенки кисты под УЗ-наведением. Поскольку киста была недоступной для визуализации при проведении стандартной уретроцистоскопии, сонография разрешила данную проблему, обеспечив прецизиозное рассечение стенки без риска травматизации соседних анатомических структур.
Комбинированный (лазерный и электрохирургический) эндоскопический метод лечения КПЖ с обструкцией семявыбрасывающего протока продемонстрирован группой ученых из Сеула под руководством Joo Yong Lee в 2012 г. [35]. Авторы описали клиническое наблюдение мужчины 32 лет с олиго- и азооспермией, имевшего срединную КПЖ размером 2 см, а также расширенные семенные пузырьки. При помощи гольмиевого лазера трансуретрально выполнено вскрытие полости КПЖ, после чего выполнена монополярная резекция кисты. Через 1 мес. после вмешательства анализ эякулята показал увеличение его объема до 3 мл, концентрация сперматозоидов составила 15,2•106/мл. В заключение авторы отметили, что использование гольмиевого лазера для комбинированного эндоскопического лечения срединной КПЖ имеет следующие преимущества: прецизия при вскрытии стенки кисты, предотвращение ненужной коагуляции, снижение риска повреждения соседних структур. Преимущества гольмиевой лазерной эндохирургии КПЖ и обструкции семявыбрасывающих протоков отмечены и в ряде других работ [36, 37].
Таким образом, масса авторов подтверждают высокую эффективность и безопасность эндоскопических методов оперативного лечения КПЖ. Трансуретральная марсупиализация остается наиболее распространенным эндоскопическим методом лечения средних по размеру кист. Однако небольшое количество данных литературы подчеркивает: трансуретральные эндоскопические вмешательства по поводу КПЖ до сих пор находятся в состоянии изучения и освоения, требуют дополнительного рассмотрения.
Кисты предстательной железы – относительно редкое заболевание, выбор метода лечения которого окончательно не определен и напрямую зависит от размера кист, анатомо-топографических особенностей их локализации, а также от мануальных навыков врачей-урологов и оснащенности клиники. При выборе метода лечения следует учитывать сопутствующий коморбидный статус пациента, который может влиять в том числе на выбор анестезиологического пособия и укладку больного на операционном столе.
Предпочтительным методом оперативного лечения симптоматических КПЖ небольшого размера при их неглубоком залегании по отношению к простатическому отделу уретры, по нашему мнению, является трансуретральная эндоскопическая марсупиализация или резекция. Кисты большого размера, а также кисты, расположенные далеко (глубоко) от простатического отдела уретры, целесообразно оперировать лапароскопическим (экстраперитонеоскопическим) доступом, что может предотвращать развитие таких потенциальных осложнений, как перфорация прямой кишки, эректильная дисфункция и недержание мочи. В то же время не следует полностью отказываться от выполнения открытых оперативных и пункционных вмешательств при КПЖ, так как в ряде клинических ситуаций они могут оказаться альтернативой эндоскопическим методам лечения или быть методом выбора. В заключение хотелось бы подчеркнуть, что выбор метода лечения КПЖ необходимо обсуждать с пациентом, придерживаясь персонифицированного подхода.



