Введение. Хронический рецидивирующий цистит (ХРЦ) – сложная многогранная проблема современной уроинфектологии [1–3]. С развитием новых методов диагностики и с изменением в последние годы точки зрения на патогенетические основы инфекционно-воспалительных заболеваний нижних мочевыводящих путей, связанных с парадигмой нестерильности мочи и мочевыводящих путей в целом, меняется укрепившееся за долгие годы мнение об этиологической структуре, патогенезе, применяемых методах диагностики и лечения ХРЦ [4–7].
Известно, что при определенных предрасполагающих факторах цистит может быть вызван не только аэробными микроорганизмами, но и анаэробными бактериями, вирусами, грибами [8–10].
В связи с этим, естественно, меняется и план обследования пациенток, страдающих данным заболеванием, который не всегда согласуется с принятыми клиническими рекомендациями по обследованию пациенток с ХРЦ [11–13].
Кроме того, учитывая, что лечение ХРЦ, в соответствии с общепринятыми рекомендацаиями, сопровождается высоким уровнем рецидива, акцентируется целесообразность дифференциального подхода к диагностике и лечению данного заболевания [14, 15].
В связи с этим на современном этапе изучения вопросов этиологии, патогенеза и диагностики ХРЦ любого генеза патофизиология заболевания признается многогранной, несмотря на то, что постулируются некоторые доминирующие механизмы воздействия, такие как инфекционные, аутоиммунные, неврологические, эндокринные и психологические факторы [16, 17].
Также доказано, что хронизация инфекционно-воспалительного процесса в стенке мочевого пузыря происходит при дисфункции местного иммунитета. Известно, что в состав мукозоассоциированной лимфоидной ткани мочевыводящих путей входят различные клетки врожденного и адаптивного иммунитета: эпителиальные клетки, лимфоциты, макрофаги, дендритные и тучные клетки, натуральные киллеры, дисфункция которых является одним из ведущих патогенетических механизмов развития цистита [18].
Мочевой пузырь, кроме того, имеет и конститутивную пассивную защиту, такую как слизь, антимикробные пептиды, секреторные иммуноглобулины и др., которые защищают его от микробной колонизации. При определенных предрасполагающих факторах, в том числе и при дисфункции местного иммунитета, эта защита может нарушаться. При этом уротелий и резидентные иммунные клетки производят дополнительные защитные молекулы, цитокины и хемокины, которые привлекают воспалительные клетки в инфицированную ткань.
Резидентные и рекрутированные иммунные клетки действуют вместе, уничтожая бактерии в мочевом пузыре и развивая устойчивую иммунную память против инфекции [19, 20]. Некоторые активные пептиды и цитокины могут быть использованы при скрининге и дифференциальной диагностике ХРЦ.
Цель исследования: изучить иммунологические показатели мочи пациенток с хроническим рецидивирующим циститом в зависимости от этиологического фактора.
Материалы и методы. Этическое заявление. Исследование спланировано, проведено в соответствии с положениями Хельсинкской декларации (пересмотренной в г. Форталеза, Бразилия, в октябре 2013 г.) и одобрено Локальным независимым этическим комитетом ФГБОУ ВО РостГМУ Минздрава России на основании ознакомления с предоставленными материалами дизайна и плана реализации работы (протокол № 16/17 от 05.10.2017).
Исследование проведено в рамках выполнения диссертационной работы «Оптимизация дифференциальной диагностики и выбора первой линии терапии хронического рецидивирующего цистита у женщин». Исследование не имело спонсорской поддержки.
Пациенты. В проспективное исследование включена 71 пациентка в возрасте 20–45 лет, которым был ранее установлен диагноз «хронический рецидивирующий цистит (ХРЦ) в период обострения». Критерии включения и невключения пациентов для участия в исследовании приведены в табл. 1.

Начальное обследование пациенток включило: сбор жалоб, анамнеза, бактериологическое исследование утренней средней порции мочи, ПЦР-исследование утренней средней порции мочи, соскоба уретры и влагалища и цитологическое исследование мочи. Методология проведения обследования подробно описана в предшествующих работах [14, 17]. По результатам бактериологического и ПЦР-исследований мочи, соскоба уретры и влагалища, в зависимости от доминирующего этиологического фактора, пациентки были разделены на три группы: группа 1 (n=30) – с папилломавирусным ХРЦ (ПВИ-ХРЦ), группа 2 (n=30) – с бактериальным ХРЦ (Б-ХРЦ), группа 3 (n=11) – с кандидозным ХРЦ (К-ХРЦ).
Анализ оценки иммунологических показателей мочи проводили при иммуноферментном анализе (ИФА–БЕСТ). Определялись провоспалительные цитокины: интерлейкин 1-бета (ИЛ-1 бета) (норма – 0–11 пг/мл), интерлейкин-8 (ИЛ-8) (норма – 0–12,0 пг/мл), интерлейкин-6 (ИЛ-6) (норма – 0,0–7,0 пг/мл) и противовоспалительные цитокины: интерлейкин-4 (ИЛ-4) (норма – 0–4 пг/мл), а также фактор некроза опухоли (ФНО) (норма <6 пг/мл), интерферон-альфа 2b (ИФНα-2b) (норма – 0–20 пг/мл), интерферон-гамма (ИФНγ) (норма – 0–20 пг/мл).
Метод определения основан на трехстадийном «сэндвич»-варианте твердофазного ИФА с использованием моно- и поликлональных антител к ИЛ-1 бета и антител к ИЛ-6, моноклональных антител к ИЛ-8 и -4, моноклональных антител к ФНО, моноклональных антител к ИФНα-2b и ИФНγ. Важным этапом исследования было изучение в моче концентрации уровней ИФНα-2b и ИФНγ, потому что полученные данные могут служить ориентиром не только диагностики, но и лечения пациенток с ХРЦ различного генеза. Кроме того, для проведения методики использовались калибровочные образцы, содержащие известное количество ИЛ-1 бета, -6, -4, -8, ФНО конъюгат – стрептавидин-пероксидаза хрена, готовый к использованию, раствор для восстановления калибровочных и контрольных образцов ИЛ (РВО), раствор для разведения образцов (РРО), концентрат фосфатно-солевого буферного раствора с твином (ФСБ-Т×25) и раствор тетраметилбензидина (раствор ТМБ плюс). После измерения оптической плотности раствора в лунках на основании калибровочного графика рассчитывалась концентрация в анализируемых образцах.
Методика проведения исследования показателей иммунитета. При иммуноферментном анализе с применением антител к ИФНα-2b и ИФНγ в лунках при добавлении исследуемого образца сыворотки крови во время первой инкубации происходит связывание ИФНα-2b или ИФНγ с моноклональными антителами, иммобилизованными на внутренней поверхности лунок планшета. Во время второй инкубации конъюгат поликлональных антител к ИФНα-2b или ИФНγ с пероксидазой связывается с альфа-интерфероном, иммобилизованным в ходе первой инкубации. Во время инкубации с раствором тетраметилбензидина происходит окрашивание раствора в лунках. Степень окраски прямо пропорциональна концентрации ИФНα-2b или ИФНγ в анализируемых пробах.
Статистические расчеты выполнялись с использованием электронных таблиц Excel (Office, 2019) и программного обеспечения Statistica, 10 (StatSoft Inc., США). Численные данные представлены значением медианы и квартилей Me (Q1; Q3). Статистическая значимость различий групп оценивалась с помощью непараметрических тестов: теста Манна–Уитни при сравнении двух групп и Краскела–Уоллиса при сравнении трех и более независимых групп. При сравнении долей качественных признаков использовались Хи квадрат с поправкой на правдоподобие и точный критерий Фишера. Применялся общепринятый критерий значимости при статистических расчетах; р≤0,05, при сравнении долей трех групп и более учитывалась поправка Бонферрони на множественность сравнений. Использовались общепринятые уровни значимости; p<0,05.
Результаты. По возрасту исследуемые группы были сопоставимыми. По длительности заболевания достоверные различия были выявлены между I и III группами, а по числу обострений в течение года имелись значимые различия между I, II группами, с одной стороны, и III группой, с другой (p<0,05) (табл. 2).

При оценке фактора некроза опухоли регистрировались достоверные различия между исследуемыми группами. Ме (Q1; Q3), и максимальные и минимальные значения разброса полученных результатов в исследуемых группах соответствовали нормативным значениям только у пациенток I группы. По Ме, Q3, и минимальным значениям II и III группы достоверно различались, а по максимальному значению практически были идентичными (рис. 1).
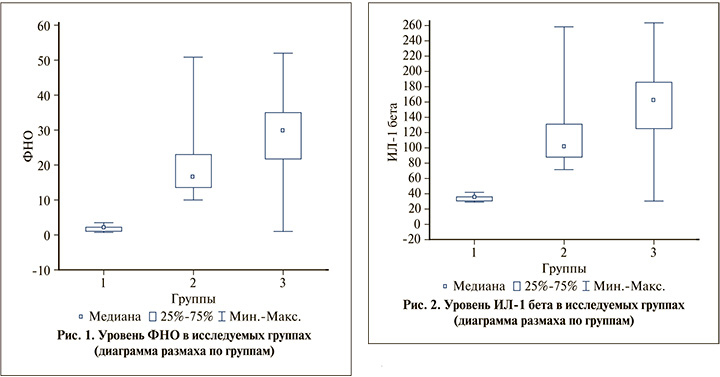
Результаты исследования Ме уровней ИЛ-1 бета и ИЛ-6 корреспондировали с результатами исследования уровня ФНО в группах, которые достоверно были выше у пациенток III группы, у пациенток I группы Ме и (Q1; Q3) исследуемых показателей оставались в пределах референсных значений (рис. 2, 3).
Касательно анализа уровня ИЛ-8 полученные результаты практически идентичны у пациенток II и III групп, Ме в двух группах практически одинаковы, хотя имеются различия по (Q1; Q3) и по максимальным и минимальным значениям.
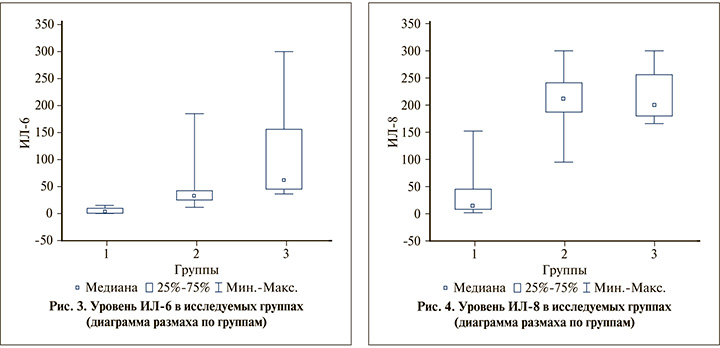
Кроме того, полученные данные II и III групп достоверно отличались от результатов пациенток I группы. Несмотря на различия по некоторым параметрам статистических данных, анализ полученного материала пациенток в трех исследуемых группах по уровню ИЛ-8 свидетельствовал о наличии инфекционно-воспалительного процесса, но с более интенсивным течением у пациенток II и III групп (рис. 4).
Уровень ИЛ-4 во всех исследуемых группах соответствовал нормативному значению, что свидетельствует об отсутствии аллергического компонента в патогенезе инфекционно-воспалительного процесса у пациенток исследуемых групп (рис. 5).
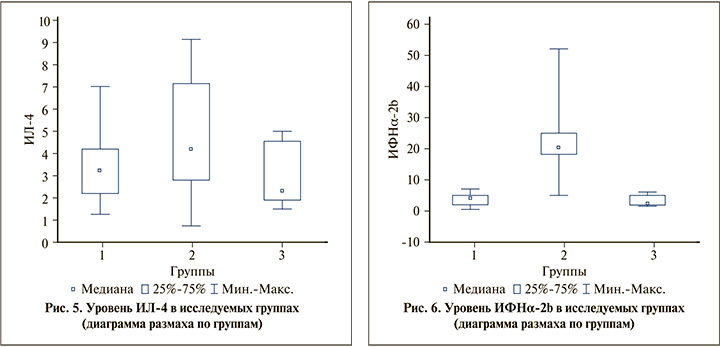
Анализ уровня ИФНα-2b выявил одинаковые результаты у пациенток I и III групп как по Ме, так и по (Q1; Q3) и максимальным и минимальным значениям. Однако, у пациенток II группы Me, Q3 и минимальное значение разброса соответствовали нормативному уровню, а Q1 и максимальное значение были выше нормы (рис. 6).
Уровень ИФНγ во всех исследуемых группах был в пределах допустимых референсных значений (рис. 7).
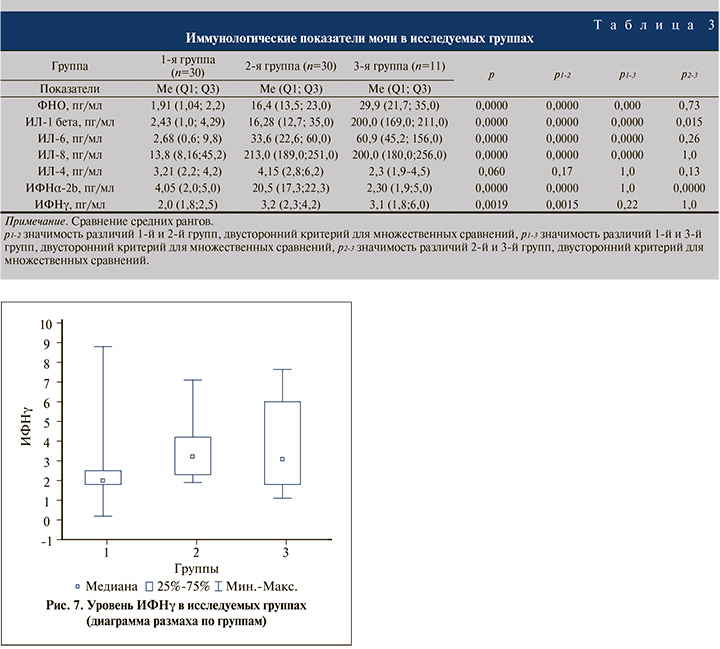
Таким образом, по уровню ФНО и данным уровней ИФНα-2b и ИФНγ, которые в исследуемых группах не превышали нормативных параметров, исследуемые группы были практически сопоставимыми (табл. 3).
Обсуждение. Основные результаты данного исследования заключаются в том, что нами были изучены иммунологические показатели мочи пациенток с ХРЦ различного генеза. При этом выявлены достоверные различия обследуемых групп больных по уровню ФНО и ИЛ-1 бета, -6, -8. У пациенток с бактериальным и грибковым циститом отмечалось значимое и достоверное повышение уровней ИЛ-1 бета и ИЛ-8, что свидетельствует об активном участии макрофагального звена в инфекционно-воспалительном процессе у пациенток данной категории. Известно, что повышение уровня макрофагов свидетельствует об активном бактериальном воспалительном процессе, при котором дегрануляции макрофагов, нейтрофилов приводят к повышению уровня интерлейкинов [19]. Следует заметить, что результаты исследования уровня интерферонов, конечно, необходимо рассматривать в контексте с остальными лабораторными и клинико-анамнестическими данными. Однако, снижение продукции альфа- и гамма-интерферона на фоне острого инфекционно-воспалительного процесса может быть следствием хронического вирусного процесса (I группа) или результатом длительного персистирующего инфекционно-воспалительного процесса (II и III группы), но в обоих случаях самое главное – это свидетельство о врожденном дефиците или приобретенном истощении системы интерферонов, что может рассматриваться как показание к интерферон-стимулирующей терапии.
По данным литературы устойчивая экспрессия цитокинов и активная и выраженная воспалительная инфильтрация различных клеток, участвующих в инфекционном-воспалительном процессе в мочевом пузыре во время активации мочевой инфекции, зависят от вида бактерий и пола [20], поэтому женщины чаще болеют ХРЦ. Доказано, что существуют некоторые видовые различия микроорганизмов, участвующих в этиологической структуре ХРЦ [4].
Кроме того, исследования последних лет доказали различия в иммунном статусе по полу, которые влияют на исход инфекционно-воспалительного процесса мочевыводящих путей [21]. В данном направлении требуется проведение многоцентровых рандомизированных исследований.
Полученные нами результаты свидетельствуют о том, что уровни ФНО и ИЛ-1 бета, -6, -8 могут быть использованы в качестве критериев скрининга в дифференциальной диагностике ХРЦ различного генеза, что позволит начать правильную этиотропную терапию, которая может быть откорректирована после получения данных культурального исследования. Учитывая значения ИФНα-2b и ИФНγ, можно определить степень нарушения иммунного ответа и необходимость проведения иммуноактивной терапии.
Выводы. Хронический рецидивирующий цистит – полиэтиологическое заболевание, а идентификация этиологического фактора – сложная задача, которая определяет залог успешного лечения.
Проведенное нами исследование показало целесообразность тестирования интерлейкинов в моче (ИЛ-1 бета, -6, -8). Данные показатели могут служить критерием в дифференциальной диагностике ХРЦ различного генеза.
Кроме того, обоснованным является изучение уровня ИФНα-2b и ИФНγ, так как при выявлении функциональной неполноценности системы ИФН у женщин с ХРЦ необходима ее коррекция



