Введение. На сегодняшний день является общеизвестным, что использование полноразмерных вагинальных сеток для лечения пролапса тазовых органов (ПТО) в сочетании с недостаточным опытом хирургов являются доминирующими факторами риска серьезных послеоперационных осложнений [1, 2]. Первые сетчатые имплантаты для коррекции ПТО имели четыре рукава и центральную площадку. Их главной задачей было полное протезирование эндопельвикальной фасции [3]. Эти стандартизированные наборы (предварительно выкроенная сетка и одноразовые инструменты) были разработаны практически без учета вариантной анатомии таза и продвигались производителями в соответствии с концепцией «подходит всем пациентам, подходит всем хирургам». Этот подход привел к значительному количеству осложнений, широкому общественному резонансу и как следствие – к неопределенному положению сеток в хирургии тазового дна во многих странах на сегодняшний день.
В недавнем систематическом обзоре, представленном Ugianskiene и коллегами, обсуждался вопрос необходимости совершенствования хирургической техники реконструкции ПТО [4]. Тот же постулат подтверждается высококачественным исследованием PROSPECT [5], и хотя в этом исследовании сообщается об осложнениях после использования вагинальных сеток, авторы отмечают, что исходы хирургического лечения могут быть более успешными, если операция будет проводиться опытными хирургами – специалистами в реконструктивной хирургии тазового дна в референс-центрах [5]. Далее в упомянутом выше обзоре Ugianskiene, оценивая перспективы использования вагинальных сеток в связи с их сложным положением на сегодняшний день, авторы предполагают, что трансвагинальные сетки должны имплантироваться только в специализированных центрах хирургами с опытом как установки, так и удаления протезов [4].
Отсутствие консенсуса относительно выбора метода хирургического лечения ПТО в сообществе урогинекологов является проблемой не только для специалистов, но и для пациенток, которые из-за этой путаницы не могут получить необходимую им медицинскую помощь.
Основной целью данного исследования являются ретроспективная оценка безопасности и эффективности различных методик коррекции ПТО при помощи вагинальных сеток и выбор наиболее оптимального метода хирургического лечения.
Материалы и методы. С 2012 по 2019 г. в Университетской клинике Санкт-Петербургского государственного университета (СПбГУ) последовательно использовалось 7 типов хирургических методик с применением сеток, различающихся объемом имплантированного материала, наличием и типом одновременной реконструктивной операции собственными тканями, методом фиксации сетки и числом точек фиксации. Каждая операция выполнялась вагинальным доступом.
Ретроспективный анализ проводился на основании данных, полученных из электронных историй болезни. Каждая история содержала данные осмотров в течение 12 мес. после операции. Критерии включения в ретроспективный анализ: наличие реконструктивной операции, выполненной с использованием сетчатых имплантатов, в связи с наличием ПТО III–IV стадий по классификации Baden-Walker, подтвержденной осмотром в кресле, подписанное информированное согласие пациенток на использование их персональных данных в исследовании. Критериями исключения были элонгация шейки матки, дисплазия шейки матки, недиагностированные нерегулярные маточные кровотечения, эндометриоз и хроническая тазовая боль. Стадия пролапса оценивалась в соответствии с системой Baden-Walker для унифакации классификации степени пролапса тазовых органов. [6]. Оценивались следующие показатели: тип проведенной операции, продолжительность операции, продолжительность послеоперационного койко-дня, интраоперационные осложнения (кровопотеря, травма мочевого пузыря или прямой кишки), ранние послеоперационные осложнения (клинически значимые гематомы, задержка мочи). Рецидивом считался клинически подтвержденный пролапс более II стадии по Baden-Walker, требующий повторной реконструктивной операции. Оценка состояния пациенток проводилась только оперирующими хирургами во время контрольных осмотров, после чего данные заносились в электронную историю болезни.
Послеоперационное обследование, проведенное через 12 мес., позволило получить информацию о самых частых осложнениях и побочных эффектах, а также об анатомической эффективности лечения и субъективной удовлетворенности пациентов. Для оценки точности и полноты данных мы использовали физикальный осмотр в гинекологическом кресле и валидированные в России опросники (Pelvic Floor Distress Inventory-20 (PFDI-20) и Pelvic Organ Prolapse/Urinary Incontinence Sexual Questionnaire-12 (PISQ-12).
Статистическая обработка. Количественные данные описывались с помощью среднего значения±стандартного отклонения, а также с помощью 95% доверительных интервалов для средних значений (95% ДИ). Для описания различных значений категориальных данных рассчитывались абсолютные частоты и проценты от общего числа наблюдений. Обработка категориальных данных проводилась с помощью таблиц сопряженности и точного теста Фишера. При множественных парных сравнениях использовалась поправка Бонферрони. Для сравнения результатов лечения между группами использовался ANOVA (однофакторный дисперсионный анализ). Уровень значимости (альфа) установлен как 0,05.
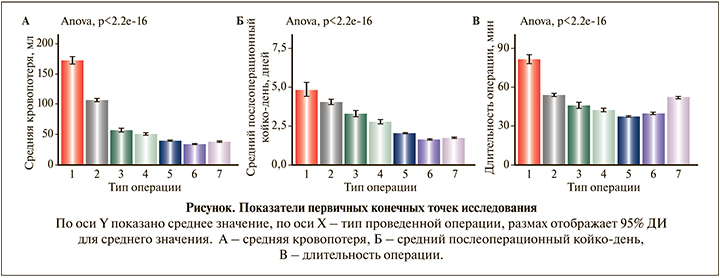
Результаты. В окончательный анализ вошла 5031 история болезни пациенток, прооперированых в период с 2012 по 2019 г. Все включенные в анализ пациентки были сопоставимыми по базовым характеристикам (табл. 1). Средний возраст пациенток составил 54±9 лет. Техники операций для упрощения дальнейшего восприятия в тексте закодированы от «1» до «7», подробно описаны и показаны в табл. 2.


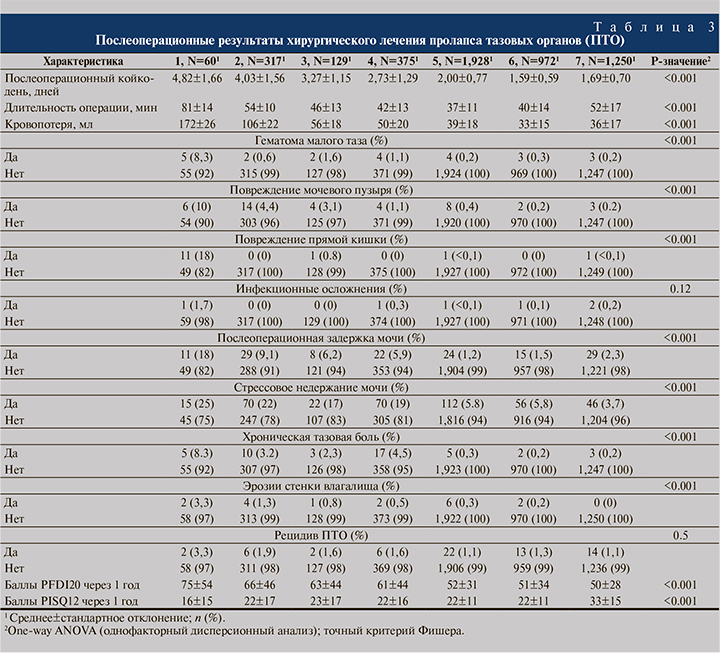
Были получены статистически значимые различия в числе большинства послеоперационных осложнений (табл. 3). Не наблюдалось различий лишь по частоте инфекционных осложнений (p=0,12). Техника «7» продемонстрировала статистически значимо более низкий риск травм мочевого пузыря, гематом в малом тазу, эрозии стенок влагалища, а также синдрома хронической тазовой боли по сравнению с техниками «1»–«6». Техники «5» и «6» показали сопоставимые результаты по всем осложнениям по сравнению с техникой «7».
Помимо объективных данных мы также оценивали субъективные показатели с помощью опросника PFDI20 до операции и через год после операции, который обладает достаточно высокой чувствительностью и может быть использован для измерения степени влияния симптомов нижних мочевыводящих путей, нижних отделов желудочно-кишечного тракта и симптомов ПТО на качество жизни женщин [7]. До операции не было значительных различий в баллах PFDI20 между всеми группами (p=0,2).
Средний балл между всеми группами составил 188±31 балл. Мы обнаружили статистически значимое снижение выраженности симптомов пролапса через год после операции во всех группах по сравнению с периодом до операции (p<0,001). По данным post-hoc-анализа показателей наблюдения отмечалось статистически значимое снижение выраженности симптомов у пациенток, которым проводилось лечение по методикам «5» (52±31), «6» (51±34), «7» (52±31) по сравнению с остальными группами, «1» (75±54), «2» (66±46) и «3» (63±44) в то время как между этими группами не было значительного улучшения (p=0,3). PISQ-12 – это валидизированная и надежная краткая форма опросника, которая оценивает сексуальную функцию женщин с недержанием мочи и/или пролапсом тазовых органов [8]. Все пациентки заполняют его при поступлении и при послеоперационном осмотре. Анализ не выявил существенных различий в результатах анкет PISQ12 у пациенток в период до операции, средняя оценка составила 21±12 баллов (p=0,7).
Тем не менее, при контрольном наблюдении значительное снижение среднего балла по опроснику наблюдалось у пациенток, которым была выполнена техника «1», на 16±15 баллов (p<0,001). Пациентки, прооперированные по технике «7», показали самый высокий средний балл (33±15) по опроснику, что было статистически значимо по сравнению с другими техниками (p<0,001). Кроме того, все группы оказались сопоставимыми по числу рецидивов ПТО (p=0.5). Рецидивы в апикальном отделе при использовании любой техники не превышали 3,3%.
Обсуждение. Известно, что наиболее распространенным видом ПТО является цистоцеле в сочетании с апикальным пролапсом [9, 10]. Традиционные методики, такие как передняя и задняя кольпоррафии, восстанавливают только II уровень поддержки, согласно DeLancey [11]. Неудивительно, что отсутствие должной апикальной поддержки приводит к анатомическому рецидиву у значительного числа пациенток уже через год после операции (до 58%) [12]. Напротив, даже изолированная хирургическая коррекция на уровне I уровня по DeLancey устраняет опущение передней стенки влагалища у половины пациенток [13]. Одной из наиболее изученных и эффективных методик апикального восстановления является сакроспинальная фиксация [14]. В 1997 г. при попытке снизить травматичность и добиться более физиологичного положения оси влагалища был предложен задний интравагинальный слинг [7]. Несмотря на высокую эффективность и хорошие функциональные результаты, эта техника не получила должного развития из-за использованного несовершенного имплантата (мультифиламентная микропористая сетка) и последующей серии осложнений инфекционного характера, связанных с имплантатом [8, 15–17]. Апикальный слинг является дальнейшим развитием этой техники. Несмотря на высокую эффективность, техника имеет ряд недостатков: фиксация протеза может приводить к хроническому болевому синдрому и диспареунии, а подшивание имплантата к ослабленным тканям свода влагалища может снижать эффективность [18, 19]. Тем не менее до 80% пациенток с апикальным пролапсом имеют сопутствующие дефекты тазового дна, такие как цистоцеле, ректоцеле или энтероцеле [20, 21]. Все это свидетельствует о необходимости поиска новых методик одновременной коррекции 1, 2 и 3 уровней поддержки для эффективного и безопасного лечения.
Ближайшей альтернативой нашему методу установки полноразмерных имплантатов была система Prolift System®. По данным Fatton et al. наиболее распространенными осложнениями, связанными с установкой этой сетки, были контрактура (17%), экструзия (4,7%), гранулема без экструзии (2,8%) и вагинальные синехии (0,9%). Непосредственные послеоперационные осложнения включали инфекцию мочевыводящих путей (11,8%), задержку мочи (11,8%) и гематому, потребовавшую хирургического вмешательства (1,8%) [22]. Наши результаты отчасти согласуются с этими данными. Поскольку тотальная реконструкция тазового дна связана с широкой диссекцией тканей, логично, что доминирующие осложнения будут связаны с дисфункцией органов малого таза.
Другой полноразмерной сеткой, близкой по техническим характеристикам к нашей, является шестирукавная трансвагинальная сетка OPUR (Abiss, Сент-Этьен, Франция). В исследовании Kluz et al. эта сетка была установлена 39 пациенткам [23]. Результаты этого исследования совпадают с нашими в отношении распространенности стрессового недержания мочи (СНМ) при наблюдении в течение 1 года. Однако они отличаются в отношении развития гематом, задержки мочи и поражения прямой кишки. Авторы не наблюдали этих осложнений в послеоперационном периоде.
Среди имплантатов для одновременной коррекции апикального и переднего отделов наиболее близкими к используемому нами являются наборы сеток большого размера, такие как Elevate Apical и Anterior (AMS). Как и имплантат нашего производства, эта сетка содержит 4 точки фиксации. Эффективность этой системы после 12-месячного наблюдения составила около 90–98%; нежелательные явления включали экструзию в 3–5% и задержку мочи в 11,9% [24]. В нашем исследовании мы наблюдали эти осложнения в меньшей степени, чем СНМ. Кроме того, в значительном числе наблюдений синдром хронической тазовой боли не отмечался.
Накапливая значительный хирургический опыт, мы пришли к выводу, что разработанная нами гибридная техника установки апикального слинга с субфасциальной кольпоперинеоррафией является наиболее оптимальной с точки зрения безопасности и эффективности. Важно отметить, что указанная техника отличается от той, что была представлена нами в предыдущих публикациях [25]. Главное отличие заключается в том, что фиксация сетчатого имплантата осуществляется не в двух крестцово-остистых связках, а в одной – односторонняя фиксация. Мы учитывали, что, по данным литературы, сакроспинальная фиксация характеризуется смещением оси влагалища. Чтобы минимизировать этот эффект ретрофлексии, мы использовали имплантат в качестве «мостика» между точками фиксации. Кроме того, выполнялась субфасциальная кольпоррафия, которая позволила закрыть большинство дефектов пубоцервикальной фасции [26]. Благодаря этим техническим решениям удалось снизить частоту рецидивов при сроке наблюдения 12 мес. Кроме того, важным отличием является необходимость восстановления не только 1-го и 2-го уровней поддержки тазового дна, но и третьего, который представлен мочеполовой диафрагмой [20]. Наиболее распространенным послеоперационным осложнением крестцово-остистой фиксации является высокая частота пролапса de novo в переднем отделе (20–33%) [27]. В нашем исследовании не было длительного периода наблюдения, и частым «поздним» осложнением было СНМ. Известно, что наличие подтекания мочи при напряжении характерно для пациенток с ПТО. До сих пор не существует единого алгоритма относительно одновременной установки слинга во время коррекции ПТО [28]. Одним из наших основных принципов в отношении СНМ был отказ от одновременной установки субуретрального слинга. Все пациентки с жалобами на подтекание мочи при напряжении при наблюдении в течение 1 года были приглашены для хирургического лечения. Наиболее распространенным осложнением раннего послеоперационного периода была задержка мочи (до 18%), которая устранялась установкой уретрального катетера на 1 неделю.
Мы получили важные данные о качестве сексуальной жизни пациенток после хирургического лечения в зависимости от типа операции. Наибольшую удовлетворенность от сексуальной жизни отмечали пациентки после «7-го» типа операции. Мы связываем это с одновременной пластикой задней стенки влагалища и промежности. Следует отметить, что наши данные контрастируют с информацией некоторых авторов, которые связывают развитие диспареунии в послеоперационном периоде с техникой фиксации крестцово-остистой связки [29].
Ограничения. Наше исследование имело ряд ограничений. Среди них ретроспективная оценка результатов и имеющиеся данные лишь за сравнительно короткий период наблюдения (12 мес.). Однако существует ряд исследований, демонстрирующих, что наибольшая частота послеоперационных осложнений после использования интравагинальной сетки развивалась именно в первые 12 мес. наблюдения [30, 31]. Кроме того, важным ограничением мы считаем то, что данные о наличии СНМ до операции были зарегистрированы не у всех пациентов, и поэтому мы не включили их в анализ. Таким образом, мы не можем однозначно ответить на вопрос, сколько пациенток изначально страдали СНМ. Известно, что на данном этапе общепринятой классификацией степени ПТО является система POP-Q, однако ее применение в нашем центре началось с 2014 г. Ввиду необходимости унификации данных о степени ПТО нами было принято решение о стадировании ПТО по системе Baden-Walker. Еще одним ограничением для воспроизведения результатов исследования в другой клинике является то, что все операции проводили опытные хирурги в клинике, выполняющей более 2500 реконструктивных операций тазового дна в год.
Заключение. Данные нашего исследования подтверждают мировые тенденции по уменьшению количества имплантируемого материала в пользу нативной реконструкции. Трехуровневая гибридная реконструкция тазового дна – безопасная и эффективная хирургическая методика, которая может быть предложена пациенткам с ПТО в специализированном стационаре при соответствующем уровне квалификации хирургов.



