Введение. Серьезной медицинской и социальной проблемой современного общества является острый цистит, особенно часто поражающий женщин [1]. В 90% случаев он бывает неосложненным и чаще всего встречается среди женщин трудоспособного возраста [2]. В России распространенность острого цистита у женщин достигает 26–36 млн случаев в год [3].
Антибактериальная терапия остается ведущим направлением в лечении острого неосложненного цистита у женщин, поскольку эрадикация возбудителя при этом заболевании по-прежему – главная задача [1, 3]. Одним из препаратов первой линии в Европе и России в настоящее время является фосфомицина трометамол, назначаемый однократно в дозе 3 г [4]. Эффективность терапии острого цистита фосфомицином достигает 89–95% [1, 3]. Однако серьезной проблемой любой антибактериальной терапии острого цистита, в том числе с использованием фосфомицина, считается сохранение симптомов заболевания в течение нескольких суток от начала лечения из-за продолжающегося воспалительного процесса в стенке мочевого пузыря, несмотря на уничтожение патогена. Болевой симптомокомплекс особенно беспокоит пациентов, ухудшает их качество жизни, подрывает доверие к назначенному лечению и к врачу.
В дополнение к антибактериальной терапии, а иногда и в виде монотерапии цистита пытаются использовать нестероидные противовоспалительные средства [5], Канефрон и другие средства фитотерапии [6], холинолитики и спазмолитики [7]. Среди последних на Урале большое распространение получил дротаверина гидрохлорид (но-шпа). Наш анализ лечения острого цистита в Пермском крае показывает, что урологами амбулаторного звена дротаверин используется в комплексном лечении острого цистита у 44,8% больных. Однако в литературе мы не нашли работ, которые бы достоверно доказали эффективность дротаверина как дополнительного симптоматического средства к антибактериальной терапии цистита.
В то же время все большее внимание ученых приковывают лекарственные средства симптоматического действия, которые широко использовались в доантибиотическую эру в лечении воспаления мочевого пузыря.
Из них в первую очередь заслуживает внимания феназопиридин (пиридиум, пиридазил) – азо-краситель (моногидрохлорид 3-фенилазо-2,6-диаминопиридина), в 1914 г. синтезированный B. Joos [8].
Вскоре возникла идея использовать этот краситель в качестве антисептика при инфекциях мочевыводящих путей, хотя механизм действия феназопиридина к тому моменту не был ясен. К 1934 г. в научной литературе был накоплен опыт использования этого препарата в отношении 3000 пациентов [9]. Одна из крупных научных работ по применению феназопиридина в суммарной дозе 600 мг в лечении неосложненной и осложненной инфекций мочевыводящих путей была опубликована T. J. Kirwin et al. в 1943 г. [10]. Из 118 пролеченных женщин автор добился выздоровления у 55,1%.
Однако открытие антибиотиков отодвинуло на задний план использование феназопиридина при цистите в качестве бактерицидного средства. Он стал применяться в комбинации с антибиотиками с целью купирования дизурии [11, 12].
Причины резко возросшего интереса к препарату в последнее время: общемировая тенденция к снижению эффективности антибиотиков; открытие новых фактов в механизме действия феназопиридина; выдвижение концепции использования уроанальгетиков – препаратов, оказывающих местное анальгетическое действие на структуры мочевыводящих путей. Установлено [13], что феназопиридин и является таким селективным уроанальгетиком.
В США начался бум использования феназопиридина: в 2018 г. было выписано более 700 тыс. рецептов на этот препарат. Россия пока не так активно применяет это новое и весьма перспективное направление в урологии – использование уроанальгетиков в лечении острого цистита и некоторых других заболеваний, а также при инструментальных вмешательствах.
Цель исследования: оценить анальгетический эффект, эффективность и переносимость феназопиридина в комбинации с фосфомицином для лечения острого неосложненного цистита у женщин трудоспособного возраста.
Материалы и методы. В 5 поликлиниках Пермского края (профессорской поликлинике Пермского государственного медицинского университета им. Е. А. Вагнера, поликлинике Пермского краевого центра ФМБА России, городских клинических поликлиниках № 1 и 2 Перми, поликлинике ГБ им. Гринберга Закамска) 6 урологами высшей и первой категорий с 1 сентября 2020 по 30 апреля 2021 г. проведено многоцентровое рандомизированное открытое исследование использования феназопиридина в комбинации с фосфомицином в лечении острого неосложненного цистита, сопровождавшегося болевым симптомокомплексом.
В исследование вошли 152 женщины трудоспособного возраста от 18 до 60 лет, страдавшие острым первичным неосложненным циститом.
Обследование пациенток включило сбор анамнеза, оценку симптомов по шкале ACSS (Acute Cystitis Symptom Score) [14], оценку по 10-балльной визуальной аналоговой шкале боли (ВАШ), физикальное исследование с осмотром наружных половых органов, общий анализ крови, общий анализ мочи с микроскопией, бактериологический анализ мочи, УЗИ мочевого пузыря, почек и женских половых органов (для дифференциальной диагностики). Все исследования проводили в динамике.
Бактериологическое исследование средней порции пузырной мочи включило посев биоматериала на искусственные питательные среды, выделение чистой культуры возбудителя и ее количественную оценку в КОЕ/мл. Среди обнаруженных штаммов преобладала E. coli (81,7%), реже высевались Enterococcus faecalis, Klebsiella pneumonia и др.
Оценку боли по ВАШ проводили при первичном осмотре, а затем через 6, 12, 24 и 48 ч. После получения инструкции по заполнению ВАШ пациентки ставили отметку по шкале от 0 до 10 баллов (в соответствии с субъективной оценкой выраженности боли).
Клинические проявления заболевания и эффективность проводимого лечения оценивали по шкале ACSS [14] на основании суммы баллов характерных симптомов (Typical) по ответам на вопросы 1–5, суммы баллов качества жизни QoL по ответам на вопросы 11–13 и ответа на вопрос об изменении самочувствия (Dynamics), который отражал мнение больной о своем состоянии.
Критерии включения: женщины трудоспособного возраста от 18 до 60 лет с диагнозом «острый неосложненный первичный цистит».
Критерии исключения: вторичный характер цистита (наличие в мочевом пузыре камней, аномалий, инородных тел и др.), осложненный цистит (пиелонефрит, катетер и др.), сопутствовавшие урологические заболевания (нефролитиаз, стрессовое недержание мочи и др.), операции на мочевыводящих путях в анамнезе, беременность, сахарный диабет.
До проведения процедур исследования и начала лечения все пациентки подписали письменное информированное согласие на участие в исследовании.
Процедуры исследования проведены на 3 визитах: 1-й – постановка диагноза, рандомизация, проведение исходных исследований, начало лечения; 2-й – через 3 сут. (промежуточные результаты); 3-й – через 6 сут. (оценка окончательных результатов).
На первом визите случайным способом (методом конвертов) пациентки были рандомизированы на 2 группы по 76 человек. В основной группе они получали перорально исследуемый препарат феназопиридин (феназалгин, «Stada») в дозе 200 мг (2 таблетки) 3 раза в день в течение 2 сут. (суммарная доза – 1200 мг) и антибиотик фосфомицина трометамол (монурал, «Zambon») в дозе 3 г однократно, в группе сравнения – однократно фосфомицина трометамол (монурал) в дозе 3 г и традиционно используемый для купирования симптомов дизурии при остром цистите препарат дротаверина гидрохлорид (но-шпа, «Chinoin», Венгрия) в дозе 80 мг (2 таблетки) 3 раза в день в течение 2 сут. (суммарная доза – 480 мг).
При выборе фосфомицина в качестве обязательного для всех 152 больных антибактериального препарата мы исходили из рекомендаций Европейской ассоциации урологов и Российских федеральных рекомендаций [1, 4], относящих его к препаратам первой линии в лечении острого цистита, и общепринятого мнения, что феназопиридин нецелесо-образно использовать для монотерапии цистита в качестве замены антибактериального средства [9].
Сравниваемые группы были однородными и не различались (p>0,05) по основным характеристикам (табл. 1). Лейкоцитурия выявлялась у всех пациенток обеих групп.

Оценку клинической эффективности проводили по следующим критериям: выздоровление–исчезновение симптомов заболевания или наличие незначительных остаточных симптомов (суммарно не более 3 баллов по шкале ACSS-Typical), восстановление прежнего качества жизни (отсутствие дискомфорта, восстановление трудоспособности, общественной и социальной активности), нормализация общего анализа мочи; улучшение–уменьшение не менее чем на 75% баллов по шкале ACSS-Typical, отсутствие лейкоцитурии или снижение ее степени; отсутствие эффекта–уменьшение балльной оценки по шкале ACSS-Typical менее чем на 75% по сравнению с исходным уровнем или сохранение лейкоцитурии без снижения ее степени.
Задачей исследования также было определить характер и частоту нежелательных эффектов феназопиридина. Для этого использовали амбулаторные карты, целенаправленный опрос и осмотр пациенток на визитах. Досрочного прекращения лечения от побочных эффектов препаратов не было ни в одной группе.
Статистический анализ выполнен с использованием программы Statistica 10 (StatSoft Inc., США), программное обеспечение Microsoft Excel, 2016. Для оценки различий использовали t-критерий, пороговым уровнем статистической значимости служил показатель p=0,05.
Результаты. Основным инструментом по определению динамики болевой симптоматики, обусловленной воспалением мочевого пузыря, служила ВАШ. У всех пациенток основной группы отмечено значительное снижение выраженности болевой симптоматики: уже через 20 мин после приема феназопиридина пациентки чувствовали уменьшение боли, затем постепенно исчезали боль и дискомфорт в надлобковой области, внизу живота и в глубине малого таза; боль, резь и жжение во время мочеиспускания (табл. 2).

В основной группе исходный показатель по ВАШ на первом визите составил 7,2±0,5 балла, что соответствует характеристике «очень сильная боль». При этом оценку 10 баллов поставили 2 пациенткам, 9 – 4, 8 – 38, от 6 до 7 баллов – 24 пациенткам. Таким образом, у 68 (89,5%) пациенток основной группы выраженность превышала 6 баллов, что свидетельствует о мучительной сильной боли, особенно выраженной в момент мочеиспускания.
Через 6 ч боль снизилась на 48,6% по сравнению с исходным уровнем (см. табл. 2). При этом 2 пациентки уже не испытывали боли ни в покое, ни при мочеиспускании, у 31 больной наблюдалась легкая боль (1–3 балла). Спустя 12 ч снижение составило 77,8% по сравнению с исходным значением. Через 24 ч констатировали уменьшение выраженности боли на 94,5%, или в 18 раз, по сравнению с показателем до лечения. При этом 53 (69,7%) пациентки к этому сроку уже не чувствовали никакой боли. А через 48 ч все 76 (100%) больных основной группы указали на отметку «0» в анкете ВАШ.
Иную картину наблюдали в группе сравнения, где использованная комбинация препаратов не позволила достичь должного положительного эффекта в купировании боли. На всех сроках наблюдения отмечали статистически значимо (p<0,001) более высокие показатели, чем в основной группе (см. табл. 2). Через 6 ч лечения показатель боли практически не отличался от исходного (p>0,05) и соответствовал «сильной боли». Через 12 и 24 ч полученные индексы соответствовали значению «умеренная боль».
И даже через 48 ч у пациенток группы сравнения сохранялся относительно высокий показатель боли (2,4±0,2 балла), при этом 9 (11,8%) больных характеризовали боль как сильную в 5–7 баллов, 60 (79 %) – как легкую или умеренную (1–4 балла) и лишь у 7 (9,2%) пациенток к этому сроку боль полностью исчезла.
Основным современным способом оценки степени выраженности клинических симптомов острого цистита и результатов лечения этого заболевания является шкала ACSS [14].
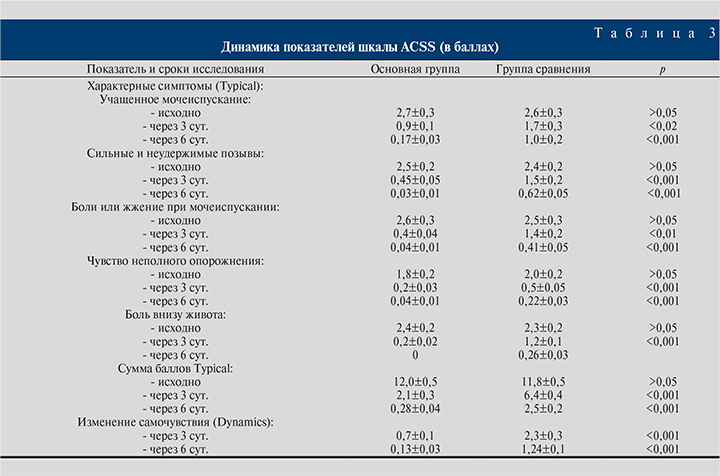
Как хорошо видно из табл. 3, статистически значимо более выраженная динамика показателей всех 5 характерных симптомов заболевания в процессе лечения (p<0,001 по большинству показателей) имела место в основной группе пациенток, принимавших фосфомицина трометамол и феназопиридин. При этом в основной группе значительно уменьшалась выраженность симптомов, связанных с болью (боль и жжение при мочеиспускании, боль внизу живота) и частотой мочеиспускания (учащение мочеиспускания, сильные и неудержимые позывы к нему).
В основной группе особенно выраженное снижение симптоматики происходило в первые 3 сут. наблюдения, т.е. в период применения больными феназалгина. Так, показатель, характеризующий сильные и неудержимые позывы на мочеиспускание, за первые 3 сут. лечения уменьшился на 82%, в следующие 3 дня – только на 16,8%, выраженность симптома «боли или жжение при мочеиспускании» – 84,6 и 13,9 % соответственно (см. табл. 3).
В данном случае налицо прямая связь с приемом феназопиридина, действие которого реализовывалось в течение первых двух суток приема и на 3-и сутки после начала лечения, так как период полувыведения препарата составляет 7,4 ч.
Через 3 сут. лечения сумма баллов характерных симптомов (Typical) в основной группе снизилась по сравнению с исходным уровнем на 9,9 балла (82,5%). В группе сравнения также констатировали снижение, но менее значительное (на 5,4 балла, или на 45,8%), оценка составила 6,4±0,4 балла, достоверно отличаясь (p<0,001) от показателя основной группы. В течение последующих 3 сут. в обеих группах сохранялась аналогичная динамика (см. табл. 3).
При повторных визитах мнение пациенток о результатах лечения лучше всего отражал ответ на вопрос об изменении самочувствия (раздел Dynamics шкалы ACSS). Через 3 сут. оценка по данному разделу в основной группе была достоверно (p<0,001) лучше, чем в группе сравнения (см. табл. 3). При этом самая распространенная среди пациенток основной группы оценка в 1 балл соответствует ответу: стало заметно лучше; большинство симптомов прошли, в то время как большинство пациенток группы сравнения ответили: стало несколько лучше (2 балла) или (реже) изменений практически нет (3 балла). Через 6 сут. показатель самочувствия и оценки пациентками проводимого лечения (Dynamics) в основной группе составил 0,13±0,03 балла, что было лучше (p<0,001), чем в группе сравнения, и у подавляющего большинства опрошенных основной группы ответом было: чувствую себя отлично; все симптомы прошли окончательно (0 баллов).
Ни в одном случае не отмечено таких серьезных осложнений острого цистита, как острый пиелонефрит и обострение хронического пиелонефрита.
В основной группе отмечена более выраженная и быстрая нормализация анализа мочи. Через 3 сут. лечения антибиотиком фосфомицином и феназалгином число лейкоцитов в поле зрения в среднем составило 10,2±2,5, что достоверно (p<0,05) меньше, чем в группе сравнения (17,8±2,8).
Через 6 сут. лечения у подавляющего большинства пациенток обеих групп нормализовался осадок мочи, но число лейкоцитов в основной группе было меньше, чем группе сравнения, – 2,3±0,5 и 5,5±0,9 соответственно (p<0,01).
Окончательные результаты лечения через 6 сут. оказались следующими. В основной группе выздоровление отмечено у 74 (97,4%) пациенток, улучшение – у 2 (2,6%), в группе сравнения – у 72 (94,7 %) и 4 (5,3 %) соответственно.
Бактериологические исследования показали, что через 6 сут. в основной группе эрадикация возбудителя имела место у 62 (96,9%) из 64 больных с исходной бактериурией, персистенция со снижением микробного числа – у 2 (3,1%), в группе сравнения – у 60 (96,8%) из 62 и у 2 (3,2%) соответственно.
Таким образом, при комплексном лечении острого неосложненного цистита фосфомицином и феназопиридином клиническая эффективность составила 97,4%, бактериологическая эффективность – 96,9%.
Результаты лечения острого цистита непосредственно влияли на реабилитацию пациенток и сроки временной нетрудоспособности. В основной группе больные пребывали на больничном листе в среднем 5,1±0,6 дня, что достоверно (p<0,05) меньше, чем в группе сравнения (7,3±0,7 дня), т.е. сроки нетрудоспособности сократились на 30,1%. Более быстрое восстановление трудоспособности пациенток основной группы связано с двумя причинами. Во-первых, с более легким перенесением болезни, так как боль и дизурия у них в среднем исчезали намного раньше, чем у больных группы сравнения. Во-вторых, к 5–6-му дню от начала заболевания психологически и физиологически подавляющее большинство пациенток основной группы были готовы к возобновлению трудовой деятельности, т.к. уже не испытывали учащенных позывов к мочеиспусканию, не нуждались в частых посещениях туалета на рабочем месте, могли свободно совершать поездки к месту работы.
Побочный эффект феназалгина диагностировали у 1 (1,3%) пациентки, он проявлялся в виде умеренной тошноты и не привел к отказу от дальнейшего приема препарата.
На яркое окрашивание мочи в красно-оранжевый цвет обратили внимание 11 (14,5%) женщин, мочи и кала – 2 (2,6%), однако все пациентки были предупреждены об этом явлении до начала лечения, поэтому это не вызывало у них негативной реакции и нами, как и другими авторами [10–13], не считалось побочным эффектом терапии.
Серьезных нежелательных явлений на фоне приема 1200 мг феназалгина не зафиксировано. Изменения уровня гемоглобина, количества эритроцитов, лейкоцитов, лимфоцитов и моноцитов в контрольном анализе крови отсутствовали.
Обсуждение. Проведенное исследование выявило значительно выраженные анальгетический и антидизурический эффекты феназопиридина в суммарной 2-суточной дозе 1200 мг при его сочетанном использовании с фосфомицином по сравнению с терапевтической комбинацией фосфомицина с дротаверином.
На всех сроках наблюдения, от 6 до 48 ч от начала лечения, в группе, где применялся феназалгин, обнаружен мощный анальгетический эффект, приведший к снижению показателя боли с исходных 7,2 балла (что характеризуется по шкале как «очень сильная боль») до крайне незначительного (0,4 балла) уже через 24 ч и затем к полному исчезновению боли спустя 48 ч после начала лечения. В группе сравнения, где с целью купирования боли использовали дротаверин, болевые ощущения по ВАШ на всех сроках наблюдения были значительно сильнее, чем в основной группе.
Выраженный местный (уроселективный) обезболивающий эффект феназалгина в суммарной дозе 1200 мг отчетливо проявился и при анализе шкалы ACSS. Среди характерных симптомов (Typical) чувство боли характеризуют симптомами № 3 («боли или жжение при мочеиспускании») и № 5 («боль внизу живота»). В основной группе через 3 сут. отмечено резкое снижение цифровых показателей выраженности этих болевых симптомов как по сравнению с высоким изначальным уровнем (снижение в 6,5 раза по симптому № 3 и в 12 – по симптому № 5), так и в сравнении с показателем группы сравнения, в которой использованная комбинация препаратов значительно уступала по купированию болевых симптомов цистита. У большинства пациенток группы сравнения в течение 3 первых сут. лечения сохранялись оба болевых симптома, причиняя выраженный дискомфорт и снижая веру во врача, в излечение и в эффективность применяемого антибиотика.
Выраженный избирательный (на нижние мочевыводящие пути) обезболивающий эффект феназопиридина, подтвержденный другими авторами [8, 13, 15], стал причиной того, что этот препарат нередко называют уроанальгетиком, т.е. относят к классу лекарственных средств, оказывающих селективное анальгетическое действие на нижние мочевыводящие пути [13].
Каков же механизм селективного обезболивающего действия феназопиридина на мочевой пузырь? Ответ на этот вопрос пытались найти многие, и в 2010 г. основной механизм раскрыла группа ученых во главе с N. Aizawa. На подопытных крысах женского пола была проведена оценка влияния феназопиридина на активность афферентной иннервации путем прямого измерения скорости проведения нервного импульса по Aδ- и С-волокнам мочевого пузыря. Было установлено, что внутривенное введение феназопиридина дозозависимо снижало активность Aδ-волокон, но не влияло на С-волокна. Таким образом, феназопиридин реализует свои клинические эффекты в результате прямого ингибирующего действия на интрамуральные афферентные Aδ-волокна, обеспечивающие чувствительность мочевого пузыря [16]. Aδ-волокна служат для приема и передачи информации, связанной с острой и сильной болью.
Однако наше исследование показывает, что действие феназопиридина не ограничивается уроселективным обезболивающим эффектом, препарат оказывает выраженное влияние и на симптомы нижних мочевыводящих путей, не связанные с чувством боли. Данные табл. 3 отчетливо демонстрируют тормозящее действие феназопиридина на симптомы № 1 шкалы ACSS (учащенное мочеиспускание), № 2 (сильные и неудержимые позывы на мочеиспускание) и № 4 (чувство неполного опорожнения мочевого пузыря). По сравнению с группой сравнения выраженность вышеперечисленных симптомов цистита уменьшалась значительнее и быстрее.
Очевидно, помимо влияния на интрамуральные афферентные Aδ-волокна существуют другие механизмы положительного действия феназопиридина при цистите.
Феназопиридин и его метаболиты быстро выводятся из организма почками. При приеме суточной дозы (600 мг) 90% препарата элиминируются в течение суток, причем 41% в неизмененном виде (в качестве азо-красителя) и 49% в виде метаболита [17]. Выделяясь в большой концентрации с мочой, феназопиридин и его метаболиты достигают воспаленной, раздраженной провоспалительными цитокинами слизистой мочевого пузыря и помимо анальгетического эффекта снимают это состояние перераздражения слизистой оболочки, тем самым уменьшая дизурические явления. Существует гипотеза, согласно которой считается, что феназопиридин местно ингибирует циклооксигеназу в уротелии. В таком случае препарат должен обладать противовоспалительным эффектом, что дополнительно позволяет уменьшать симптомы заболевания.
Проведенное исследование показало высокую клиническую эффективность феназалгина (в комбинации с антибиотиком фосфомицином) как симптоматического и анальгетического средства в лечении пациенток с острым неосложненным циститом.
Таким образом, наше исследование показало, что антибактериальное лечение острого неосложненного цистита фосфомицином целесообразно дополнять препаратом феназалгин, обладающим анальгетическим и антидизурическим эффектом. Это позволяет в более короткие сроки добиваться исчезновения лейкоцитурии, т.е. более быстрыми темпами санировать мочевыводящие пути, обеспечивать благоприятное самочувствие пациенток, значительно сокращать сроки временной нетрудоспособности.
Стоит отметить, что на заре появления феназопиридина предполагался его умеренный бактерицидный эффект в отношении кишечной палочки, стафилококка и стрептококка. После открытия антибиотиков, обладающих значительно большим бактерицидным эффектом, последние вытеснили феназопиридин как средство лечения инфекций мочевыводящих путей. Однако феназопиридин, как и любой азо-краситель, обладает антисептическим эффектом. Есть основания полагать, что феназопиридин, в большой концентрации выделяясь с мочой, губительно действует на бактерии, находящиеся на слизистой мочевого пузыря и в его полости, т.е. в какой-то степени обладает этиотропным эффектом. Уточнение этого вопроса – поле деятельности бактериологов.
Из современных работ по феназопиридину особое внимание привлекают две.
C. Deepalatha et al. [18] показали, что при неосложненной инфекции мочевыводящих путей применение феназопиридина совместно с антибиотиком уже через 2 сут. купирует симптомы дизурии у 91% больных. С. Б. Петров и соавт. [19] в плацебо-контролируемом исследовании установили, что применение при остром цистите однократной дозы (200 мг) феназалгина уже через 6 ч у всех больных уменьшает симптоматику, на 90% снижая боль и дискомфорт.
Согласно обзору литературы А. З. Винарова и соавт. [9], феназопиридин все шире используется в мире, причем не только при остром цистите и неосложненной инфекции нижних мочевыводящих путей, но и при цистоскопии, катетеризации мочеточника и мочевого пузыря, установке стента, бужировании уретры.
Таким образом, следует признать, что в начале XXI столетия в мире наблюдается подлинный ренессанс феназопиридина – средства, синтезированного и впервые примененного в медицине более века назад.
Заключение. Проведенное исследование показало, что препарат феназопиридина феназалгин в суммарной дозе 1200 мг, принятой в течение 2 сут., является эффективным и хорошо переносимым средством для симптоматической терапии больных острым неосложненным циститом и рекомендуется в качестве важного дополнительного средства к этиотропной антибактериальной терапии. Феназалгин обладает выраженным селективным уроанальгетическим и антидизурическим эффектом.
Комбинация антибиотика первой линии фосфомицина трометамола и уроанальгетика феназалгина улучшает результаты лечения острого неосложненного цистита у женщин, имеет клиническую эффективность (выздоровление) 97,4% и бактериологическую эффективность 96,9%, значительно быстрее и эффективнее ликвидирует боль и другие симптомы заболевания, на 30,1% сокращает сроки временной нетрудоспособности.



