Введение. Хронический простатит (ХП) остается во многом нерешенной проблемой для практикующих врачей и пациентов. Симптомы, характерные для данного заболевания, хотя бы 1 раз в жизни возникают у 35–50% мужчин, а его рецидивирующее течение имеет место у 2–16% мужчин и почти у 50% пожилых пациентов [1–4]. Недостаточная эффективность терапии и частые рецидивы ХП обусловлены его сложным патогенезом, множеством форм клинического течения и манифестации болезни, широким спектром возбудителей и противоречивыми данными по различным аспектам этиопатогенеза, диагностики и лечения [5–8].
Указанные обстоятельства диктуют необходимость изучения новых подходов к лечению этого заболевания. Одним из перспективных направлений в лечении ХП представляется озонотерапия, первоначальные результаты применения которой указывают на ее высокую эффективность. Например, в работе Ю. Ю. Винника и соавт. [9] продемонстрирована возможность значительного улучшения многих клинико-инструментальных показателей пациентов с ХП после использования озонотерапии: снижение интенсивности болевого синдрома, уменьшение выраженности дизурических расстройств, повышение качества жизни мужчины, улучшение кровотока в простатических сосудах, гормонального статуса, сексуальной и репродуктивной функций, уменьшение размеров предстательной железы и полная элиминация инфекционных агентов. Кроме того, к преимуществам методики можно отнести хорошую переносимость, низкую себестоимость и простоту применения [10–13]. Тем не менее широкое внедрение озонотерапии в клиническую практику лечения ХП сдерживается очень малым числом исследований в этой области [14, 15].
О достаточно успешном применении в лечении ХП другого исследуемого метода – магнитотерапии – свидетельствуют данные отечественных работ, в которых был отмечен присущий ей широкий спектр терапевтических эффектов: обезболивающего, противовоспалительного, рассасывающего, бактериостатического и стресслимитирующего [16–19]. Однако к настоящему времени лишь в единичных исследованиях проводилась оценка результатов комбинированного применения указанных двух лечебных факторов.
Цель исследования: оценить эффективность комплексного применения трансректальной озоно- и магнитотерапии в лечении бактериального ХП.
Материалы и методы. Исследование основано на обследовании и лечении в период с 2013 по 2018 г. 142 мужчин с бактериальным ХП (ХП-II согласно классификации Национального института здоровья США от 1995 г.). Алгоритм обследования пациентов включал оценку жалоб, сбор анамнеза болезни, физикальные методы, в том числе пальцевое ректальное исследование предстательной железы (ПЖ); анкетирование с помощью Шкалы оценки симптомов ХП Национального института здоровья США (NIH-CPSI) и Международного индекса эректильной функции (IIEF-5); общий анализ и посев мочи; 4-стаканную пробу мочи Meares–Stamey; микроскопическое и культуральное исследование секрета ПЖ и мочи, полученной после массажа ПЖ; трансректальное УЗИ (ТРУЗИ); урофлоуметрию; анализ крови на простатический специфический антиген.
Критерием установления диагноза бактериального ХП и включения пациентов в исследование служили следующие признаки:
- Наличие одного или нескольких клинических признаков:
- боли в тазовой области (промежности, половом члене, яичках, паховой области, прямой кишке, крестце, над лоном) продолжительностью не менее 3 мес.;
- расстройство мочеиспускания (учащенное мочеиспускание, чувство неполного опорожнения мочевого пузыря, слабая или прерывистая струя мочи, боль или ее усиление во время мочеиспускания);
- расстройство эякуляции (боли при/после эякуляции, гемоспермия).
- Увеличение количества лейкоцитов (более 10 в поле зрения) в секрете ПЖ или в моче, полученной после массажа ПЖ.
- Культуральное подтверждение бактериальной этиологии ХП.
- Длительность заболевания не менее 6 мес.
- Возраст от 20 до 50 лет.
- Приверженность к назначенному в рамках исследования лечению.
- Информированное согласие пациента.
Высеянный бактериальный штамм считали возбудителем ХП, если концентрация колониеобразующих единиц в секрете ПЖ или моче, полученной после массажа ПЖ, превышала таковую в первой или средней порции мочи в 10 и более раз [20].
Вся выборка пациентов, включенных в исследование, в зависимости от варианта лечения была подразделена на четыре группы (рис. 1).
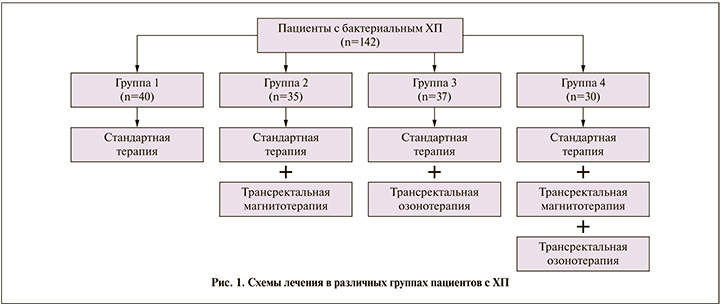
Стандартная терапия включала антибактериальные средства, α-адреноблокаторы, энзимы, витамины, микроагреганты, физиопроцедуры. Ее продолжительность составила 6 нед.
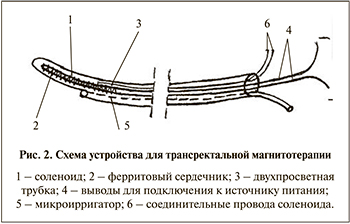 Трансректальную магнитотерапию проводили ежедневно по одному сеансу продолжительностью 15 мин в течение 10 дней с помощью устройства, предложенного сотрудниками Дагестанской государственной медицинской академии (рис. 2) [21].
Трансректальную магнитотерапию проводили ежедневно по одному сеансу продолжительностью 15 мин в течение 10 дней с помощью устройства, предложенного сотрудниками Дагестанской государственной медицинской академии (рис. 2) [21].
Данное устройство представляет собой соленоид цилиндрической формы длиной обмотки 25 мм и диаметром 4 мм. Внутри соленоида располагается ферритовый сердечник М-200-НН диаметром 2 мм и длиной 25 мм. Соленоид может работать от источника как постоянного, так и переменного тока с частотой от 20 до 1000 Гц, имеются 2 вывода для подключения к источнику питания. Устройство заливается композитом и помещается внутри двухпросветной трубки с внутренним диаметром 4 мм, внешним – 7 мм. В стенке полиэтиленовой трубки имеется микроирригатор с боковыми наружными отверстиями на уровне соленоида для введения в полость лекарственной смеси. Соединительные провода соленоида изолированы и пропущены через фторопластовый кембрик, проходящий внутри дренажной трубки. Подключение соленоида к источнику постоянного тока (батарейка-выпрямитель) с V=1,5–6В или к трансформатору переменного тока с выходным напряжением 1,5–6В позволяет создавать переменное или постоянное магнитное поле интенсивностью 9–10 мТл на концах самого соленоида.
Методика трансректальной озонотерапии. В положении лежа на боку с согнутыми и прижатыми к животу коленями в прямую кишку вводили 20 мл озонированного раствора с концентрацией озона 1200 мкг/л при длительности процедуры от 5 мин с последующим увеличением до 25 мин. Процедуру проводили 1 раз в сутки после очистительной клизмы; курс лечения включал 10 таких процедур. При этом озонированный 0,9%-ный раствор хлорида натрия получали с помощью Установки для получения озонированных растворов с заранее заданной концентрацией – ОЖК-1, или установки УОТА-60-01 «Медозон» и вводили в течение 15–20 мин после его получения.
При сочетанном применении и магнито-, и озонотерапи на первом этапе проводили магнитотерапию (10 сеансов в течение 10 дней), на втором этапе – озонотерапию (10 сеансов в течение 10 дней).
Оценку результатов проведенных видов терапии проводили через 3 мес. после окончания курса лечения.
Результаты исследования подвергнуты статистическому анализу с применением пакета прикладных программ Statistica 6.0. Количественные данные представлены в виде среднего значения (М) и стандартного отклонения (σ) (форма представления М±σ), критерии показателей микроскопического исследования секрета предстательной железы их относительной (%) и абсолютной (n) частот. Сравнение групп пациентов по различным параметрам проводили с использованием U-критерия Манна–Уитни, а динамику клинических параметров в результате лечения – критерия Вилкоксона. Различие считали статистически значимыми при уровне р менее 0,05.
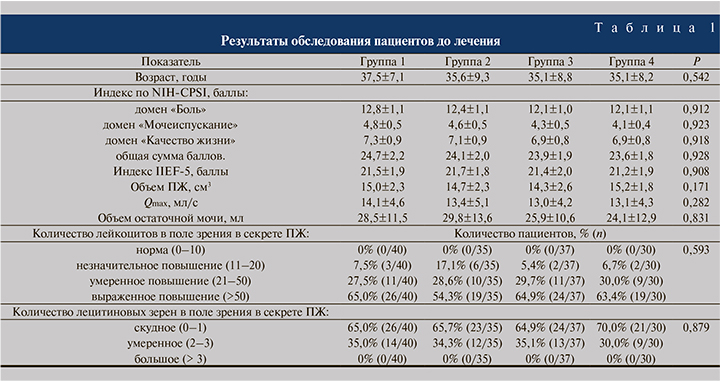
Результаты и обсуждение. Обследование пациентов до начала лечения выявило, что выделенные группы пациентов статистически значимо не различались по основным клинико-инструментальным параметрам (табл. 1). Из показателей урофлоуметрии в качестве ключевого параметра выбрана максимальная скорость мочеиспускания (Qmax).
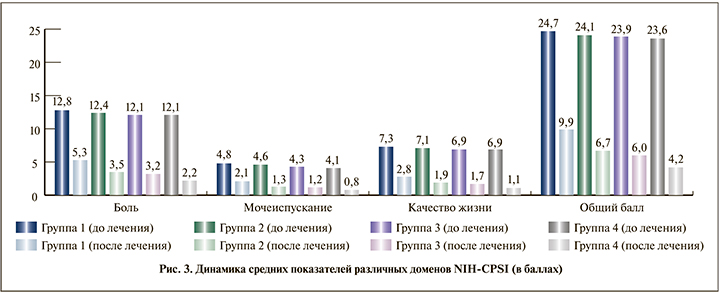
При оценке результатов установлено, что при всех вариантах лечения имело место статистически значимое (p<0,05) улучшение показателей по всем доменам анкеты NIH-CPSI (рис. 3). Однако положительная динамика в наибольшей степени была выражена среди пациентов группы 4. Так, балльная оценка по домену «Боль» в группе 1 в результате лечения снизилась на 58,6% относительно базового значения, в группе 2 – на 71,8%, в группе 3 – на 70,2%, а в группе 4 – на 81,8%; по домену «Мочеиспускание» – на 56,2; 69,6; 69,8 и 80,5%; по домену «Качество жизни» – на 61,6; 73,2; 72,5 и 82,6% соответственно. В итоге суммарный балл по анкете NIH-CPSI в группе 1 уменьшился на 58,7%, в группе 2 – на 72,2%, в группе 3 – на 71,5% и в группе 4 – на 82,2%.
Проведенное лечение во всех группах пациентов привело к улучшению эректильной функции, что было подтверждено повышением среднего значения индекса IIEF-5 (рис. 4). Однако статистически значимая (p<0,05) положительная динамика данного параметра была зарегистрирована только в группе 4. Если после курса лечения в группе 1 средний показатель индекса IIEF-5 увеличился на 5,1%, в группе 2 – на 8,3% и в группе 3 – на 7,9%, то в группе 4 – на 11,3%.
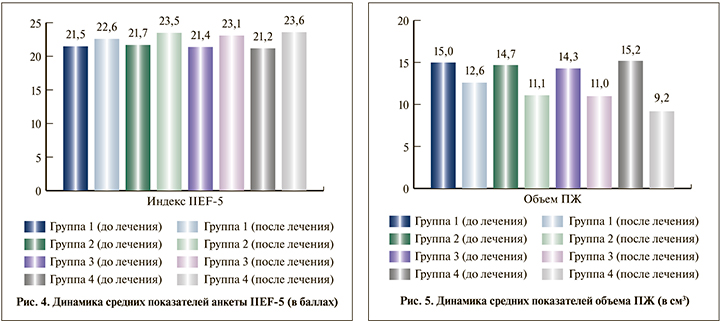
Во всех группах пациентов отмечено статистически значимое (p<0,05) уменьшение размеров ПЖ по данным ТРУЗИ (рис. 5). При этом максимально выраженное изменение данного показателя также зарегистрировано в группе 4.
У пациентов группы 1 по окончании курса лечения объем ПЖ уменьшился на 16% по сравнению с показателем до лечения, группы 2 – на 24,5%, группы 3 – на 23,1% и группы 4 – на 39,5%.
Другим положительным результатом проведенной терапии во всех группах пациентов стало достоверное (p<0,05) увеличение такого уродинамического параметра, как Qmax (рис. 6). И вновь наиболее выраженные изменения наблюдали в группе 4. В группе 1 данный показатель после лечения повысился на 30%, в группе 2 – на 53,7%, в группе 3 – на 46,9%, в группе 4 – на 74%.

Что касается такого критерия, как объем остаточной мочи, его средние значения во всех четырех группах не соответствовали клинически значимым величинам. Тем не менее результатом всех вариантов терапии ХП стало достоверное снижение этого показателя (рис. 7). Хотя наиболее выраженное уменьшение объема остаточной мочи имело место среди пациентов группы 4, выраженность снижения среднего показателя была сопоставимой во всех группах: в группе 1 он уменьшился на 12,6%, в группе 2 – на 16,8%, в группе 3 – на 15,8% и в группе 4 – на 18,3%.
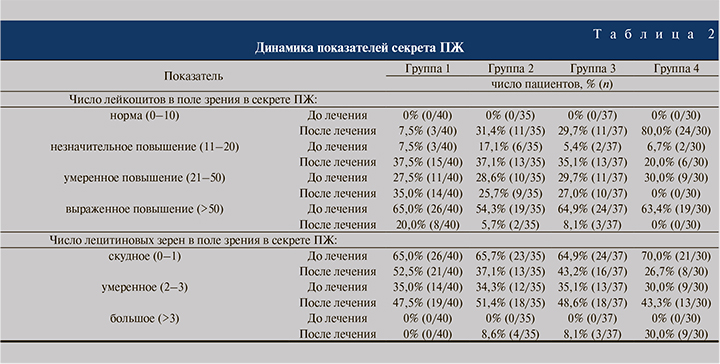
Положительный эффект от использования предложенных схем терапии был подтвержден данными микроскопического исследования секрета ПЖ. Во всех группах зафиксировано достоверное снижение доли пациентов с повышенным содержанием лейкоцитов и скудным содержанием лецитиновых зерен в секрете ПЖ. Как и в остальных случаях, наиболее существенная динамика имела место у пациентов группы 4. Так, только в этой группе после курса терапии не выявлено пациентов с умеренным и выраженным повышением числа лейкоцитов в секрете ПЖ, а доля мужчин с большим числом лецитиновых зерен достигла 30% (табл. 2).
Представленные результаты показывают, что применение пациентами с ХП любого из исследуемых факторов – магнито- и озонотерапии – позволяет добиваться более высоких результатов по сравнению с пациентами, лечение которых не предусматривает использования данных методик. При этом положительный эффект от их использования отражается практически на всех ключевых клинических параметрах. Применение обеих указанных лечебных опций приводит к еще более выраженному терапевтическому эффекту, чем при использовании только одного из них. Эффективность использованного нами подхода к лечению пациентов с ХП подтверждена результатами других отечественных работ [22; 23].
Предложенная нами тактика основана на гипотезе, согласно которой использование трансректальной магнитотерапии на первом этапе лечения обусловливает устранение эпителиальных и гнойных «пробок», вызывающих обструкцию выводных протоков ПЖ, а применение на этом фоне трансректальной озонотерапии уже на втором этапе обеспечивает оптимальную санацию патологических очагов. Установлено, что озон вступает в окислительные реакции с гнойно-некротическими тканями и, не имея способности проникать через патологические барьеры, теряет свою противовоспалительную активность [24]. Следовательно, ускорение процесса освобождения протоковой системы от гнойных «пробок» является очень важным моментом, так как, чем быстрее ПЖ будет дренирована, тем эффективнее можно достигать санации органа. В связи с этим именно магнитное низкочастотное излучение способно ускорять процесс очищения тканей от микрофлоры и гнойно-некротических масс и сокращать сроки репарации тканей. Данный эффект происходит вследствие ориентации биологически активных макромолекул и жидких кристаллов, составляющих основу многих внутриклеточных структур, после воздействия на них магнитных полей. Магнитные поля, в отличие от других физиотерапевтических факторов, легко проникают на большую глубину тканей, при этом не выделяя тепла, обладают следовым характером воздействия [25].
Заключение. Трансректальное применение таких лечебных факторов, как магнито- и озонотерапия, позволяет добиваться существенного улучшения результатов лечения пациентов с бактериальным ХП. При этом максимальный терапевтический эффект проявляется при комплексном поэтапном применении обоих методов. Патогенетически оправданным представляется использование магнитотерапии на первом этапе лечения, озонотерапии – на втором. Высокая эффективность, дешевизна и сравнительная простота использования служат важным аргументом в пользу рассмотрения указанных методов в качестве перспективных направлений оптимизации результатов лечения пациентов данной категории. Дальнейшие исследования в этой области, в том числе по оценке отдаленных результатов применения магнито- и озонотерапии, должны окончательно определить роль и место указанных методов в лечении бактериального ХП.



