Введение. Доброкачественная гиперплазия предстательной железы (ДГПЖ) и эректильная дисфункция (ЭД) входят в число заболеваний, оказывающих наиболее значимое влияние на состояние здоровья и качество жизни мужчин старше 50 лет. Между этими заболеваниями установлена прямая корреляция, которая с возрастом только усиливается [1–3]. Так, было выявлено, что в каждом из возрастных диапазонов 50–59, 60–69 и 70–79 лет существует отчетливая тенденция к повышению частоты ЭД по мере увеличения выраженности симптомов нижних мочевыводящих путей (СНМП), обусловленных ДГПЖ [4]. Помимо этого существуют данные, свидетельствующие об общности многих механизмов патогенеза этих двух заболеваний [5, 6]. Такая ассоциация ДГПЖ и ЭД обусловливает необходимость разработки общих подходов к ведению пациентов с сочетанием данных заболеваний. В связи с этим особый интерес представляют пациенты с высоким риском прогрессирования ДГПЖ (объем предстательной железы (Vprostate)>40 см3 и уровень простатического специфического антигена (ПСА)>1,5 нг/мл). В разряд рекомендованных препаратов для данной категории пациентов входят ингибиторы 5α-редуктазы [7]. Однако последние оказывают негативное влияние на сексуальную функцию мужчин. Это обстоятельство диктует необходимость изучения возможности компенсирования неблагоприятного воздействия на эректильную функцию ингибитора 5α-редуктазы с помощью ингибитора фосфодиэстеразы 5-го типа (ФДЭ-5). Отмеченное в работах последних лет положительное влияние ингибитора ФДЭ-5 еще и на СНМП служит дополнительным аргументом в пользу использования данного класса препаратов в различных схемах терапии таких пациентов [8–13]. На возможную высокую эффективность и безопасность различных вариантов комбинированной терапии мужчин с ДГПЖ в сочетании и без ЭД указывает ряд исследователей [14–16]. Однако недостаточная изученность отмеченных сторон данной проблемы обусловливает необходимость продолжения дальнейших исследований в этой области, что и подтверждает актуальность нашей работы.
Цель исследования: оценить эффективность и безопасность различных вариантов медикаментозного лечения пациентов с высоким риском прогрессирования доброкачественной гиперплазии предстательной железы (ДГПЖ) в зависимости от сопутствующей эректильной дисфункции (ЭД).
Материалы и методы. Исследование основано на обследовании 293 мужчин с симптомами ДГПЖ, проведенном с 2012 по 2016 г. Критериями включения пациентов в исследование стали: Vprostate>40 см3; уровень ПСА 1,5–4,0 нг/мл; показатель по Международной системе суммарной оценки заболеваний предстательной железы (IPSS) ≥8 баллов; максимальная скорость мочеиспускания (Qmax) более 5 мл/с и менее 15 мл/с; отсутствие в анамнезе медикаментозного (в течение предшествующих 6 мес.) и хирургического лечения по поводу ДГПЖ; отсутствие абсолютных показаний к хирургическому лечению ДГПЖ; приверженность к назначенному в рамках исследования медикаментозному лечению в течение 3 мес. и более; информированное согласие пациента. Критериями исключения служили: гиперактивный мочевой пузырь по данным комплексного уродинамического исследования; морфологически подтвержденный рак предстательной железы; воспалительные заболевания органов мочеполовой системы в стадии обострения; наличие в анамнезе оперативных вмешательств по поводу стриктуры уретры и заболеваний мочевого пузыря; неврологические расстройства, влияющие на функции накопления и опорожнения мочевого пузыря, сопутствующие заболевания в стадии суб- и декомпенсации; индивидуальная непереносимость и наличие противопоказаний к одному из исследуемых лекарственных препаратов.
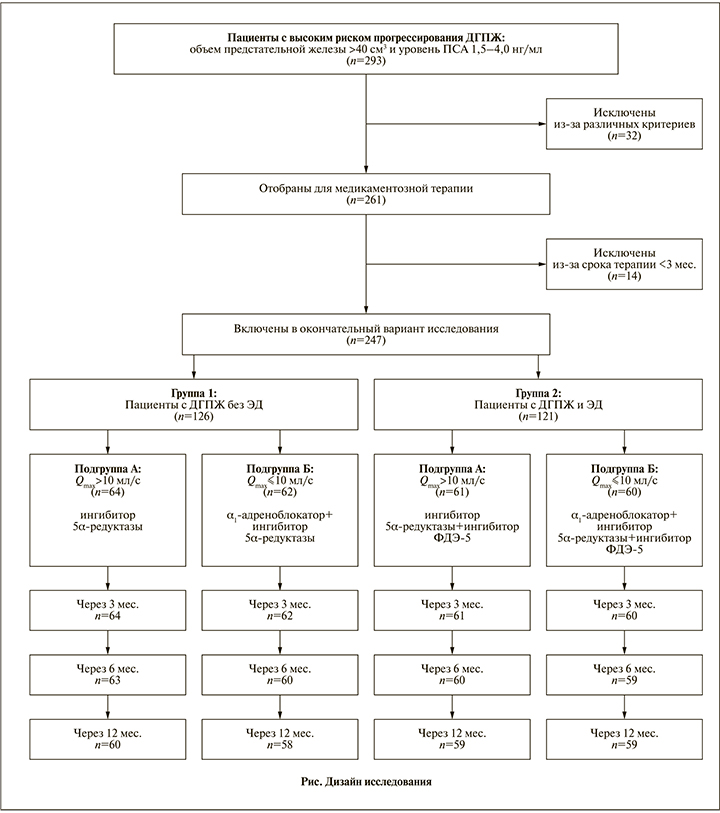
Пациенты были разделены на две группы. Группу 1 составили пациенты с ДГПЖ без ЭД (>21 балла по анкете IIEF-5), группу 2 – мужчины с ДГПЖ и ЭД (≤21 балла по анкете IIEF-5). Внутри каждой группы выделены две подгруппы: подгруппа А – пациенты со слабовыраженной обструктивной симптоматикой (Qmax>10 мл/с); подгруппа Б – пациенты с выраженной обструктивной симптоматикой (Qmax≤10 мл/с). Пациенты подгруппы А группы 1 получали ингибитор 5α-редуктазы, подгруппы Б группы 1 – α1-адреноблокатор и ингибитор 5α-редуктазы, подгруппы А группы 2 – ингибитор 5α-редуктазы и ингибитор фосфодиэстеразы 5-го типа (ФДЭ-5), подгруппы Б группы 2 – α1-адреноблокатор, ингибитор 5α-редуктазы и ингибитор ФДЭ-5. При указанных режимах фармакотерапии из α1-адреноблокаторов использован тамсулозин в дозе 0,4 мг ежедневно в течение 12 мес., ингибиторов 5α-редуктазы – дутастерид в дозе 0,5 мг ежедневно в течение 12 мес., ингибиторов ФДЭ-5 – силденафил в дозе 25 мг «по требованию» в течение 12 мес.
Контроль результатов терапии проводили через 3, 6 и 12 мес. В эти сроки объем выборки пациентов был различный, так как часть пациентов в силу разных причин выбыла из исследования (см. рисунок).
Перед началом лечения и в указанные выше сроки после начала терапии исследовали следующие параметры: показатель IPSS, качество жизни (QoL) по IPSS, уровень ПСА, Qmax, Vprostate, объем остаточной мочи (Vres) и показатель IIEF-5.
Статистическую обработку данных проводили с помощью программы StatSoft STATISTICA v. 10.0. При сравнении групп пациентов использовали U-критерий Манна–Уитни, при сопоставлении групп по динамике клинических параметров – критерий Вилкоксона. Различие между сравниваемыми группами считали статистически значимыми при значениях р<0,05.
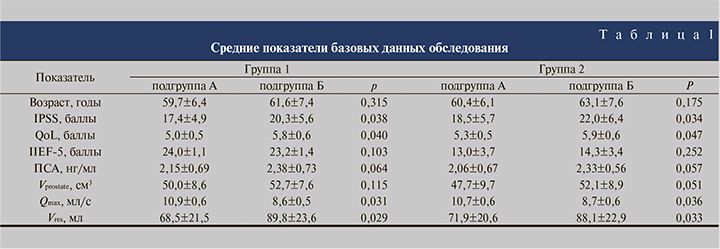
Результаты и обсуждение. Сопоставление подгрупп в каждой группе до начала медикаментозного лечения статистически значимых различий по какому-либо признаку не выявило (табл. 1).
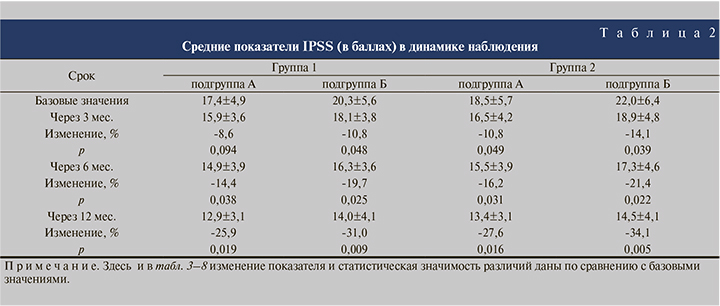
Среди пациентов группы 1 улучшение СНМП в виде достоверного снижения показателя IPSS наступило при первом контрольном обследовании, т.е. через 3 мес. лечения, тогда как монотерапия ингибитором 5α-редуктазы обеспечила такой результат через 6 мес. терапии. В обеих подгруппах пациентов группы 2 отмечено статистически значимое уменьшение показателя IPSS на первом контрольном визите (табл. 2). Вероятно, дополнительное включение в схему лечения ингибитора ФДЭ-5, положительно влияющего на течение СНМП, привело к такому эффекту в более ранние сроки, чем у аналогичной подгруппы А пациентов группы 1.
Аналогичная закономерность прослежена и в динамике показателей QoL. Во всех подгруппах пациентов, кроме подгруппы с монотерапией ингибитором 5α-редуктазы, начиная с 3-го месяца отмечено статистически значимое снижение величин QoL. По выраженности уменьшения индекса QoL лучшие результаты показала комбинированная терапия, включившая 3 класса лекарственных препаратов (табл. 3).

Характерная для ингибиторов 5α-редуктазы способность снижать концентрацию ПСА проявилась практически в одинаковой мере во всех выделенных категориях пациентов, и в каждой из них уровень ПСА снизился через 12 мес. примерно на 50% от базового значения независимо от выбранного варианта терапии (табл. 4).
При всех использованных подходах к лечебной тактике отмечено статистически значимое уменьшение показателей Vprostate начиная с 3-го месяца терапии, когда было выполнено первое контрольное обследование. Этот факт объясняется редукцией железистой ткани предстательной железы вследствие подавления образования дигидротестостерона из тестостерона за счет действия ингибитора 5α-редуктазы [17]. При этом наличие или отсутствие остальных классов лекарственных препаратов практически не оказывало никакого влияния на динамику этого параметра (табл. 5).

На первом сроке мониторинга (через 3 мес. от начала терапии) достоверное улучшение значений Qmax констатировали во всех подгруппах, за исключением подгруппы А группы 1 с монотерапией ингибитором 5α-редуктазы. Эффективность ингибитора 5α-редуктазы в монорежиме в статистически значимом масштабе была реализована только ко второму контрольному сроку наблюдения – по прошествии 6 мес. лечения. Такой результат подтвердил тезис о том, что значимый лечебный эффект ингибиторов 5α-редуктазы в отношении СНМП начинает проявляться, как правило, спустя 6 мес. непрерывного применения. Добавление α1-адреноблокатора и/или ингибитора ФДЭ-5 к ингибитору 5α-редуктазы в двух- либо трехкомпонентной терапии оказывает более выраженное положительное влияние на динамику показателей Qmax по сравнению с монотерапией ингибитором 5α-редуктазы (табл. 6).
Уменьшение показателя Vres является одним из ключевых критериев улучшения СНМП. В период медикаментозного лечения для значений показателя Vres также была характерна положительная динамика, как и для критериев IPSS, QoL и Qmax. Кроме подгруппы пациентов, получавшей ингибитор 5α-редуктазы в моноварианте, во всех остальных подгруппах пациентов отмечено прогрессивное снижение показателя Vres от начала и до конца периода наблюдения. Что касается эффективности монотерапии ингибитором 5α-редуктазы, то при таком варианте через 6–12 мес. достигнуто существенное уменьшение показателя Vres. При этом трехкомпонентная схема терапии обеспечила наиболее выраженное улучшение данного параметра (табл. 7).

В обеих подгруппах группы 1 отмечено ухудшение среднего значения IIEF-5, что связано с негативным эффектом ингибитора 5α-редуктазы на половую функцию и развитием у небольшой части пациентов ЭД. Однако по выборке пациентов группы 1 в целом такая отрицательная динамика показателей IIEF-5 не носила статистически значимый характер. Что касается группы 2, то использование ингибитора ФДЭ-5 в каждом из вариантов терапии закономерно привело к достоверному улучшению эректильной функции, начиная с первого контрольного срока обследования (табл. 8).
За весь период наблюдения различные побочные эффекты диагностированы у 16,2% (40/247) пациентов: у 14,1% (9/64) – подгруппы А группы 1, у 16,1% (10/62) – подгруппы Б группы 1, у 14,8% (9/61) – подгруппы А группы 2, у 18,3% (11/60) – подгруппы Б группы 2 (табл. 9). По доле пациентов, у которых возникло осложнение, значимого различия между всеми подгруппами не установлено (p=0,106). Из-за побочных эффектов 7 пациентов выбыли из исследования. Так как у ряда пациентов имело место сочетание нескольких видов нежелательных реакций, общее число побочных явлений превышает количество пациентов с наличием осложнений медикаментозной терапии.

В отношении тех 9 (7,1%) пациентов группы 1, у которых после 12 мес. вышеуказанной терапии вследствие негативного эффекта ингибитора 5α-редуктазы возникла ЭД, в течение последующих 3 мес. был использован ингибитор ФДЭ-5 силденафил 25 мг в режиме «по требованию». Данная тактика обеспечила восстановление сексуальной функции до базового уровня, что подтверждено данными анкеты IIEF-5. Статистические расчеты по оценке достоверности отмеченной динамики показателей IIEF-5 не проведены в связи с малым числом таких наблюдений. Тем не менее указанная положительная динамика эректильной функции на фоне применения ингибитора ФДЭ-5 дает основание предположить, что возникающие в ходе терапии ингибитором 5α-редуктазы нарушения половой функции достаточно успешно могут быть купированы с помощью ингибитора ФДЭ-5. В связи с этим перспективными представляются дальнейшие исследования возможностей такого лечебного подхода на более крупных выборках аналогичной категории пациентов.
Базовый уровень IIEF-5 у группы 1 через 12 мес. после лечения ингибиторами 5α-редуктазы снизился с 23,4 до 15,2. Однако после назначения ингибиторов ФДЭ-5 в течение 3 мес. в режиме «по требованию» показатели IIEF-5 увеличились до 22,9.

Таким образом, наши результаты подтвердили, что комбинация ингибитора 5α-редуктазы и α1-адреноблокатора пациентам с высоким риском прогрессирования ДГПЖ без ЭД обеспечивает в целом лучшие результаты по купированию СНМП, чем монотерапия с помощью ингибитора 5α-редуктазы, при сопоставимой частоте побочных эффектов фармакотерапии. Такой результат был достигнут, несмотря на более выраженный базовый уровень обструктивной симптоматики по критерию Qmax среди пациентов, получавших комбинированное лечение. Возникающие у небольшой части пациентов нарушения сексуальной функции могут быть успешно разрешены путем добавления в схему терапии ингибитора ФДЭ-5 в комбинированную терапию. Таким образом, полученные нами данные продемонстрировали возможности различных подходов к улучшению результатов лечения названной категории пациентов и открыли перспективы дальнейших научных изысканий в этой области, что позволит оптимизировать исходы лечения мужчин с ДГПЖ.
Относительно терапии пациентов с ДГПЖ в сочетании с ЭД получены такие же закономерности, что были выявлены в единичных работах, посвященных изучению результатов различных вариантов комбинированной терапии, включавших ингибитор 5α-редуктазы и ингибитор ФДЭ-5. Так, A. Casabé et al. [14] сообщили, что после комбинации «тадалафил 5 мг+финастерид 5 мг» динамика показателей IPSS и IIEF через 4, 12 и 26 нед. была достоверно лучше, чем после монотерапии финастеридом 5 мг, при сопоставимой частоте побочных эффектов. В другом исследовании не обнаружено существенных различий между комбинациями «ингибитор 5α-редуктазы+ингибитор ФДЭ-5» и «α1-адреноблокатор+ингибитор 5α-редуктазы» по динамике значений IPSS, Qmax и Vres в течение 12 нед. лечения, хотя терапия с включением ингибитора ФДЭ-5 продемонстрировала явные преимущества по коррекции ЭД, согласно IIEF [15].

Первый опыт трехкомпонентной лекарственной терапии пациентов с СНМП и ЭД отражен в работах А. А. Волкова и соавт., опубликованных в разные годы [16, 18, 19]. Авторы отметили, что добавление ингибитора ФДЭ-5 к комбинации α1-адреноблокатора с ингибитором 5α-редуктазы как в режиме постоянного приема, так и «по требованию» позволяет достигать прогрессивного улучшения эректильной функции и регресса СНМП. Однако следует понимать, что такая практика была основана на небольшом объеме выборки пациентов (21 человек) и сроках наблюдений от 3 до 9 мес.
Отмеченная в нашей работе успешность комбинированных схем фармакотерапии не сопровождалась значимым ростом частоты побочных эффектов, что служит весомым аргументом в пользу широкого внедрения в практику лечения пациентов с ДГПЖ и ЭД многокомпонентных методик лечения, включающих ингибитор ФДЭ-5 как обязательный элемент таких схем. Хотя сроки применения указанных вариантов терапии в нашей работе в целом были выше, чем в других аналогичных исследованиях, нужно понимать, что окончательные выводы о необходимости рутинного внедрения всех описанных подходов преждевременны.
Заключение. Для пациентов с высоким риском прогрессирования ДГПЖ с объемом предстательной железы более 40 см3 и уровнем ПСА выше 1,5 нг/мл без сопутствующей ЭД наиболее эффективным вариантом лечения следует признать двухкомпонентную схему терапии, включающую α1-адреноблокатор и ингибитор 5α-редуктазы. При этом негативное влияние последнего класса препаратов на половую функцию мужчин успешно может быть компенсировано посредством применения ингибитора ФДЭ-5. У пациентов с сочетанием ДГПЖ и ЭД включение ингибитора ФДЭ-5 в любую комбинацию (двух- либо трехкомпонентную) обеспечивает существенное улучшение эректильной функции вкупе с положительной динамикой СНМП. При этом многокомпонентные схемы терапии не сопровождаются значимым увеличением частоты побочных реакций. Однако необходимо учитывать, что окончательные выводы о преимуществе указанных подходов возможны только после набора достаточного клинического материала, так как на современном этапе подобный опыт слишком мал. Тем не менее все названные комбинированные схемы медикаментозного лечения с включением ингибитора 5α-редуктазы можно расценивать как перспективный подход к лечению таких пациентов, что требует продолжения дальнейших научных исследований в этом направлении.



