В 1976 г. Fernstrom и Johansson впервые предложили новую технику чрескожного удаления камней почки. К настоящему времени благодаря непрерывному техническому прогрессу при выборе метода лечения нефролитиаза перкутанная нефролитотрипсия (ПНЛ) практически полностью вытеснила открытые операции. Согласно клиническим рекомендациям Российского общества урологов, а также Европейской и Американской урологических ассоциаций, ПНЛ является «золотым» стандартом лечения крупных и коралловидных конкрементов почек [1–3]. Однако важно понимать, что перкутанная хирургия не лишена осложнений. При этом частота их развития напрямую зависит от многих факторов, в том числе от характеристик самого камня. Так, вероятность возникновения интраоперационных осложнений при удалении коралловидных камней значительно выше, чем при перкутанном лечении некоралловидных камней [4]. А полнота удаления камня почки (Stone Free Rate – SFR), по данным исследовательской группы эндоурологического общества (CROES), после ПНЛ при коралловидном нефролитиазе составляет 56,9%, тогда как у пациентов с некоралловидными камнями достигает 82,5% [5].
Важным, но редко обсуждаемым врачом и пациентом является проблема завышенных ожиданий пациента по поводу полноты удаления камней из почки, а также проблема вероятности развития осложнений. Поэтому в процессе принятия решения о выборе метода оперативного лечения необходимо использовать различные вспомогательные инструменты. Номограммы предсказания эффективности ПНЛ, аудиовизуальная информация и обучающие брошюры – все это помогает в общении между врачом и пациентом, а также положительно влияет на ожидания пациентов [6, 7].
Чтобы прогнозировать потенциальные осложнения, связанные с ПНЛ, необходимо оценивать индивидуальные особенности пациента, камня и анатомию почки. При подготовке к операции нужно проводить тщательную оценку соматического статуса пациента с определением индекса массы тела. Компьютерная томография (КТ) мочевыводящих путей является «золотым» стандартом определения характеристик конкремента и адекватной оценки анатомии полостной системы почки [8]. Она дает информацию о расстоянии от кожи до камня, расположении органов брюшной полости, размере и плотности конкремента, стереолитометрии, а также о ширине шеек чашечек, через которые осуществляется перкутанный доступ. В большинстве случаев целесообразно выполнять контрастную КТ с таким же расположением пациента, как на планируемой операции (на животе или на спине) [6].
1. Классификация осложнений ПНЛ
Все осложнения во время хирургических манипуляций должны быть описаны и задокументированы в соответствии с классификацией Clavien–Dindo [9] (см. таблицу). Вероятность возникновения осложнений после ПНЛ довольно высока и достигает 83%, но большинство из них относится к «малым» осложнениям. «Большие» осложнения должны быть вовремя определены и корректным образом устранены, их вероятность возникновения составляет 1,1–7% [10].

По времени возникновения осложнения разделяют на интраоперационные и послеоперационные. Интраоперационные осложнения включают кровотечение, повреждение собирательной системы почки, повреждение органов брюшной полости, легких и плевры, тромбоэмболические осложнения, экстраренальную миграцию конкремента, а также некорректную установку нефростомического дренажа. К послеоперационным осложнениям относят развитие инфекции и сепсиса, кровотечение, персистирующий мочевой свищ, возникновение инфундибулярного стеноза и смерть пациента. Отсутствие достижения SFR после операции мы не считаем осложнением ПНЛ, так как этот показатель относится к эффективности оперативного лечения [11].
2. Интраоперационные осложнения ПНЛ
2.1. Кровотечение
Оценка осложнения
Выполнение стандартной ПНЛ ассоциируется с высоким риском развития интраоперационного кровотечения.
В первую очередь это связано с большим диаметром используемого перкутанного кожуха Amplatz (обычно это 24–30 Шр) [12], а также с необходимостью создания дополнительных доступов для достижения SFR. Вероятность возникновения острого кровотечения, требующего переливания крови, находится в диапазоне от 0,8 до 20%. Более того, активное манипулирование ригидным нефроскопом во время ПНЛ может травмировать паренхиму почки и перешеек чашечки и привести к увеличению интенсивности кровотечения. Кровопотеря во время операции часто остается недооцененной, и предполагаемый урологом объем кровопотери часто не соответствует истине.
Эффективность использования гемостатической губки и герметиков во время ПНЛ не доказана [13]. Если во время операции визуализация снижена или отсутствует из-за развившегося кровотечения, необходимо увеличить приток ирригационной жидкости, так как достижение SFR напрямую зависит от эндоскопической видимости. При этом в случае развития гипотензии операция должна быть остановлена и предприняты соответствующие меры.
Лечение
Изменение положения кожуха Amplatz может приводить к тампонаде мелких сосудов паренхимы почки и улучшать визуализацию. В отсутствие эффекта от этого приема улучшить видимость во время ПНЛ может помочь использование транексамовой кислоты, которая кроме этого приводит к снижению продолжительности операции на 22 мин и объема ирригационной жидкости на 5,5 л. После транексамовой кислоты необходимо рассмотреть возможность установки внутреннего стента, так как кровяные сгустки в чашечно-лоханочной системе (ЧЛС) лизируются значительно дольше и могут вызывать обструкцию [14].
В случае продолжающегося активного венозного кровотечения необходимо установить нефростому большого диаметра (>18 Шр) или тампонирующую нефростому и перекрыть ее по крайней мере на 10–60 мин, что обеспечит тампонаду кровоточащих сосудов. Если возникает активное артериальное кровотечение, развивается гипотензия, может быть применен специальный баллонный нефростомический катетер Kaye 36 Шр. После его установки в экстренном порядке должна быть проведена селективная эмболизация поврежденных сосудов в условиях рентген-интервенционного отделения. Большинство кровотечений во время ПНЛ удается остановить описанными выше консервативными методами, эмболизации кровоточащих сосудов требуют менее 1,5% пациентов [15].
В крайнем случае, если ангиоэмболизация оказалась неэффективной, необходимо прибегнуть к наложению швов на поврежденную паренхиму почки или выполнить резекцию поврежденной части органа, а при неудаче провести нефрэктомию.
Для снижения риска кровотечения во время ПНЛ целесообразно использовать инструменты меньшего диаметра [16] а также выполнять перкутанный доступ в ЧЛС исключительно через сосочек чашечки.
2.2. Повреждение полостной системы почки
Оценка осложнения
 Повреждение ЧЛС во время ПНЛ встречается у 8–10% пациентов [17]. Обычно это связано с чрезмерно глубоким проведением бужа или некорректной манипуляцией ригидным нефроскопом. Возникающая в результате повреждения экстравазация и абсорбция больших объемов ирригационной жидкости может приводить к электролитным нарушениям, изменению ментального статуса и гипергидратации организма. К интраоперационным признакам повреждения полостной системы почки относят экстравазацию контрастного вещества во время флюороскопии, визуализацию перинефральной жировой ткани при нефроскопии, развитие гемодинамических изменений, а также уменьшение объема оттекающей ирригационной жидкости. Компьютерная томография с контрастным усилением в раннем послеоперационном периоде помогает вовремя диагностировать мочевой затек (рис. 1).
Повреждение ЧЛС во время ПНЛ встречается у 8–10% пациентов [17]. Обычно это связано с чрезмерно глубоким проведением бужа или некорректной манипуляцией ригидным нефроскопом. Возникающая в результате повреждения экстравазация и абсорбция больших объемов ирригационной жидкости может приводить к электролитным нарушениям, изменению ментального статуса и гипергидратации организма. К интраоперационным признакам повреждения полостной системы почки относят экстравазацию контрастного вещества во время флюороскопии, визуализацию перинефральной жировой ткани при нефроскопии, развитие гемодинамических изменений, а также уменьшение объема оттекающей ирригационной жидкости. Компьютерная томография с контрастным усилением в раннем послеоперационном периоде помогает вовремя диагностировать мочевой затек (рис. 1).
Лечение
Было доказано, что доступ в почку под эндоскопическим контролем снижает вероятность возникновения осложнений, связанных с чрезмерной дилатацией нефростомического хода. Так, по данным Khan et al., использование этого метода позволяет выполнять прецизионную пункцию с последующей дилатацией, что в свою очередь снижает вероятность повреждения ЧЛС [17]. Однако у пациентов с коралловидным нефролитиазом гибкий эндоскоп может не достигать желаемой чашечки. Небольшая экстравазация при незначительном повреждении полостной системы почки чаще всего не требует прекращения оперативного вмешательства. При перфорации лоханки почки или обширном повреждении ЧЛС необходимо закончить операцию и установить нефростомический дренаж или мочеточниковый стент как минимум на 5–7 дней. Использование специализированного клея для закрытия дефекта ЧЛС не рекомендовано [18].
2.3. Повреждение органов брюшной полости
2.3.1. Печень
Оценка осложнения
Повреждение печени во время ПНЛ — довольно редкое осложнение, которое может остаться нераспознанным. Высокий риск повреждения печени (до 14%) отмечается при правостороннем межреберном доступе (выше 11-го ребра) кпереди от задней подмышечной линии. При гепатомегалии риск повреждения печени выше [10]. В послеоперационном периоде пациенты могут описывать необычное жжение в правой половине живота. С помощью КТ можно оценить траекторию пункции и область повреждения печени (рис. 2). Предотвратить повреждение печени помогает ультразвуковое сканирование в области предполагаемой пункции.
Лечение
Если состояние пациента гемодинамически стабильно, никакого вмешательства не требуется. Консервативное лечение включает тщательное наблюдение за пациентом и использование гемостатических препаратов. Рекомендуется более длительное дренирование ЧЛС нефростомой для самопроизвольного заживления поврежденной ткани печени [10]. Наш опыт показывает, что более эффективной тактикой по сравнению с установкой только нефростомы является удаление нефростомического катетера и дренирование ЧЛС с помощью внутреннего стента. В дополнение к этому в мочевой пузырь по уретре должен быть установлен катетер Фолея на 24–48 ч для обеспечения адекватного дренажа мочевыводящих путей. В послеоперационном периоде на 5–6-е сутки показано выполнение УЗИ или КТ для исключения формирования биломы [19].
2.3.2. Селезенка
Оценка осложнения
Данные о серьезных повреждениях селезенки публикуются редко, и провести истинную оценку их частоты довольно сложно [20]. К настоящему времени описано всего 11 подобных случаев [10]. Селезенка расположена вдоль длинной оси 10-го ребра с левой стороны в непосредственной близости от переднелатеральной поверхности левой почки. Таким образом, создание перкутанного доступа с левой стороны в 10-м межреберье или наличие спленомегалии у пациента значительно повышает риск повреждения селезенки. Если ПНЛ была проведена слева с высоким межреберным доступом и у пациента возникла гипотония без признаков выраженного кровотечения, необходимо в первую очередь заподозрить травму селезенки. Ввиду массы симптомов, которые могут возникать непосредственно после ПНЛ или в течение нескольких дней после операции, вовремя выявить повреждение селезенки иногда бывает трудно. После стабилизации гемодинамических показателей необходимо проводить КТ брюшной полости для оценки объема повреждения.
 Лечение
Лечение
Гемодинамически стабильным пациентам с выявленным с помощью КТ повреждением селезенки рекомендован строгий постельный режим. Также можно оставить нефростому на более долгий срок для заживления раны и снижения риска массивного кровотечения [21]. Гемодинамически нестабильным пациентам необходимо выполнять ушивание селезенки или производить спленэктомию в экстренном порядке (рис. 3). Остановить кровотечение и сохранить селезенку может помочь использование гемостатической губки [22]. При стандартной ПНЛ в положении на животе снизить риск повреждения селезенки помогает пункция ЧЛС по задней подмышечной линии, а также применение ультразвукового сканирования.
2.3.3. Толстый кишечник
Оценка осложнения
Повреждение толстого кишечника во время ПНЛ диагностируют менее чем в 1% случаев [10]. Обычно толстая кишка располагается кпереди от почки, но в 0,6% случаев встречается ее ретроренальное расположение [23], чаще всего с левой стороны, где интимно прилегает к нижнему сегменту почки. Наличие ретроренальной толстой кишки и/или выполнение слишком латеральной пункции служат основным фактором риска повреждения толстого кишечника во время ПНЛ [24].
Как правило, повреждение толстой кишки выявляется при антеградной пиелографии уже после установки нефростомического катетера. Если повреждение толстого кишечника было выявлено интраоперационно или в раннем послеоперационном периоде до удаления нефростомы, эффективность консервативного лечения составляет 86%. Вероятность самопроизвольного закрытия дефекта кишечной стенки снижается до 50% при установке диагноза спустя длительное время после операции и уже удаленной нефростоме [25].
Симптомами, позволяющими заподозрить перфорацию толстой кишки, являются необъяснимая лихорадка, диарея или гематохезия, симптомы перитонита, отхождение кишечных газов или кала по нефростомическому катетеру [25]. Компьютерная томография брюшной полости – лучший способ диагностики перфорации толстого кишечника (рис. 4). Чтобы предотвратить повреждение толстой кишки, необходимо выполнять ультразвуковое сканирование в области предполагаемой пункции.
Лечение
При выявлении экстраперитонеальной перфорации толстой кишки в первую очередь необходимо разобщить кишечно-почечный свищ. С помощью внутреннего стента выполняют дренирование почки, а нефростому под флюо-
роскопическим контролем подтягивают и устанавливают в забрюшинное пространство. В мочевой пузырь устанавливают катетер Фолея для предупреждения пузырно-мочеточникового рефлюкса. Консервативное лечение включает разгрузку кишечника (парентеральное питание) и применение антибиотиков широкого спектра действия. Через 5–7 дней терапии проводят рентгеноконтрастное исследование. Основанием для удаления мочепузырного и нефростомического катетеров служит отсутствие экстравазации контрастного вещества по данным колостографии или ретроградной урографии или признаков формирования кишечно-почечного свища. При возникновении толстокишечно-кожного свища может потребоваться формирование колостомы. При интраперитонеальном повреждении, перитоните, сепсисе или неэффективности консервативного лечения показана лапаротомия с колостомией [24].
2.3.4. Желчный пузырь
Оценка осложнения
Повреждение желчного пузыря при ПНЛ является редким, но потенциально очень опасным осложнением, требующим ранней диагностики. Из-за трудностей с постановкой диагноза повреждение желчного пузыря чаще выявляется после развития желчного перитонита. По данным
H. Öztürk et al., описано 8 случаев повреждения желчного пузыря [10]. Сочетание медиального правостороннего чрескожного доступа к почке с увеличенным желчным пузырем повышает риск повреждения последнего, особенно у астеничных пациентов [26]. Аспирация зеленоватой жидкости из пункционной иглы служит признаком повреждения желчных путей. Пациент с развивающимися перитонеальными признаками в раннем послеоперационном периоде должен быть экстренно обследован на предмет повреждения желчного пузыря.
Лечение
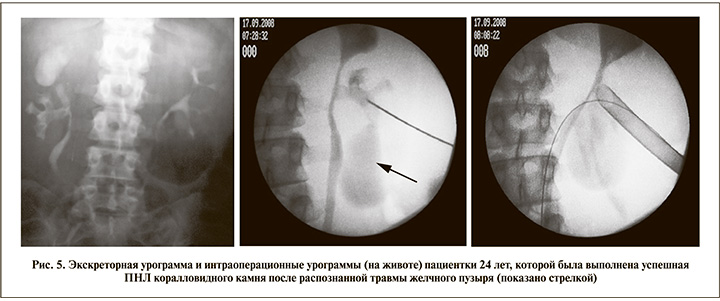
Семерым из восьми описанных пациентов с повреждением желчного пузыря во время ПНЛ потребовалась холецистэктомия [10]. В единственном случае на фоне консервативного лечения произошло самопроизвольное заживление перфорации желчного пузыря (рис. 5). Пациенты с подозрением на повреждение желчного пузыря после операции требуют тщательного наблюдения. При ухудшении состояния пациента показана немедленная холецистэктомия из-за угрозы развития перитонита и сепсиса. Избежать перфорации желчного пузыря во время выполнения пункции ЧЛС позволяет комбинированный ультразвуковый и флюороскопический контроль.
2.3.5. Повреждение тонкого кишечника
Оценка осложнения
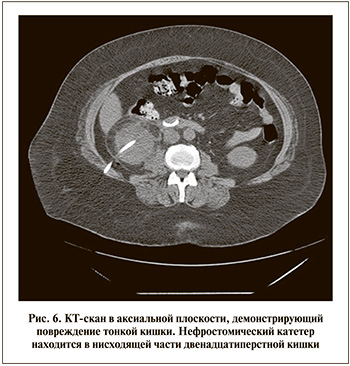 С учетом интраперитонеального расположения тонкой кишки она, как правило, находится на безопасном расстоянии от почки и риск ее повреждения во время ПНЛ чрезвычайно низок. Повреждение тонкой кишки обычно возникает при правосторонней ПНЛ на этапе пункции или дилатации пункционного хода [27]. Чаще всего повреждаются нисходящая и горизонтальная части двенадцатиперстной кишки, поскольку они ближе всего расположены к нижнему сегменту правой почки (рис. 6) [24]. Обычно перфорация возникает из-за чрезмерного продвижения иглы или инструмента и малой подвижности двенадцатиперстной кишки. Пиелография в конце операции обычно позволяет выявлять любое повреждение тонкой кишки. Появление жидкости янтарного цвета в отделяемом из нефростомического дренажа может быть следствием повреждения тонкой кишки, для дифференциальной диагностики которого необходимо проверить в ней уровень билирубина и креатинина.
С учетом интраперитонеального расположения тонкой кишки она, как правило, находится на безопасном расстоянии от почки и риск ее повреждения во время ПНЛ чрезвычайно низок. Повреждение тонкой кишки обычно возникает при правосторонней ПНЛ на этапе пункции или дилатации пункционного хода [27]. Чаще всего повреждаются нисходящая и горизонтальная части двенадцатиперстной кишки, поскольку они ближе всего расположены к нижнему сегменту правой почки (рис. 6) [24]. Обычно перфорация возникает из-за чрезмерного продвижения иглы или инструмента и малой подвижности двенадцатиперстной кишки. Пиелография в конце операции обычно позволяет выявлять любое повреждение тонкой кишки. Появление жидкости янтарного цвета в отделяемом из нефростомического дренажа может быть следствием повреждения тонкой кишки, для дифференциальной диагностики которого необходимо проверить в ней уровень билирубина и креатинина.
Лечение
При повреждении тонкого кишечника обычно выполняют лапаротомию с ушиванием дефекта кишки [10]. Однако на сегодняшний день описано три случая консервативного лечения. В двух случаях лечение перфорации тощей кишки заключалось в длительном голодании с переводом на тотальное парентеральное питание в течение 10 и 21 дня соответственно [27]. В третьем случае успешно проведено эндоскопическое клипирование дефекта стенки двенадцатиперстной кишки [28].
2.4. Повреждение органов грудной клетки
Оценка осложнения
Пневмоторакс, гидроторакс, гемоторакс и уриноторакс (уроторакс) – редкие осложнения ПНЛ, общая частота которых не превышает 2% [29]. Выявлено, что надреберный доступ (выше 12-го ребра) [30], а также ПНЛ с левой стороны [31] связаны с более высокой частотой торакальных осложнений. Повреждения органов грудной клетки возникают в 10 и 25% случаев, когда доступ осуществляется выше 12-го и 11-го ребер соответственно [32]. Данные предоперационной КТ позволяют урологам определять оптимальное место для пункции ЧЛС, а также ее взаимоотношение с плеврой. Во избежание травмы плевры при надреберном доступе может быть использована техника смещения почки [33]. Если все же был осуществлен надреберный чрескожный доступ, нужно обязательно выполнять обзорную рент-
генографию органов грудной клетки (желательно в положении стоя) в раннем послеоперационном периоде.
Лечение
При бессимптомном пневмо- или гемотораксе небольшого объема пациент может находиться только под наблюдением. Однако при появлении признаков легочной недостаточности или нестабильном состоянии в экстренном порядке должно быть проведено дренирование плевральной полости; оно должно быть выполнено в экстренном порядке. Нефроплевральный свищ может проявляться в любое время с момента завершения операции вплоть до двух недель. Основным симптомом является укороченное дыхание. Диагноз обычно устанавливают по данным пиелографии. Чаще всего свищ самопроизвольно закрывается после разделения верхних мочевыводящих путей и плевральной полости соответствующими дренажами [34].
2.5. Тромбоэмболические осложнения
Оценка осложнения
Тромбоз глубоких вен встречается у 1–3% пациентов после ПНЛ [35]. Его можно заподозрить у пациентов с припухлостью, покраснением или болью в нижних конечностях. Выявить тромбоз глубоких вен нижних конечностей позволяет УЗИ с допплерографией [36].
Лечение
Антикоагулянты препятствуют распространению тромботических масс. Однако применение кроворазжижающих препаратов сопряжено с риском кровотечения, поэтому назначать их следует с осторожностью и только в случае длительного стояния нефростомы и/или отсутствия признаков кровотечения в послеоперационном периоде.
2.6. Эмболия легочной артерии
Оценка осложнения
Эмболия легочной артерии – очень редкое, но фатальное осложнение ПНЛ. Чаще всего оно связано с использованием воздуха под давлением во время пиелографии (при так называемом двойном контрастировании [37]) или возникает у пациентов с внутрисердечным шунтированием кровотока, например при дефекте межпредсердной или межжелудочковой перегородки [38]. Эмболия легочной артерии проявляется гипоксией, брадикардией, гиперкапнией или остановкой сердца. Интраоперационно воздушную эмболию легочной артерии можно выявить по данным эхокардиографии.
Лечение
Если есть подозрение на развитие эмболии легочной артерии, необходимо немедленно прекратить ПНЛ и уложить пациента на левый бок. Установка центрального венозного катетера позволяет проводить аспирацию пузырьков воздуха. В послеоперационном периоде пациенту могут потребоваться кардиопульмональный мониторинг, инотропная поддержка, интенсивная терапия. Если есть признаки вовлечения ЦНС, может быть эффективным применение гипербарической оксигенации [38]. Чтобы минимизировать риск воздушной эмболии легочной артерии, не рекомендуется использовать воздух для пиелографии во время ПНЛ.
2.7. Экстраренальная миграция конкремента и инородные тела после ПНЛ
Оценка осложнения
Экстраренальная миграция камня – относительно редкое осложнение после ПНЛ. Очень важно документировать подобные случаи и указывать в выписной справке. Обычно миграция камня происходит при применении чрезмерного давления зондом во время литотрипсии, наличии перфорации полостной системы почки или нарушении техники экстракции фрагментов конкремента через кожух Amplatz. Определить наличие конкрементов за пределами ЧЛС позволяет интраоперпационная пиелография или УЗИ.
 В ходе ПНЛ может происходить отрыв части катетера, струны-проводника или поломка экстрактора (рис. 7) или зонда для литотрипсии. Диагностика данного вида осложнений несложна и заключается в макроскопической оценке сломанного инструмента и рентгенологическом контроле с определением локализации отломков.
В ходе ПНЛ может происходить отрыв части катетера, струны-проводника или поломка экстрактора (рис. 7) или зонда для литотрипсии. Диагностика данного вида осложнений несложна и заключается в макроскопической оценке сломанного инструмента и рентгенологическом контроле с определением локализации отломков.
Лечение
При неинфекционных конкрементах или камнях, не вызывающих обструкции мочевых путей, никакого лечения обычно не требуется. Эндоскопическое удаление мигрировавших фрагментов, выявленных интраоперационно, обычно не вызывает каких-либо трудностей, но в ряде случаев может приводить к увеличению размера перфорации. В литературе были также описаны случаи интраперитонеальной [39] и внутриплевральной [40] миграций фрагментов конкрементов. В этих ситуациях может потребоваться использование лапаро- или торакоскопии для предупреждения развития осложнений.
Инородные тела в почке или забрюшинном пространстве удаляют с помощью литоэкстрактора под рентгенологическим и эндоскопическим контролем.
2.8. Некорректная установка нефростомического катетера
Оценка осложнения
Установка нефростомического катетера в почечную вену является очень редким осложнением. На сегодняшний день опубликовано всего 13 случаев. Это осложнение, как правило, случается на этапе бужирования, при котором развивается массивное кровотечение, требующее незамедлительной остановки операции и установки наспех нефростомического катетера [41].
Лечение
В отношении большинства гемодинамически стабильных пациентов можно ограничиться консервативным лечением, которое включает строгий постельный режим и антибактериальную терапию. В таких случаях удаление нефростомы необходимо выполнять под контролем КТ или флюороскопии. Иногда удалять нефростомический дренаж приходится в условиях операционной с привлечением рентгенэндоваскулярных хирургов, готовых к проведению экстренной эмболизации в случае развития кровотечения. Открытая операция может потребоваться как альтернативный метод остановки кровотечения.
3. Послеоперационные осложнения
3.1. Инфекционные осложнения и сепсис
Оценка осложнения
Инфекция мочевыводящих путей после ПНЛ возникает у 25–37% пациентов [42], чаще у больных коралловидным нефролитиазом, и может приводить к развитию сепсиса в 0,3–7,6% случаев [43].
Уросепсис – это жизнеугрожающее состояние, которое может служить причиной смерти в 66–80% случаев [44]. Более чем у 60% пациентов коралловидные камни возникают из-за активности уреазопродуцирующих бактерий, поэтому ПНЛ коралловидного нефролитиаза вызывает особенное беспокойство из-за высокой вероятности развития инфекционных осложнений.
В дополнение к этому сложная конфигурация коралловидных камней может потребовать создания множественных стандартных (> 24 Ch) перкутанных трактов, которые ассоциируются с более высоким риском кровотечения и повышением вероятности гемотрансфузии. Как дополнительные доступы, так и периоперационное переливание компонентов крови значительно повышают риск послеоперационных септических осложнений. По данным некоторых исследований [45], сахарный диабет и женский пол также служат фактором риска инфекционных осложнений.
Значительный лейкоцитоз и лихорадка в послеоперационном периоде являются поводом для беспокойства и показанием к проведению антибактериальной терапии. Полезным для выявления значимой послеоперационной инфекции считается определение уровня прокальцитонина и лактата в крови.
Лечение
Пациентам с коралловидным камнем предположительно инфекционного происхождения антибактериальная терапия должна проводиться в течение минимум 1 нед. до операции. Пациентам низкой группы риска с отрицательным предоперационным посевом мочи без мочевых дренажей достаточно проведения стандартной однократной антибиотикопрофилактики. Если при пункции ЧЛС получена гнойная моча, следует установить нефростомическую трубку и прекратить операцию. Отделяемое из нефростомы необходимо направить на бактериологическое исследование, а пациенту назначить антибактериальные препараты широкого спектра действия и наблюдать до получения результатов посева. Пациентам группы высокого риска развития инфекции (реконструктивные операции на мочевыводящих путях в анамнезе, рецидивирующая инфекция мочевыводящих путей), для того чтобы минимизировать риск развития сепсиса после ПНЛ, целесообразна предоперационная установка нефростомы за 7–10 дней до ПНЛ с антибиотикотерапией по результатам посева мочи [46].
Во время дробления инфекционного камня целесообразно отправлять его образец для культурального исследования, поскольку бактерии в камне и в моче могут различаться [47]. Пациенты этой группы должны находиться под пристальным наблюдением, включая мониторинг жизненно важных функций, лабораторных показателей и психического статуса. При подозрении на уросепсис пациента необходимо немедленно перевести в отделение интенсивной терапии для проведения инфузионной и антибактериальной терапии, поддерживающего лечения, включая стероиды и/или вазопрессоры. Пациенты, не отвечающие на эту интенсивную терапи, могут страдать дополнительной патологией, включая нераспознанные травмы (которые могут быть выявлены с помощью визуализационных методов диагностики) или грибковые инфекции (особенно пациенты с ослабленным иммунитетом, сахарным диабетом или с длительно стоящими мочевыми дренажами) [48].
3.2. Послеоперационное кровотечение
Оценка осложнения
Раннее послеоперационное кровотечение (<24 ч) обычно встречается в следующих вариантах: кровотечение по нефростомическому катетеру, кровотечение из перкутанного тракта после удаления нефростомического катетера и перинефральное кровоизлияние с формированием гематомы, которое следует подозревать при отсутствии выраженной гематурии, снижении уровня гемоглобина и гематокрита, а также при нарастающей боли в боку. КТ позволяет обнаруживать большую перинефральную гематому. Отсроченное послеоперационное кровотечение, которое возникает через 1–3 нед. после ПНЛ, является редким осложнением (1,2%) [49] и может быть связано с формированием артериовенозной фистулы или псевдоаневризмы.
Лечение
Венозное кровотечение из нефростомического катетера может быть остановлено путем пережатия нефростомы на 1–2 ч. Кровотечение из перкутанного тракта можно остановить пальцевым прижатием или сдавлением, положив один кулак на спину, другой — на живот пациента [50]. Перинефральное кровоизлияние обычно отграничено и лечится консервативно: строгий постельный режим и переливание компонентов крови по мере необходимости. Неконтролируемое кровотечение с падением уровня гемоглобина (>40 г/л) и/или нестабильная гемодинамика служат показанием к неотложному вмешательству (эмболизация/резекция/нефрэктомия).
 Отсроченное кровотечение обычно возникает из-за формирования артериовенозной фистулы или псевдоаневризмы. В этом случае пациенту может потребоваться ангиография с суперселективной эмболизацией (рис. 8). Если консервативные меры, в том числе селективная ангиоэмболизация, неэффективны, в качестве крайней меры можно прибегнуть к открытому хирургическому вмешательству, вплоть до нефрэктомии [50].
Отсроченное кровотечение обычно возникает из-за формирования артериовенозной фистулы или псевдоаневризмы. В этом случае пациенту может потребоваться ангиография с суперселективной эмболизацией (рис. 8). Если консервативные меры, в том числе селективная ангиоэмболизация, неэффективны, в качестве крайней меры можно прибегнуть к открытому хирургическому вмешательству, вплоть до нефрэктомии [50].
3.3. Формирование персистирующего мочевого свища
Оценка осложнения
Вероятность формирования персистирующего мочевого свища составляет 1,5–4,6%. Нефростомический тракт обычно закрывается в течение 6–12 ч после удаления нефростомического катетера [51]. Длительное подтекание мочи по нефростомическому свищу (24 ч) требует дообследования. Рекомендуется выполнить КТ или урографию для исключения резидуальных камней, которые могут вызывать обструкцию.
Лечение
В большинстве случаев для самопроизвольного закрытия нефростомического свища достаточно установить мочеточниковый стент. В некоторых случаях показано дополнительное дренирование мочевого пузыря катетером Фолея, который устанавливается на 24–48 ч для борьбы с пузырно-мочеточниковым рефлюксом.
3.4. Инфундибулярный стеноз
Оценка осложнения
Послеоперационный инфундибулярный стеноз представляет собой редкое осложнение (менее 2%) ПНЛ, связанное с затяжным воспалительным процессом, который предположительно вызывает фиброз и формирование рубцов с постепенной облитерацией просвета перешейка чашечки. К рентгенологическим признакам инфундибулярного стеноза относятся расширенная чашечка или чашечки в сочетании с нерасширенной почечной лоханкой. К факторам риска развития инфундибулярного стеноза относятся коралловидный нефролитиаз, а также размер нефроскопа, который может быть непропорционально велик по отношению к диаметру перешейка чашечки, что в свою очередь может стать причиной его разрыва [52].
Лечение
Лечение при инфундибулярном стенозе обычно эндоскопическое (антеградным или ретроградным доступом), несмотря на то что эффективность операции составляет всего 60–80% [53]. Используют рассечение холодным ножом [54], лазерную аблацию [55], баллонную дилатацию или эндоскопическое формирование нового перешейка чашечки. Если ни один из этих методов не приносит результата, можно оставить пациента под динамическим наблюдением при условии бессимптомного течения и отсутствия признаков снижения функции почки [52].
К альтернативным методам лечения относят перманентное стентирование, резекцию почки или геминефрэктомию.
3.5. Смертность
Смерть после ПНЛ является крайне редким осложнением. В когорте из 1406 пациентов уровень смертности составил лишь 0,2% [56], который напрямую связан как с индексом коморбидности Charlson (CCI), так и с продолжительностью операции [57]. Основной причиной летальных исходов после ПНЛ служит сепсис. К факторам риска относятся множественные сопутствующие заболевания, а также пациенты с повреждением спинного мозга [57]. Пациентам с высоким риском смерти необходимо проводить надлежащее предоперационное обследование, а также информировать о возможных вариантах исхода.
Перкутанная нефролитотрипсия – достаточно безопасная операция с известным набором осложнений, своевременное выявление и лечение которых позволят избегать серьезных последствий для пациента. Большинство осложнений ПНЛ не требует оперативного лечения и может быть разрешено консервативно.



