Введение. Под термином «эректильная дисфункция» (ЭД) понимают продолжающуюся более 3 мес. неспособность достижения или поддержания эрекции, достаточной для проведения полового акта. Это определение применимо к широкому спектру состояний различной степени выраженности: от частичной недостаточности эрекции перед эякуляцией до полной ее утраты, что ведет к невозможности осуществления полового акта [1]. По разным оценкам, около 90 млн мужчин во всем мире страдают нарушением эрекции различной степени тяжести [2].
В Российской Федерации данное заболевание выявляется у 48,9% мужчин в возрасте 20–77 лет. Так, ЭД легкой степени выраженности встречается у 34,6% мужчин, 7,2% имеют заболевание средней степени выраженности, у 7,1% пациентов выявляется тяжелая степень ЭД. В зависимости от патогенеза ЭД выделяют следующие формы заболевания: психогенная, на долю которой приходится около 40% случаев; органическая – в 29% случаев, в 25% случаев причина ЭД сочетает как органический, так и психологический фактор и рассматривается как смешанная форма ЭД. Также выделяют ЭД неясного генеза, на долю которой приходится 6% [3].
Распространенность ЭД в популяции и ее негативное влияние на нормальную физиологию мужской репродуктивной системы, а также угнетение психо-эмоцианального состояния свидетельствуют о необходимости подробного изучения данного заболевания [4]. Помимо этого известно, что диагностика и лечение ЭД могут приводить к обнаружению некоторых угрожающих жизни состояний, которые в противном случае могли остаться не диагностированными. Так, артериогенная форма ЭД является ранним проявлением системной сосудистой патологии, в основе которой лежит эндотелиальная дисфункция, что ассоциировано с наличием скрытой ишемической болезни сердца [5].
Одним из основных факторов риска развития ЭД является возраст. Еще в 1948 г. Kinsey и соавт., обследовав 15 781 мужчину в возрасте до 80 лет, установили, что частота ЭД среди мужчин 55–65 лет составляет 25%, у мужчин моложе 30 лет – всего 1% [6]. Это объясняется тем, что с возрастом все системы органов и механизмы регуляции организма претерпевают ряд изменений. Исследование, проведенное H. S. Ahn и соавт., показало, что существует положительная корреляция между уровнем свободного тестостерона и нарушениями эрекции и эякуляции [7]. Помимо этого с возрастом в половом члене происходят значительные структурно-функциональные изменения. Коллагеновые и эластические волокна белочной оболочки являются основным элементом, обеспечивающим увеличение толщины и длины полового члена во время эрекции. Исследования биоптатов полового члена продемонстрировали, что количество эластических волокон с возрастом снижается, что в свою очередь приводит к снижению эластичности белочной оболочки и играет важную роль в патогенезе ЭД у пожилых людей [8]. Кроме того, имеются данные о том, что у мужчин старше 60 лет на 35 % снижается количество гладкомышечных клеток в половом члене. Уменьшение соотношения гладкомышечная/соединительная ткань в половом члене ведет к повышению риска венозной утечки, следовательно, к недостаточно стойкой эрекции, а также к риску окклюзии вен полового члена, что ассоциировано с таким патологическим состоянием, как приапизм [9]. Развитию ЭД также способствует снижение количества коллагена типа III, увеличение количества коллагена типа I. Ученые предполагают, что нарушение содержания коллагеновых и эластических волокон служит первичным фактором в развитии ЭД, а в дальнейшем приводит к хронической ишемии пещеристых тел, которая является причиной гибели части гладкомышечных клеток [10].
Таким образом, можно утверждать, что возрастные гормональные изменения и структурно-функциональная перестройка полового члена лежат в основе патогенеза ЭД [11].
В настоящее время для клинической оценки ЭД используется анкета – Международный индекс эректильной функции (МИЭФ-5), которая состоит из пяти вопросов, позволяющих оценивать эректильную функцию мужчины [12]. Не менее значимым для врача-уролога является оценка течения ЭД: так, для органического компонента заболеваня характерно прогрессирующее нарастание симптомов, тогда как для психологической формы заболевания характерно резкое нарушение копулятивной функции без видимых на то причин. Важными этапами в диагностике состояния являются физикальный осмотр и лабораторная диагностика, включающая общий анализ мочи и крови, биохимическое исследования крови и оценку гормонального статуса. Наиболее распространенным и доступным методом инструментальной диагностики выступает ультразвуковое и допплерографическое исследования полового члена, позволяющие выявлять признаки фиброза кавернозных тел, нарушение артериального кровотока или наличие патологического венозного сброса [13, 14].
На сегодняшний в лечении ЭД активно применяются как консервативная терапия, так и оперативные методики для коррекции данного заболевания. Препаратами первой линии выступают ингибиторы фосфодиэстеразы 5-го типа (ФДЭ-5): тадалафил, силденафил, варденафил, уденафил. Данные лекарственные средства могут быть назначены при всех формах ЭД, а их эффективность подтверждена множеством исследований [15, 16]. Механизм действия ингибиторов ФДЭ-5 основан на релаксации гладкой мускулатуры, приводящей к вазодилатации и последующей эрекции.
В отсутствие эффекта от применения пероральных форм могут быть назначены интракавернозные инъекции алпростадила.
Длительное применение интракавернозных инъекций ассоциировано с фиброзом кавернозной ткани, а также пролонгированной эрекцией и развитием такого неотложного состояния, как приапизм [17].
У пациентов с непереносимостью медикаментозной терапии альтернативным методом лечения могут выступать вакуумные эректоры, применение которых обусловливает нефизиологичную эрекцию. Для этого половой член помещают в специальное устройство (колбу), в котором создается отрицательное давление, обусловливающее приток крови к пещеристым телам. Для сохранения эрекции накладывают специальное кольцо, ограничивающее венозный отток крови. Важно проинформировать пациентов о возможности развития подкожных кровоизлияний и затруднения эякуляции [18].
В добавление к медикаментозному лечению может назначаться физиотерапия, а именно ударно-волновая терапия, действие которой основано на влиянии акустических волн на пещеристую ткань полового члена, что приводит к неоваскуляризации в кавернозных телах [19].
При неэффективности консервативной терапии может быть предложена фаллопластика с протезированием. Несмотря на наличие современных методик фаллопротезирования и непрерывно развивающуюся в данном направлении хирургию, не могут быть исключены и такие серьезные осложнения, как протезная инфекция, эрозивные дистальные поражения полового члена, S-образная пенильная деформация при несоответствии размеров пенильных имплантатов и кавернозных тел [20]. Именно поэтому важно максимально пролонгировать этап медикаментозной терапии до оперативного вмешательства и прибегать к последнему лишь при наличии строгих показаний.
На современном фармацевтическом рынке появились ингибиторы ФДЭ-5 в таблетированной форме, диспергируемые в полости рта, что облегчает прием медикаментов: не требует наличия воды, сублингвальная форма обладает более выраженной биодоступностью, а эффект от приема наблюдается быстрее.
Актуальность и широкая распространенность проблемы диктуют необходимость поиска не только эффективного, но и более удобного для применения препарата.
Цель исследования: оценить эффективность и безопасность диспергируемой формы силденафила («Риджамп» 50 мг) по сравнению со стандартной таблетированной формой препарата силденафил (50 мг).
Материалы и методы. В настоящее проспективное клиническое исследование были включены 60 мужчин в возрасте от 27 до 67 лет (средний возраст – 40,2 года) с умеренной ЭД (11–15 баллов, по данным опросника МИЭФ-5). Все больные проходили обследование и получали лечение амбулаторно в клинико-диагностическом центре ФГБОУ ВО ПСПбГМУ им. акад. И.П. Павлова Минздрава России.
Критерием включения в исследование стала подтвержденная по результатам опросника МИЭФ-5 ЭД умеренной степени выраженности.
Информированное согласие было подписано всеми участниками исследования. Получено одобрение локального этического комитета на проведение исследования.
Критерии исключения: анатомическая деформация полового члена (болезнь Пейрони); заболевания, предрасполагающие к развитию приапизма (серповидно-клеточная анемия, множественная миелома, лейкоз, тромбоцитемия); нестабильная стенокардия, перенесенные за последние 6 мес. инфаркт миокарда, инсульт или жизнеугрожающие аритмии, артериальная гипертензия (АД >170/100 мм рт. ст.).
На первом визите проведен сбор жалоб и анамнеза, физикальный осмотр пациентов с целью выявления заболеваний наружных половых органов. Все мужчины заполняли опросник МИЭФ-5. Проведен клинический минимум: общий анализ мочи, клинический и биохимический анализ крови. Далее при помощи автоматизированного генератора случайных чисел все мужчины были разделены на две группы: в группе I (n=30) пациенты принимали диспергируемую форму препарата силденафил, 50 мг («Риджамп») за 60 мин до полового акта; в группе II (n=30) была назначена стандартная форма препарата силденафил в дозировке 50 мг за 60 мин до полового акта.
Повторный визит назначен через 4 нед. с целью оценки эффективности и безопасности терапии.
Все полученные данные вносились в специальную исследовательскую карту. Расчет и статистический анализ результатов исследования проводились при помощи программы STATISTICA 10.0. Количественные переменные описывали следующими статистическими методами: число валидных случаев, среднее арифметическое значение (М), стандартное отклонение от среднего арифметического значения (σ). Качественные переменные описывали абсолютными и относительными частотами (процентами). Различия считали статистически значимыми при уровне ошибки p<0,05. Для оценки динамики изменения данных, выраженных количественными показателями, использовали методы статистического анализа: непарный t-критерий Стьюдента, непараметрические критерии Манна–Уитни.
Результаты. По прошествии 4 нед. от начала терапии все пациенты были приглашены на повторный визит с целью оценки эффективности и переносимости назначаемого препарата. Результаты представлены в табл. 1.

Из табл. 1 видно, что положительная динамика, по данным анкетирования, наблюдалась во всех исследуемых группах, что свидетельствует об эффективности любой формы силденафила. Так, в группе I прирост баллов составил 53,85%, тогда как в группе II – 50% (p<0,05). При этом статистически значимых различий между группами не наблюдалось.
Посредством опроса пациента установлено количество половых актов и их длительность до начала медикаментозной терапии и после нее (табл. 2).
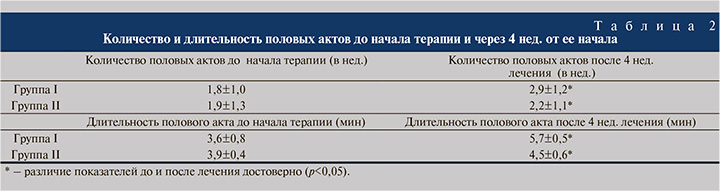
В ходе второго визита установлено среднее время начала действия препарата: в группе I – 45±2,2 (мин) , тогда как в группе II – 51±1,9 (мин).
В основной группе (группа I) – 1 (3,33%) пациент предъявил жалобы на возникновение стойкой головной боли после приема препарата, в связи с чем отказался от подобранной терапии. В группе сравнения (группа II) – 1 (3,33%) пациент сообщил о диспепсических расстройствах на фоне приема препарата, 1 (3,33%) пациент – о головокружении. Однако данные нежелательные явления не повлекли за собой отмены препарата.
Всеми пациентами основной группы отмечено удобство приема препарата «Риджамп», отсутствие необходимости запивать его водой, что облегчает его применение вне зависимости от обстановки.
Обсуждение. Как было сказано ранее, препаратами первой линии в лечении ЭД являются ингибиторы ФДЭ-5. Силденафил – первое лекарственным средство, которое появилось на фармацевтическом рынке в 1998 г. [21]. Эффективность и безопасность препарата подтверждена большим количеством как отечественных, так и зарубежных исследований. При этом лекарственное средство может быть назначено не только мужчинам без заболеваний других систем органов, но и людям с отягощенным анамнезом. Так, по результатам работы, проведенной FDA, более 3700 мужчин получали силденафил для купирования ЭД и почти 2000 получали плацебо. При этом 25% пациентов страдали артериальной гипертонией и принимали препарат на фоне антигипертензивной терапии. Полученные результаты свидетельствовали о том, что частота серьезных сердечно-сосудистых осложнений была одинаковой в группе силденафила и плацебо, что делает возможным назначение препарата пациентам с сердечно-сосудистыми заболеваниями [22].
Goldstein и соавт. при исследовании эффективности силденафила в дозировке 50 мг у пациентов с сахарным диабетом сообщают о 52%-ном улучшении эректильной функции по сравнению с группой плацебо [23].
В нашем исследовании проведена сравнительная оценка двух лекарственных форм препарата силденафил, а именно форма, диспергируемая в ротовой полости («Риджамп») и таблетированная форма. Эффективность обеих форм препарата, оцениваемая по опроснику МИЭФ-5, оказалась сопоставимой. При этом в основной группе (группа I) зафиксировано увеличение количества половых актов. Со слов пациентов, отсутствие визуального сходства диспергируемой формы силденафила с обычной формой препарата, а также возможность не употреблять воду помогли избежать затруднительного положения перед половым партнером.
Лекарственный препарат, поступивший в организм сублингвально, всасывается значительно быстрее благодаря высокой васкуляризации ротовой полости. Попадая в системный кровоток через систему верхней полой вены, вещество не подвергается инактивации печеночными ферментами, а также влиянию кислой среды и пищеварительных ферментов ЖКТ [24].
Таким образом, назначение диспергируемой лекарственной формы позволяет добиться более быстрого наступления терапевтического эффекта, повысить уровень удобства и лёгкости применения препарата, что является оптимальным выбором при лечении ЭД.
Выводы. Полученные нами результаты свидетельствуют о сопоставимой эффективности диспергрируемой формы силденафила (группа I) и стандартной таблетированной формы препарата (группа II), однако частота нежелательных явлений ниже при сублингвальном приеме. Также важно отметить, что все пациенты основной группы (группа I) отметили более быстрое начало действия препарата, а также удобство его использования и возможность принимать лекарственное средство без приема воды.



