Киста простатической маточки (англ.: prostatic utricle cyst), или срединная киста простаты, – дивертикулоподобное образование, располагающееся в предстательной железе по средней линии и имеющее сообщение с задней уретрой в области семенного бугорка. По данным литературы, у взрослых пациентов простатическая маточка может клинически проявляться рецидивирующей инфекцией мочевыводящих путей, образованием камней в полости кисты, эпидидимитами, бесплодием, а также неопластическими изменениями ее стенки [1]. Выявление кисты простатической маточки в детском возрасте чаще связано с пороками развития уретры и полового члена, такими как проксимальные формы гипоспадии, а также с рецидивирующими инфекциями нижних мочевых путей.
Киста простатической маточки является эмбриологическим остатком Мюллерового протока, не редуцированного полностью на фоне пониженного уровня тестостерона плода на 9–10-й неделе гестации, когда происходит формирование уретры [1–6]. Как свидетельствуют данные эмбриологических исследований, краниальная часть предстательной железы происходит из Мюллеровых протоков, а каудальный сегмент имеет смешанное происхождение из Мюллеровых и Вольфовых протоков, а также урогенитального синуса. При дифференцировке эмбриона по женскому типу Мюллеровы каналы дают начало фаллопиевым трубам, матке и проксимальной части влагалища, тогда как у эмбрионов мужского пола под действием антимюллерового гормона (АМН) Мюллеровые протоки регрессируют. Урогенитальный синус, который развивается в дистальную треть влагалища у девочек, не тропен АМН, а у мальчиков маскулинизируется в ответ на повышение уровня тестостерона [5, 7, 8], формируя так называемую простатическую маточку — слепой карман в предстательной железе, открывающийся в мочеиспускательный канал щелевидным отверстием на верхушке семенного бугорка. В связи с этим при гистологическом исследовании кисты выстилки кисты определяются плоскоклеточный эпителий (Мюллеровые протоки), кубоидальный эпителий и переходный эпителий (Вольфовы протоки и урогенитальный синус) [5, 7]. Снижение концентрации тестостерона или отсутствие гормональной чувствительности тканей на стадии, когда урогенитальная пластинка, сформированная из нередуцированных Мюллеровых протоков, вступает в контакт с урогенитальным синусом, приводит к образованию кистозной полости, сообщающейся с задней уретрой, т.е. в кисте простатической маточки [1, 6, 9].
Фактическую распространенность аномально увеличенной простатической маточки установить трудно, так как скорее всего у большинства пациентов она никак клинически не проявляется [1, 8, 10].
В педиатрической практике выявление кисты, как было отмечено выше, чаще связано с пороками развития уретры и полового члена. По данным литературы, аномально увеличенная простатическая маточка ассоциируется с гипоспадией и встречается у 11–14 % пациентов с проксимальной формой гипоспадии и до 57–75 % — с промежностной [2, 4, 11]. Также сообщается и о других ассоциированных пороках урогенитального тракта: односторонней агенезии почки, клапанах задней уретры, пузырно-мочеточниковом рефлюксе, крипторхизме [8]. Кисты простатической маточки больших размеров могут вызывать очень редкое осложнение, ретроградную эякуляцию, когда сперма не выходит из уретры, а попадает в мочевой пузырь [12].
Рецидивирующие инфекции мочевыводящих путей являются основным клиническим проявлением. Застой мочи в полости кисты приводит к размножению микроорганизмов, образованию конкрементов и подтеканию мочи, так как устье простатической маточки находится ниже сфинктерного аппарата. Описаны случаи пиурии у пациентов с кистой простатической маточки [8]. У оперированных пациентов с гипоспадией подтекание инфицированной мочи в большинстве случаев приводит к несостоятельности швов неоуретры и неудовлетворительным результатам. Выявляемое у ряда пациентов бесплодие, по всей видимости, связано с компрессией семявыносящих протоков аномально увеличенной маточкой [8, 13]. Неопластические изменения описаны у 3% пациентов с кистой простатической маточки с пиковой частотой около четвертого десятилетия жизни [1]. В связи с этим в проанализированных нами публикациях авторы рекомендуют раннее хирургическое лечение.
Киста простатической маточки больших размеров у пациентов педиатрического профиля может быть выявлена при трансабдоминальном УЗИ в виде позадипузырного жидкостного образования [4, 7]. В отношении взрослых пациентов можно использовать трансректальное ультразвуковое сканирование для визуализации простаты и параректальной клетчатки [6, 8]. Не потеряла актуальности и уретроцистография [4, 8, 14, 15]. Из неинвазивных диагностических процедур наиболее информативной представляется МРТ, которая обеспечивает многоплоскостную визуализацию взаимоотношения полости кисты, мочевого пузыря и органов малого таза [8, 14–17]. Выполнение МСКТ также позволит выявить наличие дополнительной жидкостной структуры по средней линии в позадипузырном пространстве [8–14]. Некоторые клиники имеют возможность использовать трансуретральное УЗИ для диагностики урогенитальной патологии, в том числе и кистозных образований простаты [12].
Методом, позволяющим поставить окончательный диагноз, является цистоскопия, которая позволяет визуально обнаружить отверстие под семенным бугорком, ведущее в полость кисты с гладкой стенкой и эпителием, напоминающим нормальный уротелий. Полость, как правило, заполнена мутной мочой и мелкими конкрементами [1, 4, 6–8].
В список заболеваний для дифференциальной диагностики наряду с кистой простатической маточки необходимо включать кисты Мюллеровых протоков, дивертикул мочевого пузыря, кисту семенного пузырька. Труднее всего дифференцировать кисту простатической маточки и кисты Мюллерового протока, так как они имеют схожие эмбриологию, клинику и данные визуализации, являясь срединными внутрипростатическими кистами, однако последние, как правило, не связаны с предстательной железой. Они имеют круглую форму и часто встречаются у взрослых (20–40 лет) мужчин с нормальными наружными гениталиями. Киста простатической маточки имеет трубчатую или везикулярную форму и чаще всего выявляется у мужчин до 20 лет с пороками развития урогенитального тракта и всегда имеет сообщение с уретрой [4, 8, 18].
В литературе описано консервативное лечение кисты простатической маточки, которое включает применение антибактериальной терапии, уросептиков и катетеризацию кистозной полости с промыванием или без, а также одномоментную аспирацию содержимого под контролем трансректального УЗИ, однако консервативный подход не всегда эффективен [8].
В настоящее время предложены различные хирургические доступы для удаления кисты: транспузырный транстригональный, внепузырный, передне- и заднесагиттальный [8, 11, 19]. Однако эти доступы травматичны, зачастую не обеспечивают полного удаления кисты, требуют тщательной предоперационной подготовки и связаны с риском осложнений, таких как нарушение функции тригональной мускулатуры, перфорация прямой кишки, травма сфинктерного аппарата мочевого пузыря и повреждение срамного нерва. Перспективными казались эндоскопические методы, заключающиеся в электрокоагуляции эпителиальной выстилки кисты, однако в большинстве случаев пациентам требовалась повторная операция, после которой, рецидивы развивались в 17 % случаев [7]. Кроме того, эндоскопическое лечение не обеспечивает полного удаления ткани простатической маточки, что может приводить к ее неоплазии.
С внедрением лапароскопии доступ к ретропузырному пространству стало малотравматичнее и безопаснее. Лапароскопия обеспечивает условия для полного удаления с хорошим косметическим результатом, а также проведения полноценной ревизии малого таза при сопутствующей патологии. Многократное увеличение изображения позволяет четко дифференцировать структуры кисты, семявыносящих протоков, стенки мочевого пузыря и т.д. [8]. Идентификация кисты простатической маточки в большинстве описанных случаев проводится при помощи интраоперационной цистоскопии, при которой можно контролировать уровень перевязки шейки кисты для исключения ее неполного удаления и сужения уретры в месте наложения лигатуры.
Также описано успешное применение робот-ассистированных операций в лечении кисты простатической маточки у взрослых [20].
Таким образом, анализ данных литературы показал, что все больше авторов склоняются к хирургическому удалению патологической простатической маточки для профилактики вышеописанных осложнений. В связи с этим представляем собственное клиническое наблюдение.
Пациент А. 4 лет поступил в отделение детской хирургии ФГБУ «Центральная клиническая больница с поликлиникой» УДП РФ с диагнозом «мошоночная форма гипоспадии, состояние после неоднократных оперативных пособий» .

Из анамнеза известно, что в возрасте 2лет по месту жительства выполнено выпрямление полового члена по поводу его выраженного искривления. Через 6 мес. в той же клинике проведена уретропластика по Duplay. В послеоперационном периоде отмечалось подтекание мочи помимо уретрального катетера, что стало причиной мочевого затека и как следствие – двух свищевых отверстий по средней трети ствола полового члена и в области пеноскротального угла. В последующем мочеиспускание у ребенка происходило через проксимальный свищ. В возрасте 3 лет 6 мес. ребенок госпитализирован в ГДКБ им Н. Ф. Филатова, где сформированная ранее уретра расценена как несостоятельная вследствие ее стенозирования до диаметра катетера 4 Ch, в связи с чем выполнено ее иссечение и сформирована площадка неоуретры из слизистой щеки. В возрасте 4 лет ребенок поступил в детское хирургическое отделение ФГБУ «ЦКБ с поликлиникой» УДП РФ для выполнения второго этапа буккальной пластики уретры. Учитывая жалобы на постоянное подтекание мочи, воспалительные изменения в анализах мочи на протяжении жизни ребенка, а также неудовлетворительные результаты ранее выполненных пластик, проведено дополнительное обследование. Экскреторная и микционная урография не обнаружила патологии. При МРТ органов малого таза выявлено жидкостное образование, расположенное между предстательной железой и прямой кишкой, овальной формы размером 5×7×17 мм (рис. 1). Семенные пузырьки с четкими контурами однородной структуры. При уретроцистоскопии под уплощенным семенным бугорком выявлено отверстие, ведущее в полость с гладкими стенками, заполненную мутновато-желтой жидкостью с хлопьями и микролитами (рис. 2). На основании полученных данных поставлен диагноз «киста простатической маточки». Данные анамнеза (неоднократные оперативные вмешательства с неудовлетворительным исходом), частичное недержание мочи, рецидивирующая лейкоцитурия явились показанием к первоочередному удалению кисты простатической маточки.
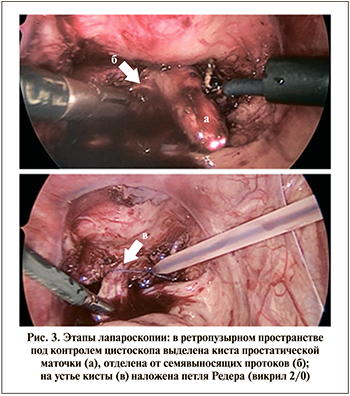 Проведены лапароскопия и цистоскопия. Цистоскоп № 9,0 Ch введен в полость кисты. Мочевой пузырь фиксирован к передней брюшной стенке тракционными швами. Свет цистоскопа был использован в качестве ориентира. Киста простатической маточки остро и при помощи электрокоагулятора выделена из окружающих тканей. С особой деликатностью отделены от дна кисты семявыносящие протоки, интимно спаянные с ней (рис. 3). Дальнейшее выделение до шейки не вызвало технических трудностей. Под контролем цистоскопии и лапароскопии на шейку кисты наложена петля Редера (викрил 2/0), киста отсечена. В мочевой пузырь установлен катетер Фоллея на 8 сут., после удаления которого ребенок выписан из стационара в удовлетворительном состоянии.
Проведены лапароскопия и цистоскопия. Цистоскоп № 9,0 Ch введен в полость кисты. Мочевой пузырь фиксирован к передней брюшной стенке тракционными швами. Свет цистоскопа был использован в качестве ориентира. Киста простатической маточки остро и при помощи электрокоагулятора выделена из окружающих тканей. С особой деликатностью отделены от дна кисты семявыносящие протоки, интимно спаянные с ней (рис. 3). Дальнейшее выделение до шейки не вызвало технических трудностей. Под контролем цистоскопии и лапароскопии на шейку кисты наложена петля Редера (викрил 2/0), киста отсечена. В мочевой пузырь установлен катетер Фоллея на 8 сут., после удаления которого ребенок выписан из стационара в удовлетворительном состоянии.
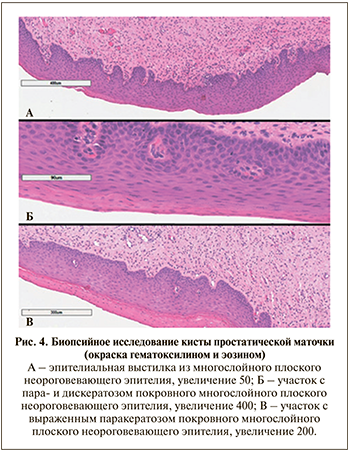
При гистологическом исследовании: стенка кисты образована фиброзной и гладкомышечной тканью и выстлана многослойным плоским неороговевающим эпителием, характерным для кисты простатической маточки (рис. 4).
Через 3 мес. после удаления кисты простатической маточки выполнен второй этап пластики уретры до верхушки головки полового члена. Предоперационная цистоскопия выявила точечный слепо заканчивающийся дефект слизистой в области устья кисты простатической маточки. Проведена пластика уретры по Dupley—Smitt. Послеоперационное течение гладкое, уретральный катетер удален на 8-е сутки. Катамнез прослежен в течение года: жалоб нет, мочеиспускание широкой струей, недержания мочи нет, общий анализ мочи без патологических изменений.
 Кистозно-измененная простатическая маточка – редкое клиническое наблюдение в педиатрической практике, ассоциирующееся главным образом с тяжелыми формами гипоспадии и другими пороками урогенитального тракта [2, 4, 8, 11]. Истинную встречаемость данной патологии установить трудно в связи с отсутствием патогномоничной симптоматики. Большинство первичных пациентов не подвергаются углубленному урологическому обследованию, и подозрение врачей на наличие сопутствующей патологии, как и в нашем наблюдении, возникает лишь при неудовлетворительных результатах оперативного лечения [1, 8, 12–14].
Кистозно-измененная простатическая маточка – редкое клиническое наблюдение в педиатрической практике, ассоциирующееся главным образом с тяжелыми формами гипоспадии и другими пороками урогенитального тракта [2, 4, 8, 11]. Истинную встречаемость данной патологии установить трудно в связи с отсутствием патогномоничной симптоматики. Большинство первичных пациентов не подвергаются углубленному урологическому обследованию, и подозрение врачей на наличие сопутствующей патологии, как и в нашем наблюдении, возникает лишь при неудовлетворительных результатах оперативного лечения [1, 8, 12–14].
Причиной развития осложнений в первую очередь следует считать рецидивирующие инфекции мочевыводящих путей в связи с застоем мочи в полости кисты и постоянным ее подтеканием. Устранение этого фактора позволило в нашем случае избежать несостоятельности швов неоуретры при повторном оперативном лечении.
Наше наблюдение показало неинформативность трансабдоминального УЗИ в качестве скринингового исследования. Экскреторная и микционная урографии также не способствовали диагностике патологии. Только МРТ позволила четко идентифицировать ретропузырное кистозное образование, имеющее сообщение с задней уретрой. Окончательный диагноз, как и в большинстве публикаций, удалось выставить только по данным цистоскопии [1, 4, 6–8]. Заполненная мутной мочой и мелкими конкрементами полость с устьем под семенным бугорком не вызывает сомнений в источнике хронической инфекции и показаниях к ее удалению.
Консервативное лечение не позволяет радикально излечить пациента, обеспечить профилактику осложнений и обрекает пациента на пожизненное применение антибактериальных препаратов, уросептиков и катетеризаций с инстиляциями. В связи с этим мы отдали предпочтение хирургическому методу лечения. Ввиду травматичности открытой хирургии мы не рассматривали ее в качестве оперативного доступа. Достаточный опыт, на наш взгляд, лапароскопических вмешательств при различной патологии брюшной полости и забрюшинного пространства у детей позволил нам применить данный доступ в этом наблюдении.
Представленное клиническое наблюдение продемонстрировало эффективность лапароскопических методов в лечении порока развития мочеполовой системы — кисты простатической маточки, которая клинически проявлялась постоянным подтеканием мочи и поддержанием хронической инфекции уретры, что обусловливало осложнения оперативного лечения гипоспадии. Как показал анализ литературы, при проксимальных формах гипоспадии частота встречаемости аномально увеличенной простатической маточки достигает 75%. В связи с этим в дооперационный алгоритм обследования детей с проксимальными формами гипоспадии, наряду с общепринятыми методами обязательно долны быть включены цистоскопия и МРТ/МСКТ малого таза.



